Pytanie 1
Promieniowanie jonizujące pośrednio to
Wynik: 35/40 punktów (87,5%)
Wymagane minimum: 20 punktów (50%)
Promieniowanie jonizujące pośrednio to
Co określa M₀ w systemie klasyfikacji nowotworów TNM?
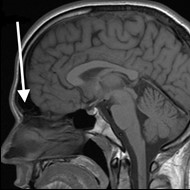
Na obrazie rezonansu magnetycznego głowy strzałką wskazano zatokę
W systemie międzynarodowym czwarty górny ząb mleczny po stronie prawej oznacza się symbolem
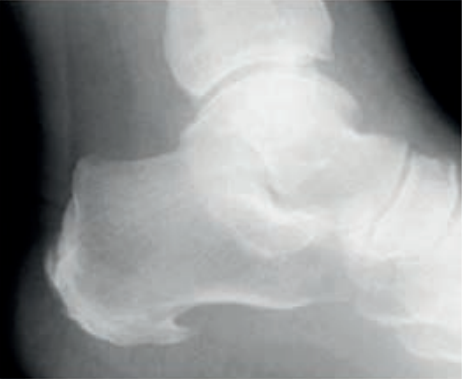
Co zostało uwidocznione na zamieszczonym radiogramie?
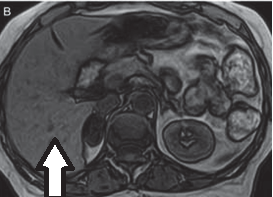
Na przekroju poprzecznym rezonansu magnetycznego strzałką oznaczono
Jakie źródła promieniowania stosowane są w brachyterapii?
Do zdjęcia rentgenowskiego żeber w projekcji skośnej tylnej pacjenta należy ustawić
Zadaniem technika elektroradiologa w pracowni naczyniowej jest
Którym skrótem oznacza się tomografię komputerową wysokiej rozdzielczości?
W pozytonowej emisyjnej tomografii komputerowej PET radioznacznik podawany jest pacjentowi najczęściej
Którą kasetę należy wykorzystać do wykonania rentgenogramu klatki piersiowej w projekcji bocznej u 35-letniej pacjentki o wzroście 165 cm i wadze 54 kg?
W standardowym badaniu elektrokardiologicznym elektrodę C4 należy umocować
Który program wtórnej rekonstrukcji obrazów TK pozwala na odwzorowanie wnętrza jelita grubego, tchawicy i oskrzeli?
W badaniu PETCT radioizotop ulega
Którym skrótem w badaniu spirometrycznym oznaczana jest pojemność życiowa płuc?
Który radioizotop jest stosowany w diagnostyce i terapii raka tarczycy?
Rozpoczęcie badania TK nerek po 20-30 sekundach od początku podania środka kontrastowego umożliwia diagnostykę
Hiperfrakcjonowanie dawki w teleradioterapii polega na napromienianiu 2 do 3 razy dziennie dawką frakcyjną
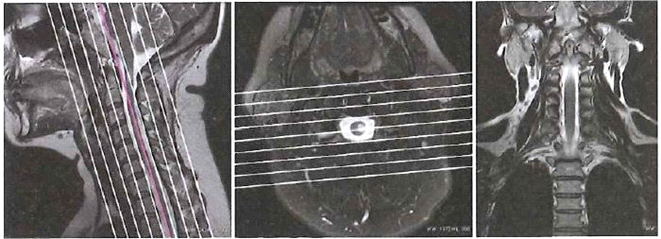
Obrazy MR kręgosłupa szyjnego przedstawiają etap planowania badania warstw
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz
Pracownia radioterapii z przyspieszaczem liniowym jest obszarem
W brachyterapii MDR stosowane są dawki promieniowania
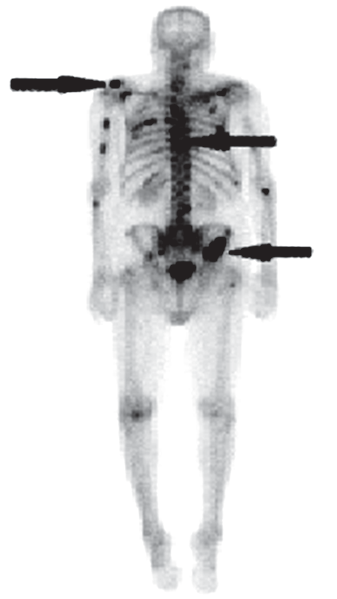
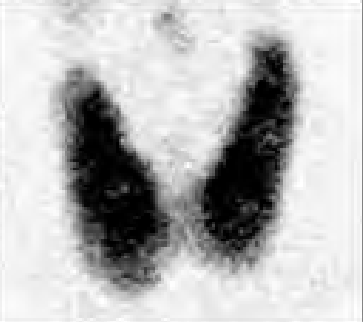
Na którym obrazie zarejestrowano badanie scyntygraficzne?
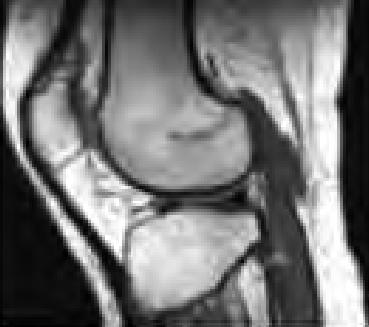
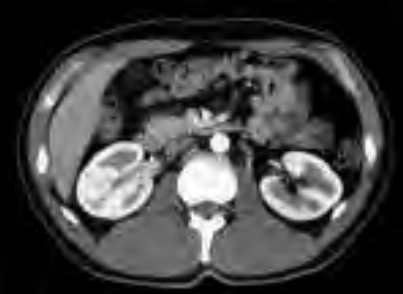
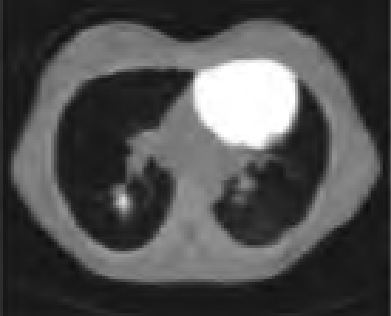
Które ciało obce w obszarze badania nie stanowi przeciwwskazania do wykonania MR?
W diagnostyce metodą rezonansu magnetycznego biorą udział
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
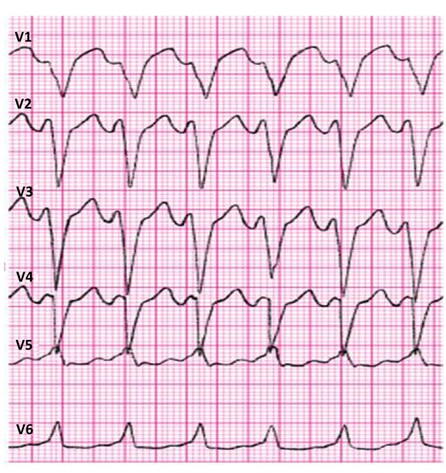
Które zaburzenie rytmu serca zarejestrowano na elektrokardiogramie?
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
W badaniu MR czas repetycji TR jest parametrem określającym odstęp czasu między
Zdjęcie zatok przynosowych wykonuje się w pozycji
Pozytywny środek cieniujący najczęściej stosowany w rentgenodiagnostyce powinien charakteryzować się
W badaniu cystografii wstępującej środek kontrastowy należy podać
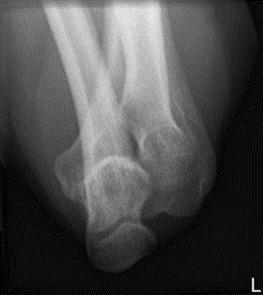
Którą strukturę anatomiczną i w jakiej projekcji uwidoczniono na radiogramie?
Bezwzględnym przeciwwskazaniem do wykonania badania rezonansem magnetycznym jest
W scyntygrafii wykorzystywane są głównie radioizotopy emitujące promieniowanie
Efekt „tea cup” widoczny jest na mammografach wykonanych w projekcji
Wskazaniem do wykonania badania spirometrycznego jest
Droga przewodnictwa powietrznego fali akustycznej przebiega przez
Na scyntygramie kości strzałkami oznaczono ogniska