Pytanie 1
Jakie jest stężenie molowe kwasu siarkowego(VI) o zawartości 96% i gęstości 1,84 g/cm3?
Wynik: 37/40 punktów (92,5%)
Wymagane minimum: 20 punktów (50%)
Jakie jest stężenie molowe kwasu siarkowego(VI) o zawartości 96% i gęstości 1,84 g/cm3?
Jaką masę siarczanu(VI) miedzi(II)-woda(1/5) należy poddać suszeniu, aby otrzymać 300 g soli bezwodnej?
| CuSO4 · 5H2O → CuSO4 + 5H2O |
| (MCuSO4·5H2O = 249,5 g/mol, MCuSO4 = 159,5 g/mol, MH2O = 18,0 g/mol) |
Na rysunku przedstawiono aparat
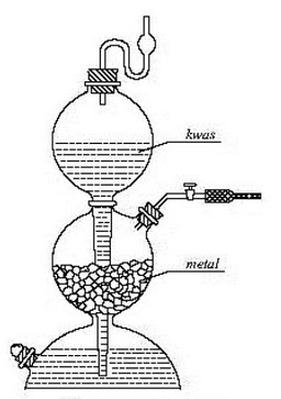
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Po połączeniu 50 cm3 wody z 50 cm3 alkoholu etylowego, objętość otrzymanej mieszanki jest poniżej 100 cm3. Zjawisko to jest spowodowane
W chemicznym laboratorium apteczka pierwszej pomocy powinna zawierać
Aby otrzymać roztwór AgNO3 (masa molowa AgNO3 to 169,8 g/mol) o stężeniu 0,1 mol/dm3, należy
Podczas reakcji chlorku żelaza(III) z wodorotlenkiem potasu dochodzi do wytrącenia wodorotlenku żelaza(III) w formie
Butle gazowe (czasy butli) napełnione wodorem są oznaczone kolorem
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Reagenty o najwyższej czystości to reagenty
Przedstawiony zestaw stosowany jest w laboratorium do przeprowadzenia procesu
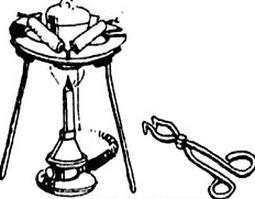
Aby przygotować roztwór wzorcowy potrzebny do oznaczania miana, konieczne jest użycie odczynnika chemicznego o czystości przynajmniej
Wskaż typy reakcji I, II, III na podstawie ich równań chemicznych.
I. \( 2\, \text{Mg} + \text{O}_2 \rightarrow 2\, \text{MgO} \)
II. \( \text{Cu(OH)}_2 \rightarrow \text{CuO} + \text{H}_2\text{O} \)
III. \( \text{Zn} + \text{HCl} \rightarrow \text{ZnCl}_2 + \text{H}_2 \)
Komora przeszklona w formie dużej szafy, wyposażona w wentylator, która zapobiega wydostawaniu się szkodliwych substancji do atmosfery laboratorium oraz chroni przed pożarami i eksplozjami, to
Na rysunku przedstawiono proces
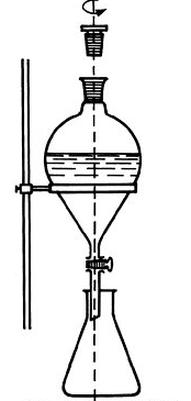
Nie należy używać do czyszczenia szklanych naczyń laboratoryjnych
Ile masy kwasu mrówkowego jest wymagane do uzyskania 11,2 dm3 tlenku węgla(II) (w warunkach normalnych) w procesie odwodnienia kwasu mrówkowego (M = 46 g/mol) za pomocą kwasu siarkowego(VI), zakładając efektywność procesu na poziomie 70%?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Oblicz masę wapienia, który został rozłożony, jeśli w trakcie reakcji uzyskano 44,8 dm3 CO2 (w warunkach standardowych).
MC = 12 g/mol, MCa = 40 g/mol, MO = 16 g/mol
Jakim kolorem oznacza się instalację gazową w laboratorium analitycznym?
Zawarty fragment instrukcji odnosi się do
Po dodaniu do kolby Kjeldahla próbki analizowanego materiału, kwasu siarkowego(VI) oraz katalizatora, należy delikatnie ogrzewać zawartość kolby za pomocą palnika gazowego. W początkowym etapie ogrzewania zawartość kolby wykazuje pienienie i zmienia kolor na ciemniejszy. W tym czasie należy przeprowadzać ogrzewanie bardzo ostrożnie, a nawet z przerwami, aby uniknąć "wydostania się" czarnobrunatnej masy do szyjki kolby.
Substancje utleniające opisuje piktogram

To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Po rozpuszczeniu substancji w kolbie miarowej, należy odczekać przed dopełnieniem jej wodą "do kreski" miarowej. Taki sposób postępowania jest uzasadniony
W trakcie destylacji cieczy wykorzystuje się tzw. kamienie wrzenne, ponieważ
Chemikalia, dla których upłynął okres przydatności,
Przedstawiony sposób dotyczy pobierania próbki wody do przeprowadzenia badań
| Sposób pobierania próbki wody do przeprowadzenia badań: - próbki pobrać do sterylnych butelek; - przed przystąpieniem do pobierania wody zdjąć z kurka wszelkie urządzenia, zeskrobać zanieczyszczenia, następnie całkowicie otwierając i zamykając zawór, wielokrotnie płukać; - metalowy kurek wysterylizować płomieniem, a kurek z tworzywa sztucznego alkoholem etylowym; - kurek otworzyć do połowy przepływu i spuszczać wodę przez około 2-3 minuty do osiągnięcia stałej temperatury; - pobrać próbkę wody napełniając butelkę do około ¾ objętości i natychmiast zamknąć korkiem. |
Wskaż definicję fiksanali?
Jednym z sposobów oddzielania jednorodnych mieszanin jest
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Aby uzyskać całkowicie bezwodny Na2CO3, przeprowadzono prażenie 143 g Na2CO3·10H2O (M = 286 g/mol). Po upływie zalecanego czasu prażenia odnotowano utratę masy 90 g. W związku z tym prażenie należy
Zabieg, który wykonuje się podczas pobierania próbki wody do analizy, mający na celu zachowanie jej składu chemicznego w trakcie transportu, określa się mianem
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Określ, jakie informacje powinny być zarejestrowane w ewidencji wydania substancji niebezpiecznych, stosowanych w badaniach laboratoryjnych?
Na zdjęciu przedstawiono proces

Jak nazywa się naczynie o płaskim dnie, które wykorzystuje się do pozyskiwania substancji stałej poprzez stopniowe odparowanie rozpuszczalnika z roztworu?
Oblicz, ile moli gazu można zebrać w pipecie gazowej o pojemności 500 cm3, jeśli gaz będzie gromadzony w warunkach normalnych. (W normalnych warunkach jeden mol gazu ma objętość 22,4 dm3)
Jakiego odczynnika chemicznego, oprócz Na2Cr2O7, należy użyć do sporządzenia mieszaniny chromowej do czyszczenia sprzętu szklarskiego w laboratorium?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.