Pytanie 1
Czym jest efekt wspólnego jonu?
Wynik: 29/40 punktów (72,5%)
Wymagane minimum: 20 punktów (50%)
Czym jest efekt wspólnego jonu?
Drobnoustroje posiadające zdolność do rozkładu białek oraz peptydów charakteryzują się właściwościami
W celu wykrycia cukrów metodą Tollensa należy wybrać zestaw sprzętu oznaczonego w tabeli numerami:
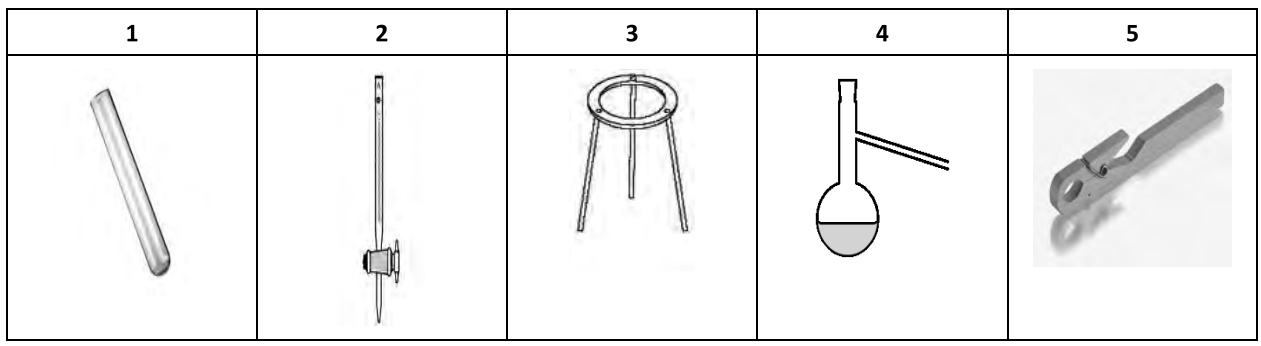
Wymaganie chemiczne na tlen ChZT określa ilość
Przewodnictwo właściwe roztworu \( \text{KNO}_3 \) wynosi \( 8{,}9 \cdot 10^{-3} \, \text{S} \cdot \text{cm}^{-1} \). W jakiej odległości powinny być ustawione elektrody o powierzchni \( 5 \, \text{cm}^2 \), aby przewodnictwo roztworu wynosiło \( 5 \, \text{mS} \)?
Wzór do obliczeń:$$ \frac{1}{R} = G = \frac{\kappa \cdot S}{l} $$gdzie:
\( R \) – oznacza opór przewodnika
\( G \) – przewodnictwo elektryczne
\( \kappa \) – przewodnictwo właściwe
\( S \) – powierzchnia elektrod
\( l \) – odległość elektrod względem siebie
Na schemacie przedstawiono
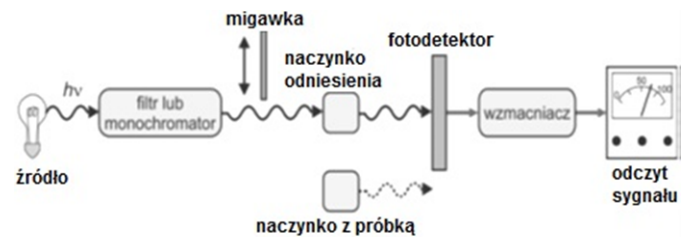
pH wodnego roztworu gleby jest miarą kwasowości
Na rysunku przedstawiono schemat aparatury do
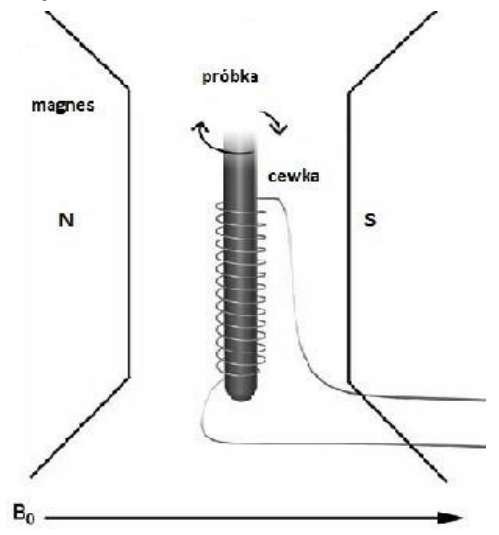
W celu wykonania posiewu redukcyjnego należy nanieść drobnoustroje na podłoże, a następnie
| A. | 1. wyżarzyć ezę, 2. obrócić szalkę, 3. ponownie nanosić drobnoustroje, zahaczając przynajmniej raz o wcześniejszą ścieżkę. |
| B. | 1. nie wyżarzać ezy, 2. obrócić szalkę, 3. ponownie nanosić drobnoustroje, zahaczając przynajmniej raz o wcześniejszą ścieżkę. |
| C. | 1. wyżarzyć ezę, 2. obrócić szalkę, 3. ponownie nanosić drobnoustroje, nie zahaczając ani razu o wcześniejszą ścieżkę. |
| D. | 1. wyżarzyć ezę, 2. pozostawić szalkę w tym samym miejscu, 3. ponownie nanosić drobnoustroje, zahaczając przynajmniej raz o wcześniejszą ścieżkę. |
W Polsce normy dotyczące pyłów zawieszonych PM10 są określone na trzech poziomach (dobowych):
- poziom dopuszczalny 50 ug/m3 - oznacza, że jakość powietrza nie jest zadowalająca, ale nie wywołuje poważnych skutków dla zdrowia ludzi.
- poziom informacyjny 200 ug/m3 - oznacza, że stan powietrza jest zły i należy ograniczyć aktywności na świeżym powietrzu, gdyż normę przekroczono czterokrotnie.
- poziom alarmowy 300 ug/m3 - wskazuje, że jakość powietrza jest bardzo zła, norma przekroczona sześciokrotnie i konieczne jest zdecydowane ograniczenie pobytu na zewnątrz, a najlepiej pozostać w domu, szczególnie dla osób chorych.
Na stacji Monitoringu Środowiska przeprowadzono pomiary zanieczyszczenia powietrza pyłem PM10, uzyskując średnią dobową wartość 0,25 mg/m3. Z analizy wynika, że
Wskaż zestaw kationów, które można zidentyfikować za pomocą próby płomieniowej.
| A. Ag+, Ni2+ |
| B. Mg2+, Al3+ |
| C. Na+, Ca2+ |
| D. Fe2+, Fe3+ |
Który ze sprzętów przedstawionych na rysunkach jest niezbędny do przygotowania 250 cm3 mianowanego roztworu NaOH z fiksanalu?
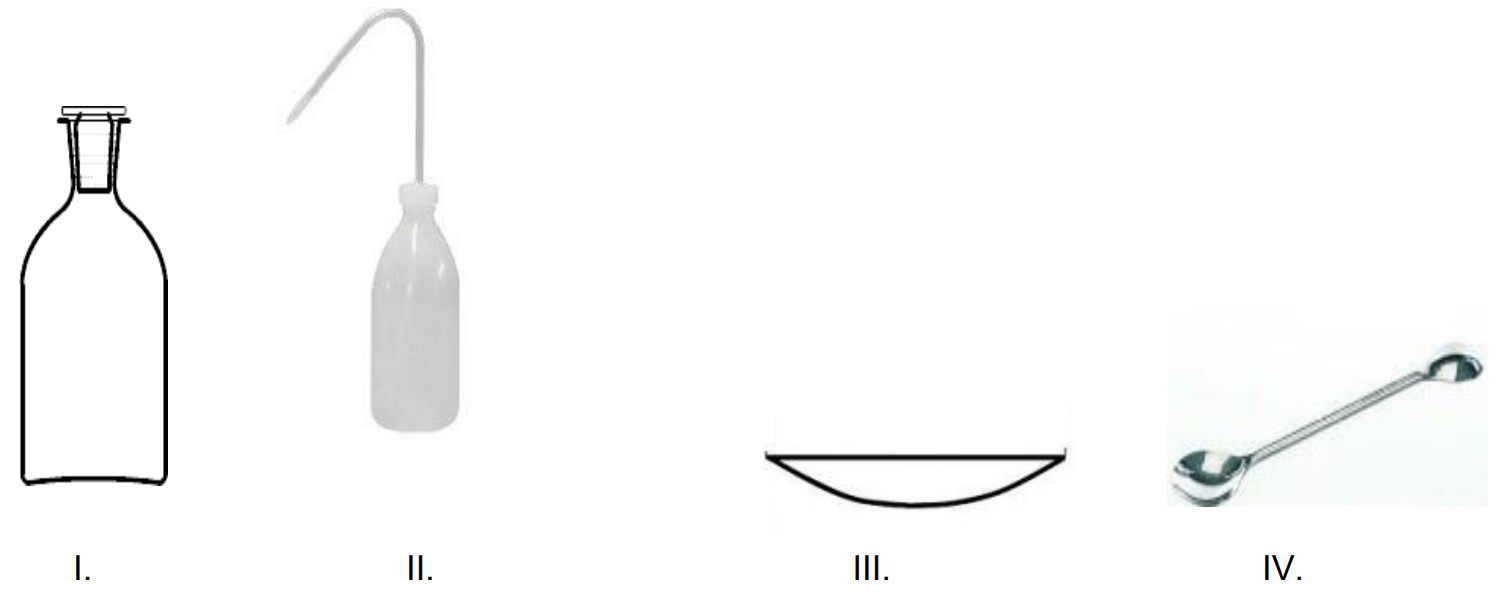
Metoda analityczna opierająca się na pomiarze kąta rotacji płaszczyzny światła spolaryzowanego to
Oznaczanie jonów cynku przy użyciu EDTA stanowi przykład miareczkowania
W jakiej proporcji molowej EDTA reaguje z jonami Zn2+?
Przy separacji osadu z roztworu za pomocą wirówki laboratoryjnej istotne jest, aby rotor wirówki
Aby przeprowadzić analizę gleby, przygotowuje się jej zawiesinę w wodzie destylowanej lub w roztworze neutralnej soli, na przykład KCl, w celu określenia jej
W dwóch niezidentyfikowanych probówkach znajdują się roztwory: w jednej - glukozy, a w drugiej - sacharozy. Jakiego odczynnika należy użyć, aby rozpoznać glukozę?
Woda pobrana do analizy mikrobiologicznej została rozcieńczona w proporcji 1:1000. Z uzyskanej mieszanki pobrano 0,1 ml, który następnie umieszczono na szalce z pożywką. Po hodowli na szalce zaobserwowano 10 jtk. Jakie było stężenie bakterii w analizowanej wodzie?
W zamieszczonej informacji przedstawiono równania reakcji zachodzące podczas oznaczania chlorków metodą
| Ag+ + Cl- → AgCl ↓ Ag+ + SCN- → AgSCN ↓ Fe3+ + SCN- → Fe(SCN)2+ |
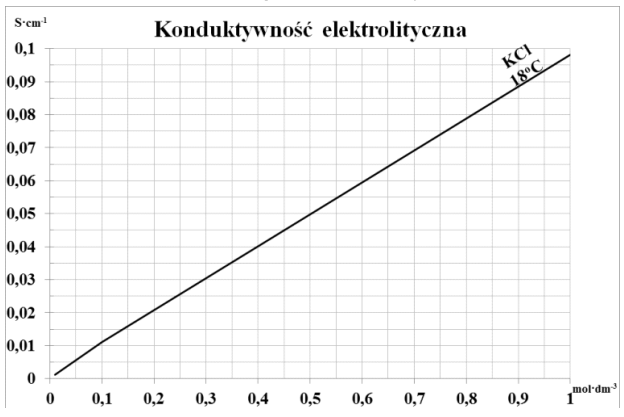
W celu wyznaczenia stężenia badanej próbki chlorku potasu, wykonano krzywą wzorcową zależności konduktywności elektrolitycznej od stężenia. Przewodność badanego roztworu wyniosła 0,045 S∙cm-1. Stężenie badanego roztworu KCl wynosi
Przedstawione reakcje zachodzą w produktach żywnościowych podczas fermentacji
| C12H22O11 + H2O → C6H12O6 + C6H12O6 |
| C6H12O6 → 2 CH3 −CH(OH) −COOH |
Do zmiany objętości próbki roztworu NaOH wykorzystano 10,0 cm3 roztworu HCl o stężeniu 0,1000 mol/dm3. Jaką ilość NaOH (M = 40 g/mol) zawierała próbka?
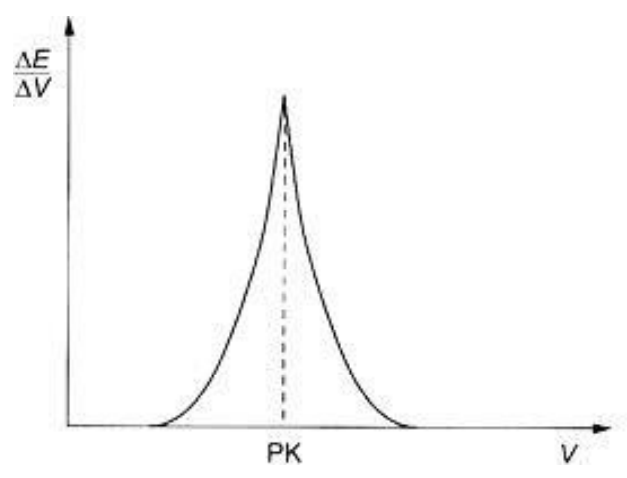
Na rysunku przedstawiono wyznaczanie punktu końcowego miareczkowania metodą
Twardość całkowita wody
Związki lotne, które występują w wielu roślinach i mogą być wydobywane, np. poprzez destylację z parą wodną lub dzięki ciągłej ekstrakcji w aparacie Soxhleta, to
W badanym powietrzu zawartość mikroorganizmów wyniosła 33,33 w 10 dm3. Zgodnie z zamieszczonymi normami powietrze takie uważa się za
| Stopień zanieczyszczenia | Ogólna liczba bakterii w 1 m3 |
|---|---|
| Niezanieczyszczone | poniżej 1000 |
| Średnio zanieczyszczone | od 1000 do 3000 |
| Silnie zanieczyszczone | powyżej 3000 |
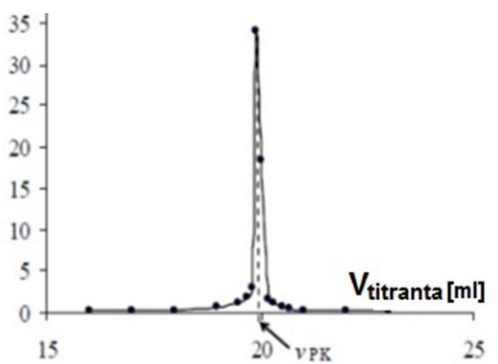
Sporządzono wykres potencjometrycznego miareczkowania alkacymetrycznego. W jaki sposób należy opisać oś Y?
| A. | ΔpH/ΔVtitranta |
| B. | ΔSEM/ΔVtitranta |
| C. | pH/ΔVtitranta |
| D. | SEM/ΔVtitranta |
Zjawisko polegające na przepuszczaniu rozpuszczalnika przez membranę półprzepuszczalną z roztworu o wyższym stężeniu do roztworu o niższym stężeniu substancji rozpuszczonej określa się mianem
W wyniku oznaczenia wagowego otrzymano 0,2451 g tlenku żelaza(III). Ile gramów żelaza zawierała analizowana próbka?
| MFe = 55,845 g/mol, MO = 15,999 g/mol |
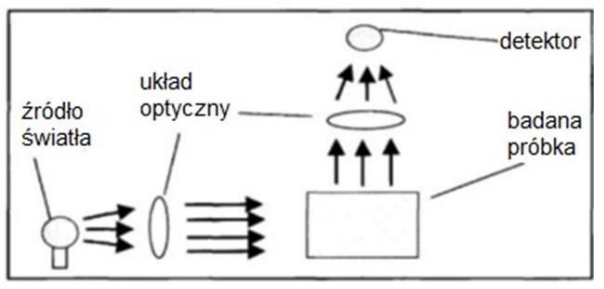
Na ilustracji przedstawiono bieg promieni świetlnych
Wskaź zespół substancji, które przyczyniają się do twardości niewęglanowej wody?
W równaniu dotyczącym iloczynu rozpuszczalności siarczanu(VI) baru: Kso = [Ba2+][SO42-], jonowe stężenia Ba2+ oraz SO42- są przedstawione jako
W laboratorium anaerostat wykorzystywany jest
Metoda Mohra do oznaczania chlorków polega na
Uwzględniając zamieszczoną informację, dobierz metodę stosowaną do oznaczania azotanów(V) w wodzie.
| W środowisku stężonego kwasu siarkowego(VI) jony azotanowe(V) ulegają reakcji z salicylanem sodu, dając kwas nitrosalicylowy, który pod wpływem zasad przechodzi w formę zjonizowaną o żółtym zabarwieniu. |
Zgodnie z zamieszczonym fragmentem metodyki postępowania analitycznego mineralizację próbki paszy należy przeprowadzić w kolbie
| Fragment metodyki postępowania analitycznego: |
| (...) Metoda służy do oznaczania zawartości białka w paszach na podstawie zawartości oznaczonego azotu. Próbka jest mineralizowana kwasem siarkowym(VI) w obecności katalizatora. Kwaśny roztwór jest alkalizowany za pomocą wodorotlenku sodu. Amoniak oddestylowany z zasadowego roztworu jest zbierany w znanej ilości roztworu kwasu siarkowego(VI), którego nadmiar jest z kolei miareczkowany roztworem wodorotlenku sodu. (...) |
Który nawóz, spośród wymienionych w tabeli, zawiera najwięcej azotu azotanowego?
| Tabela. Zawartość składnika czynnego w nawozach azotowych | |
|---|---|
| Nawóz | Zawartość składników, % |
| Saletra potasowa | N – 13,5% |
| Saletra magnezowa | N – 10,8% |
| Saletra amonowa | N – 34% (NH4+ – 17%, NO3- – 17%) |
| Saletra wapniowa | N – 14,5% |
| Siarczan amonu | N – 21% |
| Mocznik | N – 46% |
Wyznacz refrakcję molową (Rm) dla kwasu octowego korzystając z danych zawartych w tabeli.
Rm = ∑a ∙ Ra gdzie: a – liczba atomów jednego rodzaju, Ra – refrakcja atomowa

Jaką metodą dokonuje się oceny intensywności koloru karmelu?