Pytanie 1
Po zakończeniu badania angiograficznego należy zapisać w dokumentacji medycznej pacjenta:
Wynik: 23/40 punktów (57,5%)
Wymagane minimum: 20 punktów (50%)
Po zakończeniu badania angiograficznego należy zapisać w dokumentacji medycznej pacjenta:
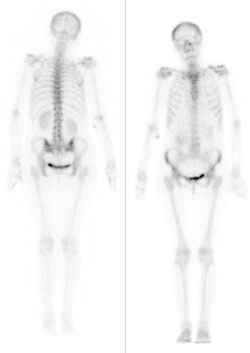
Na obrazie uwidoczniono
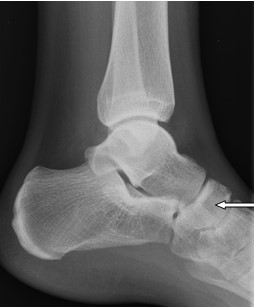
Na radiogramie strzałką oznaczono
Jednostką indukcji magnetycznej jest
Limfografia to badanie kontrastowe
W której projekcji należy wykonać badanie radiologiczne kręgosłupa lędźwiowego, by na otrzymanym zdjęciu wyrostki kręgów lędźwiowych układały się w charakterystyczny kształt piesków (teriera szkockiego)?
Który środek ochrony radiologicznej należy zastosować podczas badania czaszki 53-letniego pacjenta za pomocą tomografii komputerowej?
Parametrem krwi, który powinien zostać oznaczony u pacjenta przed wykonaniem badania MR z kontrastem jest
Która właściwość promieniowania X pozwala na skierowanie promienia centralnego na wybrany punkt topograficzny podczas wykonywania badania radiologicznego?
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
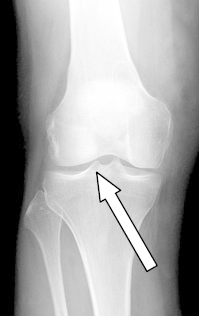
Którą strukturę anatomiczną oznaczono strzałką na radiogramie stawu kolanowego?
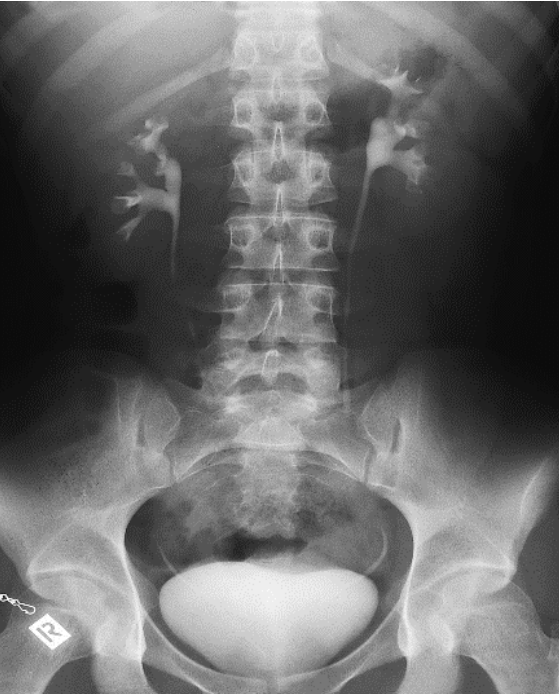
Na którym radiogramie uwidoczniona jest kamica nerkowa?
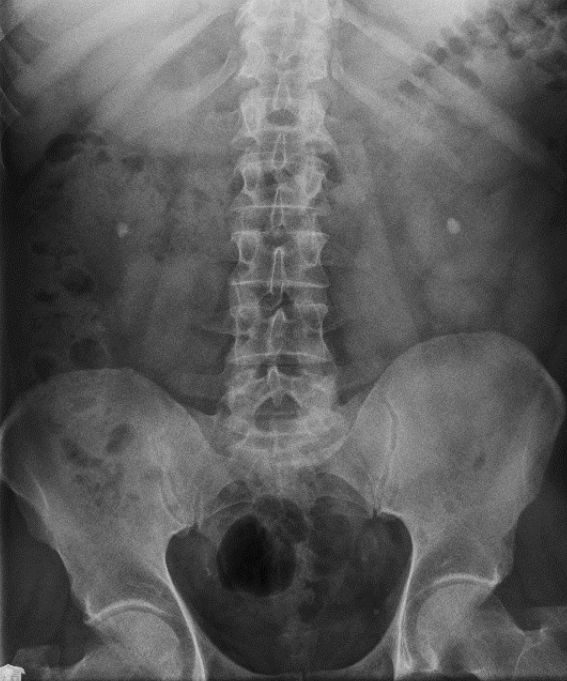
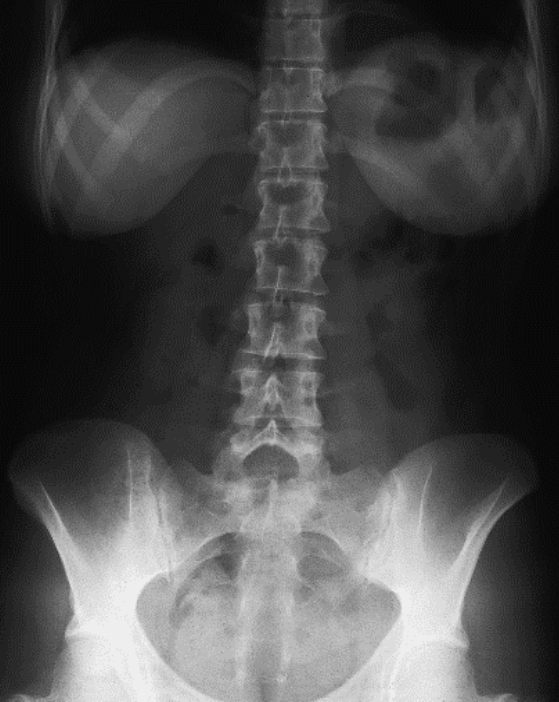
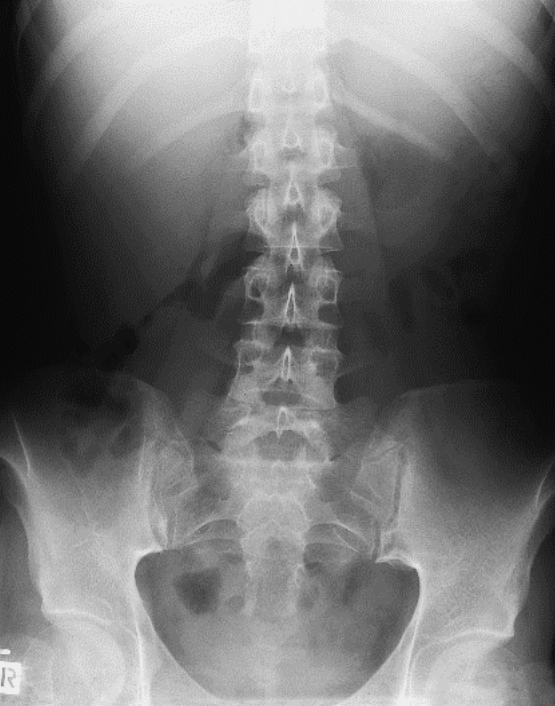
Do zdjęcia rentgenowskiego żeber w projekcji skośnej tylnej pacjenta należy ustawić
Powierzchnia gabinetu rentgenowskiego, w którym zainstalowany jest aparat rentgenowski wyposażony w oddzielną lampę, nie może być mniejsza niż
Dobierz dla standardowego pacjenta projekcję, pozycję i sposób ułożenia kasety o wymiarach 30 cm x 40 cm do zdjęcia przeglądowego układu moczowego.
| Projekcja | Pozycja | Ułożenie kasety | |||
|---|---|---|---|---|---|
| 1. | AP | 3. | stojąca | 5. | poprzeczne |
| 2. | PA | 4. | leżąca | 6. | podłużne |
Na rentgenogramie stopy uwidocznione jest złamanie
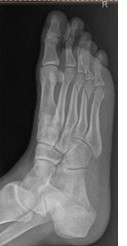
Jaki jest cel stosowania bolusa w radioterapii?
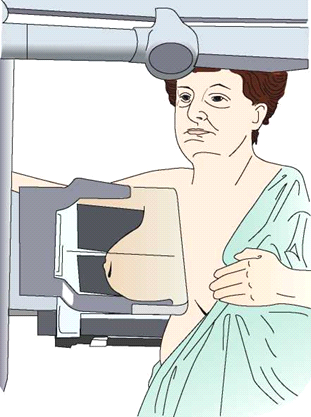
Ilustracja przedstawia pozycjonowanie pacjentki do badania mammograficznego w projekcji
W którym miejscu, zgodnie z zasadami wykonywania badania EKG, należy umocować żółtą elektrodę przedsercową V2?
Do zdjęcia rentgenowskiego kręgosłupa piersiowego w projekcji AP pacjenta należy ułożyć
Obrazy DDR są tworzone w trakcie
Standardowe badanie urografii polega na podaniu pacjentowi środka kontrastującego
W medycynie nuklearnej wykorzystuje się:
Badanie cewki moczowej polegające na wstecznym wprowadzeniu środka kontrastowego to
W których projekcjach podstawowych wykonuje się standardowe badanie mammograficzne?
Radiofarmaceutyki stosowane w medycynie nuklearnej powstają dzięki połączeniu radioizotopu
Audiometria impedancyjna polega na pomiarze
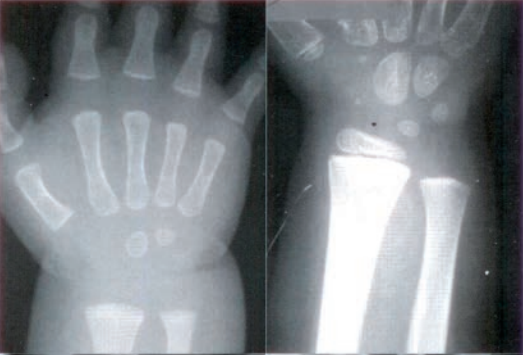
Zestaw rentgenogramów przedstawia
Promieniowanie jonizujące pośrednio to
Który radioizotop jest stosowany w scyntygrafii perfuzyjnej mózgu?
W zapisie EKG prawidłowego rytmu zatokowego wszystkie załamki P są
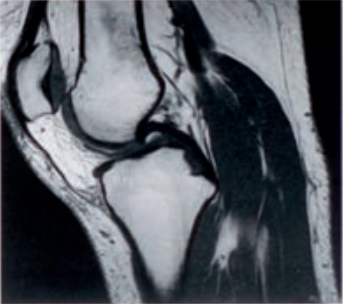
Którą metodę badania zastosowano w obrazowaniu stawu kolanowego?
Bezwzględnym przeciwwskazaniem do wykonania badania rezonansem magnetycznym jest
Elementem systemu rejestracji obrazu, w którym fotony promieniowania X są bezpośrednio konwertowane na sygnał elektryczny, jest
Jaki rozmiar kasety należy zastosować, wykonując standardowe zdjęcie stawu kolanowego w projekcji bocznej?
Przy ułożeniu do zdjęcia kręgów szyjnych CIII-CVII w projekcji przednio-tylnej lampa może być odchylona o kąt
HRCT (high-resolution computed tomography) jest metodą obrazowania TK
Wskaż osłonę radiologiczną, która jest stosowana w pracowniach radiodiagnostyki stomatologicznej.




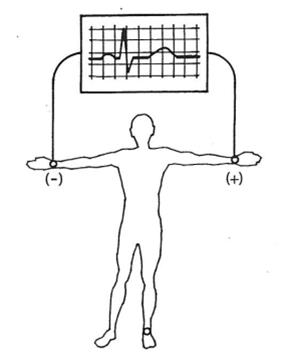
Które odprowadzenie elektrokardiograficzne przedstawiono na ilustracji?
W celu wykonania badania scyntygraficznego układu kostnego radiofarmaceutyk należy podać pacjentowi