Pytanie 1
Podczas badania EEG otwarcie oczu powoduje
Wynik: 35/40 punktów (87,5%)
Wymagane minimum: 20 punktów (50%)
Podczas badania EEG otwarcie oczu powoduje
Radiofarmaceutyki stosowane w medycynie nuklearnej powstają dzięki połączeniu radioizotopu
Która struktura może być oknem akustycznym w badaniu ultrasonograficznym?
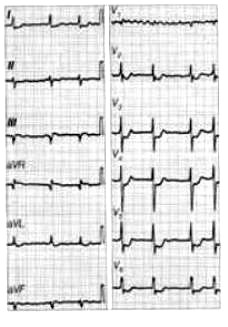
Na elektrokardiogramie uwidoczniono
W badaniu cystografii wstępującej środek kontrastowy należy podać
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
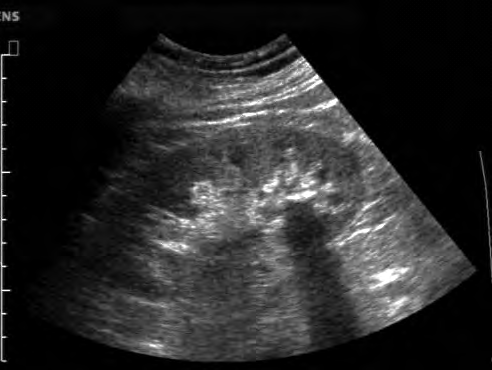
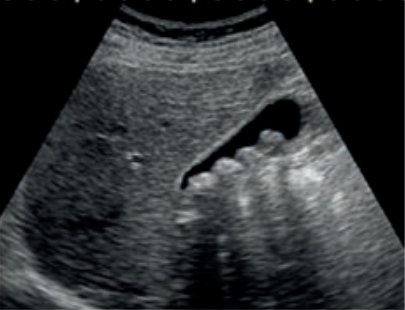
Na obrazie ultrasonograficznym jamy brzusznej uwidoczniono
Kolonoskopia to badanie, które ma na celu ocenę błony śluzowej
Jakie są wielkości mocy dawki stosowanej w brachyterapii HDR?
Hiperfrakcjonowanie dawki w radioterapii oznacza napromieniowywanie pacjenta
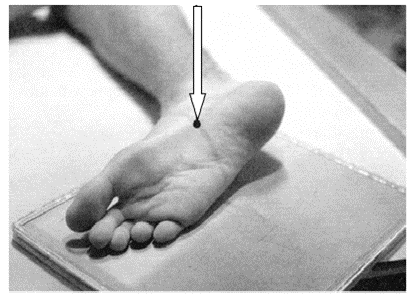
Na zamieszczonej ilustracji przedstawiono ułożenie pacjenta do wykonania zdjęcia rentgenowskiego
Która sekwencja obrazowania MR wykorzystuje impulsy RF o częstotliwości rezonansowej tłuszczu do tłumienia sygnału pochodzącego z tkanki tłuszczowej?
Przemiana promieniotwórcza radu w ren opisana wzorem \( {}_{88}^{226}\text{Ra} \to {}_{86}^{222}\text{Rn} + {}_{2}^{4}\text{He} \) jest rozpadem
Jakie wiązki promieniowania emituje medyczny akcelerator liniowy?
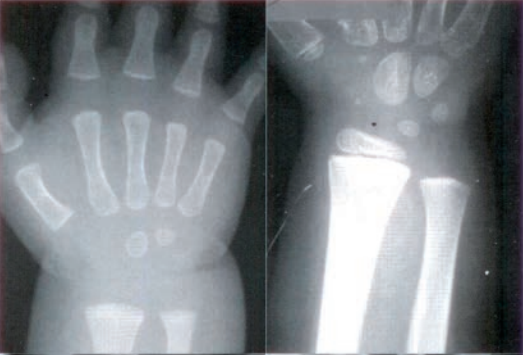
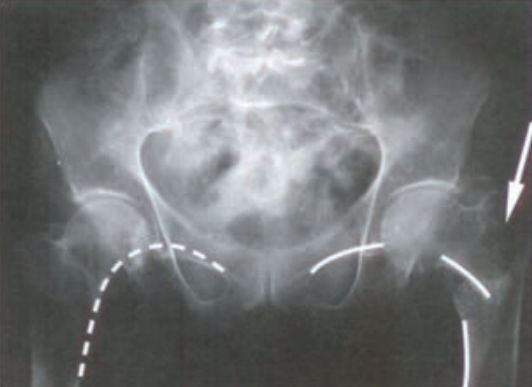
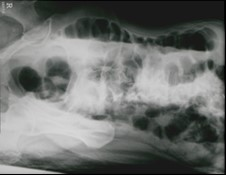
Radiogram przedstawia
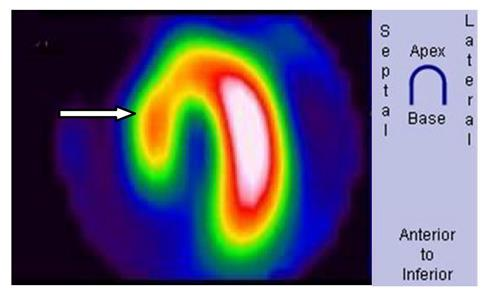
Na obrazie scyntygrafii perfuzyjnej serca strzałką wskazano ścianę
W scyntygrafii dynamiczne badanie najczęściej rozpoczyna się
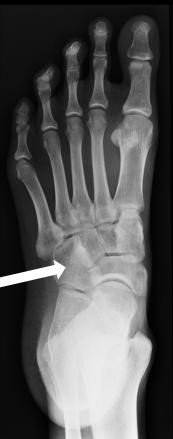
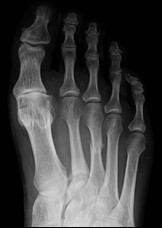
Którą kość zaznaczono strzałką na radiogramie stopy?
W technice napromieniania SSD mierzona jest odległość źródła promieniowania od
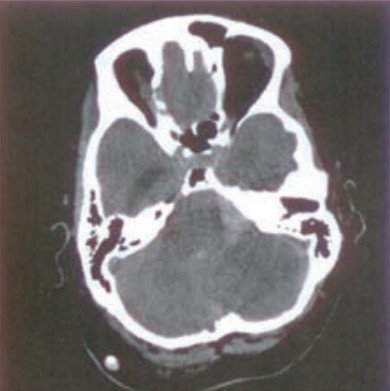
Zamieszczony obraz został wykonany metodą
Która składowa prawidłowej krzywej EKG odpowiada powolnej repolaryzacji komór mięśnia sercowego?
Do zdjęcia rentgenowskiego żeber w projekcji skośnej tylnej pacjenta należy ustawić
Na zamieszczonym przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano

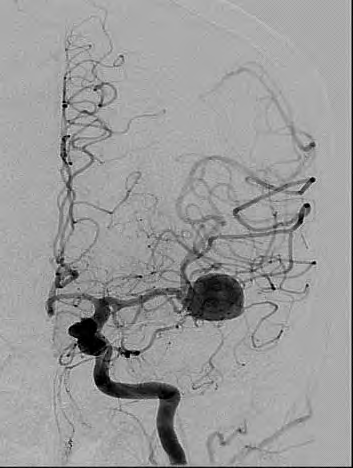
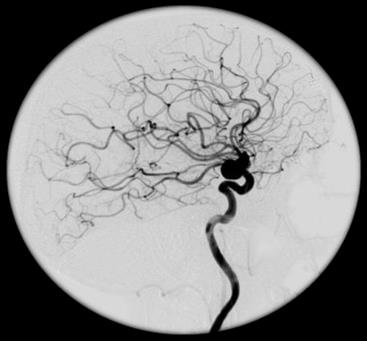
Którą patologię uwidoczniono w badaniu angiograficznym?
W radiologii stomatologicznej ząb o numerze 23 to kieł
Scyntygrafia kości „whole body” jest wskazana podczas diagnostyki
Który radioizotop jest emiterem promieniowania alfa?
Jakie struktury anatomiczne uwidoczniono na obrazie USG?
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
Które badanie zostało zarejestrowane na przedstawionym radiogramie?
W której próbie stroikowej przystawia się stroik do czoła (u podstawy nosa) lub na szczycie głowy i porównuje się przewodnictwo kostne ucha prawego i lewego?
Gadolin jako dożylny środek kontrastowy stosowany w MR powoduje
Na radiogramie stopy uwidocznione jest złamanie trzonu
W przedstawionym na ilustracji obrazie badania angiograficznego uwidoczniono
W badaniu PET stosuje się tylko radioizotopy emitujące
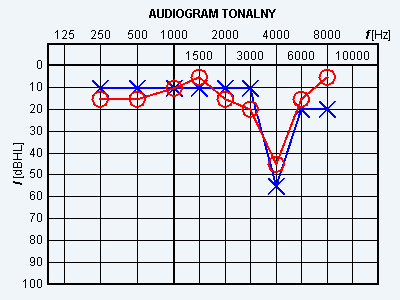
Wynik badania słuchu metodą audiometrii tonalnej wskazuje na
Który radioizotop jest stosowany w scyntygrafii perfuzyjnej mózgu?
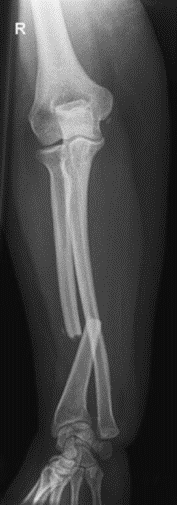
Na radiogramie uwidoczniono złamanie
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
Zestaw rentgenogramów przedstawia