Pytanie 1
Zadaniem technika elektroradiologii w pracowni badań naczyniowych jest
Wynik: 32/40 punktów (80,0%)
Wymagane minimum: 20 punktów (50%)
Zadaniem technika elektroradiologii w pracowni badań naczyniowych jest
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
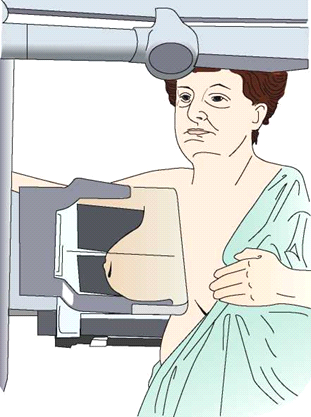
Ilustracja przedstawia pozycjonowanie pacjentki do badania mammograficznego w projekcji
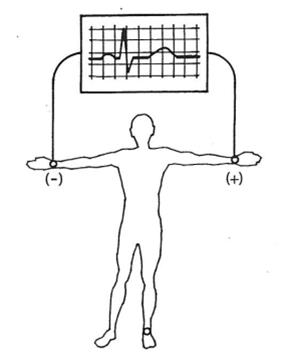
Która składowa prawidłowej krzywej EKG odpowiada powolnej repolaryzacji komór mięśnia sercowego?
Wiązka elektronów najczęściej stosowana jest do leczenia zmian nowotworowych w obrębie
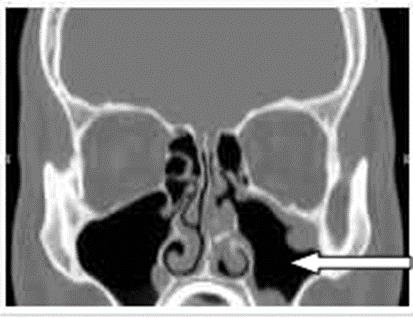
Na zamieszczonym obrazie TK strzałką zaznaczono zatokę
Rutynowe badanie koronarografii prawej tętnicy wieńcowej wykonywane jest w rzucie skośnym przednim
Ilustracja przedstawia pozycjonowanie pacjentki do badania mammograficznego w projekcji
W radiografii mianem SID określa się
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
Który radioizotop stosuje się do badania scyntygraficznego kości?
Zgodnie ze standardami do wykonania zdjęcia bocznego czaszki, należy zastosować kasetę o wymiarze
Przy ułożeniu do zdjęcia kręgów szyjnych CIII-CVII w projekcji przednio-tylnej lampa może być odchylona o kąt
Hiperfrakcjonowanie dawki w radioterapii oznacza napromienienie pacjenta
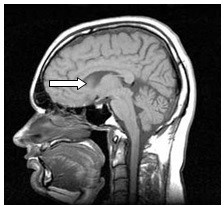
Zaznaczona strzałką struktura anatomiczna na obrazie rezonansu magnetycznego to
Po wykonanej radioterapii do dokumentacji pacjenta należy wpisać dawkę promieniowania w jednostce
Co określa M₀ w systemie klasyfikacji nowotworów TNM?
Która metoda leczenia onkologicznego zaliczana jest do leczenia systemowego?
Jakie wymagania techniczne muszą spełniać aparaty terapeutyczne stosowane w zakładach brachyterapii, służące bezpośrednio do napromieniania pacjenta metodą zdalnego wprowadzania źródeł promieniotwórczych?
Wyniosłość międzykłykciowa znajduje się na nasadzie
Celiakografia jest badaniem kontrastowym
W technice napromieniania SSD mierzona jest odległość źródła promieniowania
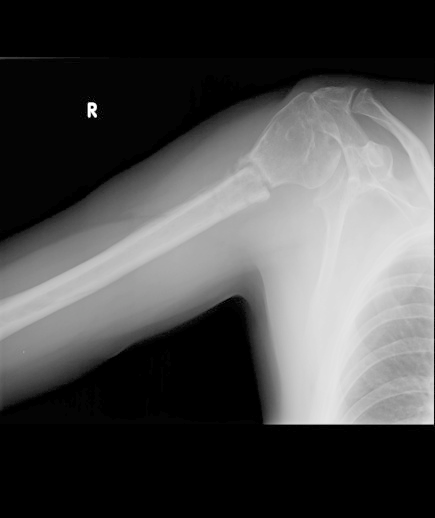
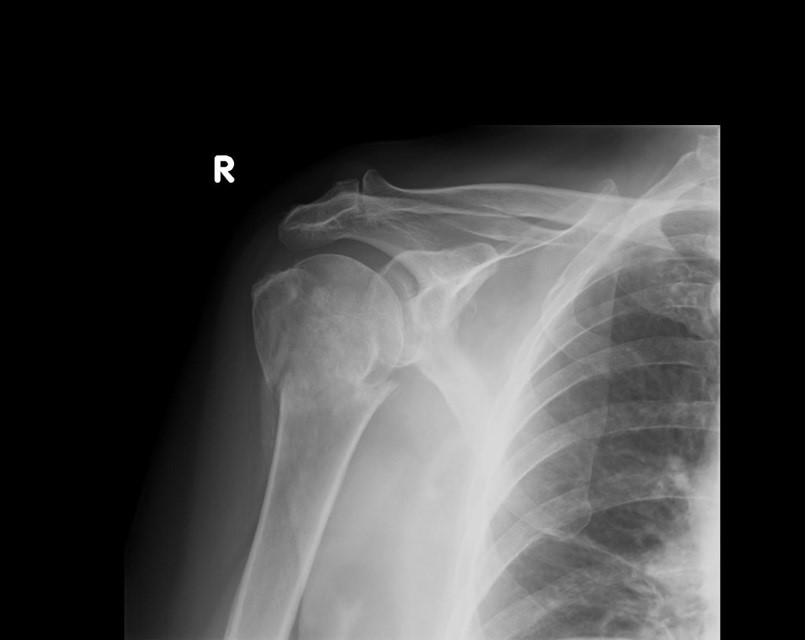
Na radiogramie uwidoczniono złamanie
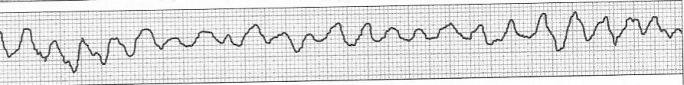
Zamieszczony elektrokardiogram przedstawia
W badaniu cystografii wstępującej środek kontrastowy należy podać
Standardowe badanie USG średniej wielkości piersi wykonuje się głowicą w zakresie częstotliwości
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
Zgodnie z obowiązującą procedurą radiologiczną zdjęcie jamy brzusznej przy podejrzeniu zapalenia nerek zostanie wykonane w projekcji
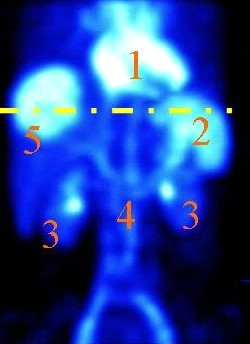
Który narząd na obrazie scyntygrafii znakowanej erytrocytami zaznaczono cyfrą 2?
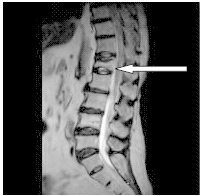
Na obrazie rezonansu magnetycznego strzałką oznaczono patologiczny kręg
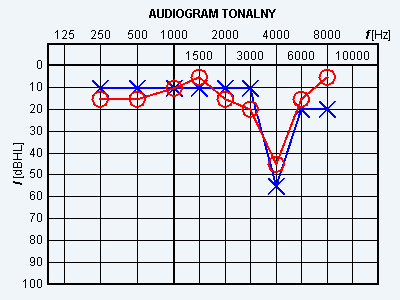
Wynik badania słuchu metodą audiometrii tonalnej wskazuje na
Badanie przewodu pokarmowego metodą podwójnego kontrastu wiąże się z podaniem pacjentowi
Wskazaniem do wykonania badania spirometrycznego jest
Który zestaw zdjęć narządów klatki piersiowej należy wykonać u pacjenta z podejrzeniem lewostronnego zapalenia płuc?
Fala głosowa rozchodzi się
Które odprowadzenie elektrokardiograficzne przedstawiono na ilustracji?
Jaki jest cel stosowania bolusa w radioterapii?
Dobierz dla standardowego pacjenta projekcję, pozycję i sposób ułożenia kasety o wymiarach 30 cm × 40 cm do zdjęcia przeglądowego układu moczowego.
| Projekcja | Pozycja | Ułożenie kasety | |||
|---|---|---|---|---|---|
| 1. | AP | 3. | stojąca | 5. | poprzeczne |
| 2. | PA | 4. | leżąca | 6. | podłużne |
Na radiogramie uwidoczniono złamanie
W którym okresie ciąży wykonanie u kobiety zdjęcia rentgenowskiego klatki piersiowej jest najbardziej szkodliwe dla płodu?