Pytanie 1
Wskaź urządzenie, które wykorzystuje się do pomiaru zasolenia wody?
Wynik: 34/40 punktów (85,0%)
Wymagane minimum: 20 punktów (50%)
Wskaź urządzenie, które wykorzystuje się do pomiaru zasolenia wody?
Zakończenie miareczkowania ustala się na podstawie pomiaru zmiany przewodnictwa roztworu poddanego miareczkowaniu w metodzie
Roztwór K2CrO4 jest używany jako wskaźnik przy oznaczaniu chlorków w metodzie Mohra. Powoduje on zmianę koloru mieszaniny reakcyjnej, co jest skutkiem
Gdy podczas analizy ilościowej wyniki są zbliżone do wartości rzeczywistej, mówi się wtedy o
| Zawartość chlorowodoru w próbce można obliczyć wg wzoru: mB = CA · VA⁄1000 · pB⁄pA · MB w którym: mB – masa analizowanej substancji [g] CA – stężenie titranta [mol/dm3] VA – objętość titranta [cm3] pA i pB – współczynniki stechiometryczne reakcji, odpowiednio titranta i substancji oznaczanej MB – masa molowa substancji oznaczanej; 36,46 g/mol Do oznaczenia zużyto średnio 20,0 cm3 titranta, którego stężenie wynosiło 0,1000 mol/dm3. Obliczono masę próbki, która wyniosła 0,07292 g. |
| A. | HCl + NaOH → NaCl + H2O |
| B. | 3HCl + Al(OH)3 → AlCl3 + 3H2O |
| C. | 2HCl + Na2CO3 → 2NaCl + H2O + CO2 |
| D. | 2HCl + Na2B4O7 + 5H2O → 4H3BO3 + 2NaCl |
Zjawisko dzielenia się składników mieszaniny pomiędzy fazę stacjonarną a ruchomą w układzie to proces widoczny w
Określ zawartość amoniaku w analizowanej próbce, jeżeli na jej zmiareczkowanie zużyto 20,0 cm3 roztworu HCl o stężeniu 0,1 mol/dm3.
Zawartość olejku w liściach eukaliptusa zmierzono za pomocą destylacji w aparacie Derynga. Z 20 g surowca uzyskano 0,5 cm3 olejku o gęstości 0,920 g/cm3. Jak oblicza się procentową zawartość olejku w liściach eukaliptusa?
Odczynnikiem grupowym kationów IV grupy analitycznej jest
| A. | H2S w roztworze NH3(aq) i NH4Cl. |
| B. | roztwór HCl o stężeniu 2 mol/dm3. |
| C. | (NH4)2CO3 w roztworze NH3(aq) i NH4Cl. |
| D. | H2S w roztworze HCl o stężeniu 0,3 mol/dm3. |
Które elektrody wykorzystuje się w typowym zestawie do analizy elektrograwimetrycznej przedstawionej na zamieszczonym schemacie?
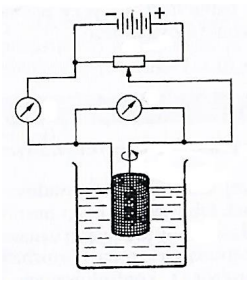
Na rysunku przedstawiono schemat aparatury do oznaczania w wodzie
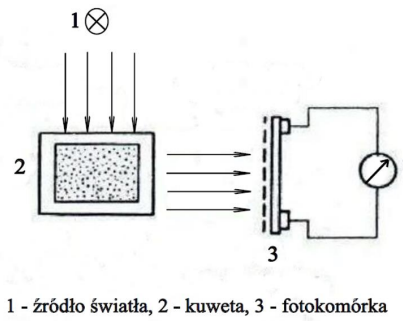
Na rysunku przedstawiono schemat procesu
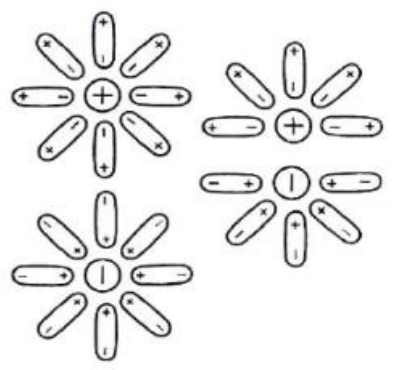
Błąd kwasowy oraz błąd sodowy wprowadzają ograniczenia w użyciu elektrody
Na zmiareczkowanie 10 cm3 NaOH zużyto 2 cm3 0,1-molowego roztworu H2SO4. Ilość wodorotlenku sodu w badanej próbce w g/100 cm3 wynosi (Na — 23 g/mol, O — 16 g/mol, H — 1 g/mol)
W literaturze chromatografię określa się skrótem GC
Konduktometria to technika analityczna, która opiera się na pomiarze
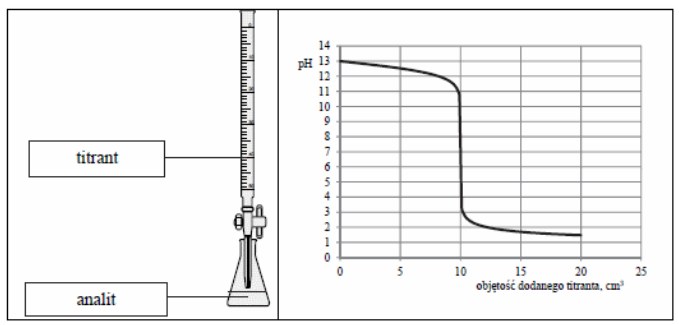
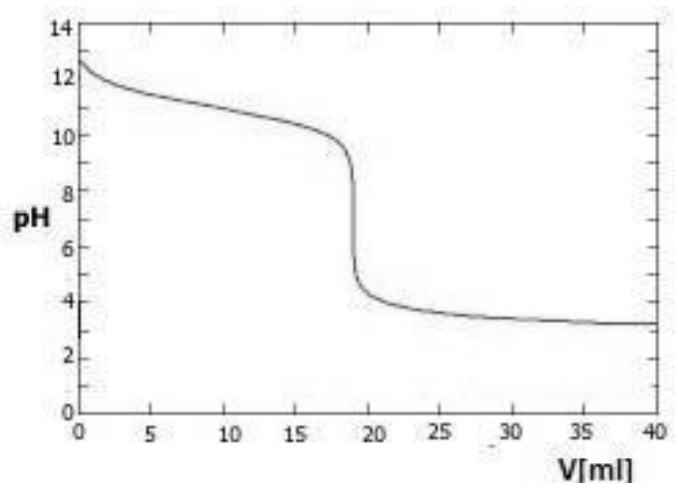
Na wykresie przedstawiono krzywą miareczkowania
Jakiego odczynnika użyć do wykrywania jonów chlorkowych w roztworze soli fizjologicznej?
W celu preparatywnego rozdzielania aminokwasów wykorzystuje się metodę elektroforezy, która bazuje na
Piknometr umożliwia określenie
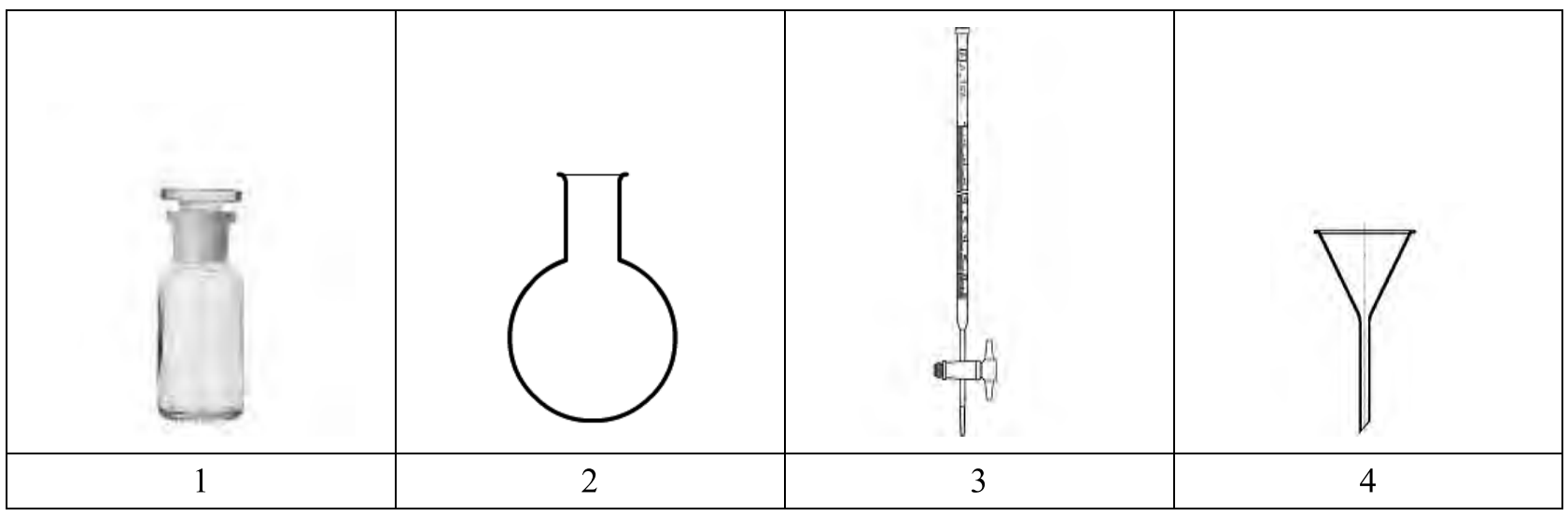
Korzystając z rysunków zamieszczonych w tabeli, wybierz zestaw sprzętu potrzebnego do oznaczania CO2 w wodach powierzchniowych metodą miareczkową.
Elektroforeza to technika wykorzystywana głównie do segregacji mieszaniny
Na podstawie informacji zamieszczonych w tabeli wskaż wzór związku, który wytrąci się w postaci osadu.
| Badany kation | Odczynnik grupowy | NaOH | Barwienie płomienia |
|---|---|---|---|
| Mg2+ | brak | biały osad | |
| K+ | brak | fiołkowy | |
| Na+ | brak | żółty |
Podczas miareczkowania kwasu octowego używając roztworu wodorotlenku sodu dochodzi do reakcji
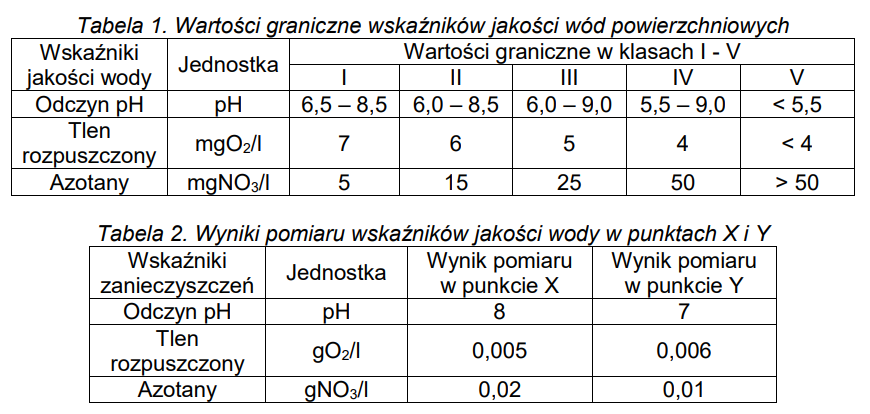
Na podstawie danych w tabelach 1-2 zawierających wartości graniczne wskaźników jakości wody i uzyskane wyniki pomiarowe oceń jakość wody w punktach pomiarowych X i Y, określając jej klasę.
Wskaźników używanych w oznaczeniach kompleksometrycznych nie obejmuje
Jakie badanie chemiczne dotyczące wody przeprowadza się przy użyciu miareczkowania kompleksometrycznego?
Klasyfikacja kwasowości soku owocowego jest związana z metodami
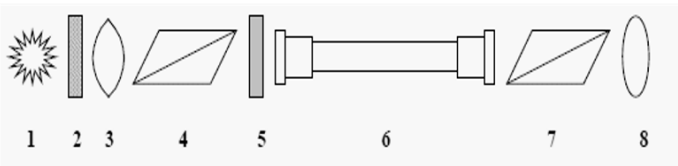
Na rysunku przedstawiającym schemat polarymetru, cyfrą 4 oznaczono
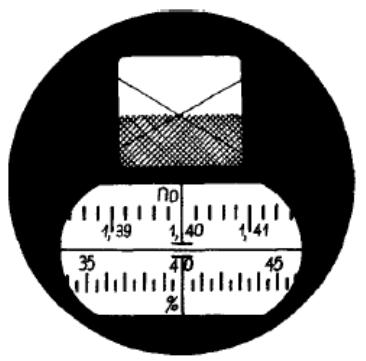
Na rysunku przedstawione jest pole widzenia
Zjawisko zatrzymywania obcych jonów wewnątrz strącanej substancji podczas analizy wagowej określa się mianem
Absorbancja barwnego roztworu o stężeniu 0,0004 mol/dm3, zmierzona w kuwecie o grubości 1 cm wynosi 0,30. Korzystając z zamieszczonego wzoru, oblicz wartość molowego współczynnika absorpcji £.
| A = ε · l · c |
| gdzie: |
| A – wartość absorbancji |
| ε – molowy współczynnik absorpcji; dm3/mol · cm |
| c – stężenie molowe roztworu; mol/dm3 |
| l – grubość kuwety; cm |
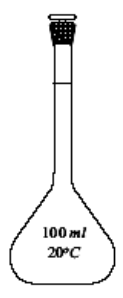
Wskaż, w jakim rodzaju analizy stosowany jest sprzęt przedstawiony na rysunku.
Analiza, która opiera się na kontrolowanym wprowadzaniu roztworu o znanym stężeniu do badanego roztworu, to metoda oznaczeń ilościowych zwana
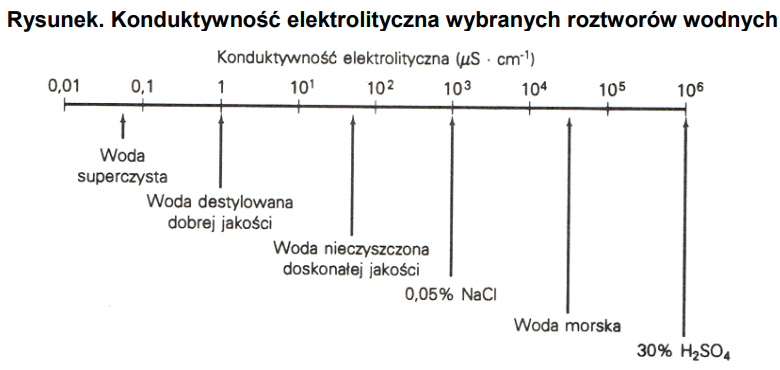
Konduktywność elektrolityczna wody destylowanej stosowanej w laboratorium chemicznym wynosi 0,001 mS cm-1. Z analizy danych przedstawionych na rysunku wynika, że woda ta jest
Jakie kationy wchodzą w skład II grupy analitycznej?
Zgodnie z informacją zawartą w ramce zawartość jonów chlorkowych i jodkowych w roztworze można oznaczyć
Zasada oznaczenia zawartości jonów chlorkowych i jodkowych w roztworze. Podstawą metody jest reakcja strąceniowa zachodząca między jonami Cl- i I- a jonami Ag+. Oznaczenie polega na badaniu zmian potencjału elektrody wskaźnikowej podczas dodawania do analizowanego roztworu, mianowanego roztworu AgNO3. |
KOH w formie roztworu jest wykorzystywany jako titrant w analizie żywności do określenia
Komplekson III (sól disodowa kwasu etylenodiaminotetraoctowego) używana w analizie objętościowej tworzy z metalami kompleksy w stosunku ligandu do metalu
Na podstawie rysunku analitem może być roztwór