Pytanie 1
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Wynik: 1/40 punktów (2,5%)
Wymagane minimum: 20 punktów (50%)
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Czułość bezwzględna wagi definiuje się jako
Aby przyspieszyć reakcję, należy zwiększyć stężenie substratów
Brak odpowiedzi na to pytanie.
Jaką objętość w warunkach standardowych zajmie 1,7 g amoniaku (masa molowa amoniaku wynosi 17 g/mol)?
Brak odpowiedzi na to pytanie.
Na rysunku przedstawiono przyrząd do pobierania próbek

Brak odpowiedzi na to pytanie.
Przedstawiono wyciąg z karty charakterystyki substancji chemicznej. Na podstawie informacji zawartej w zamieszczonym fragmencie karty wskaż wzór chemiczny substancji, której można użyć jako materiału neutralizującego lodowaty kwas octowy.
Kwas octowy lodowaty 99,5% Materiały zapobiegające rozprzestrzenianiu się skażenia i służące do usuwania skażenia Jeżeli to możliwe i bezpieczne, zlikwidować lub ograniczyć wyciek (uszczelnić, zamknąć dopływ cieczy, uszkodzone opakowanie umieścić w opakowaniu awaryjnym). Ograniczyć rozprzestrzenianie się rozlewiska przez obwałowanie terenu; zebrane duże ilości cieczy odpompować. Małe ilości rozlanej cieczy przysypać niepalnym materiałem chłonnym (ziemia, piasek oraz materiałami neutralizującymi kwasy, np. węglanem wapnia lub sodu, zmielonym wapieniem, dolomitem), zebrać do zamykanego pojemnika i przekazać do zniszczenia. Zanieczyszczoną powierzchnię spłukać wodą. Popłuczyny zebrać i usunąć jako odpad niebezpieczny. |
Brak odpowiedzi na to pytanie.
Który symbol literowy umieszczany na naczyniach miarowych wskazuje na kalibrację do "wlewu"?
Brak odpowiedzi na to pytanie.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Osady kłaczkowe, które powstają w wyniku prostego koagulowania, określa się mianem osadów
Brak odpowiedzi na to pytanie.
Woda używana w laboratorium chemicznym, uzyskana poprzez filtrację przez wymieniacz jonowy, jest określana mianem wody
Brak odpowiedzi na to pytanie.
Na podstawie informacji zawartych w tabeli określ, który parametr spośród podanych należy oznaczyć w pierwszej kolejności.
| Tabela. Sposoby utrwalania próbek wody i ścieków, miejsce analizy, dopuszczalny czas przechowywania próbek | ||||
|---|---|---|---|---|
| Oznaczany parametr | Rodzaj naczynia do przechowywania próbki | Sposób utrwalania próbki | Miejsce wykonania analizy | Dopuszczalny czas przechowywania próbki |
| Chlorki | szklane lub polietylenowe | - | laboratorium | 96 godzin |
| Chlor pozostały | szklane | - | w miejscu pobrania próbki | - |
| ChZT | szklane | zakwaszenie do pH<2, schłodzenie do temperatury 2-5°C | laboratorium | 24 godziny |
| Kwasowość | szklane lub polietylenowe | schłodzenie do temperatury 2-5°C | laboratorium | 4 godziny |
| Mangan | szklane lub polietylenowe | zakwaszenie do pH<2, schłodzenie do temperatury 2-5°C | laboratorium | 48 godziny |
Brak odpowiedzi na to pytanie.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Po połączeniu 50 cm3 wody z 50 cm3 alkoholu etylowego, objętość otrzymanej mieszanki jest poniżej 100 cm3. Zjawisko to jest spowodowane
Brak odpowiedzi na to pytanie.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Reagenty o najwyższej czystości to reagenty
Brak odpowiedzi na to pytanie.
Na etykiecie próbki środowiskowej należy umieścić datę jej pobrania, lokalizację poboru oraz
Brak odpowiedzi na to pytanie.
W celu przeprowadzenia opisanego doświadczenia, należy przygotować:
| Opis procesu wydzielenia kwasu acetylosalicylowego z tabletek |
|---|
| Pięć rozgniecionych tabletek aspiryny (polopiryny) umieszcza się w kolbie stożkowej o pojemności 100 ml, dodaje 10 ml etanolu i ogrzewa na łaźni wodnej, aż do momentu rozpadnięcia się tabletek. W roztworze znajduje się kwas acetylosalicylowy, natomiast masa tabletkowa pozostaje w osadzie. Osad ten odsącza się na ogrzanym lejku szklanym zaopatrzonym w sączek karbowany. Do odebiornego przesączu dodaje się 20-30 ml zimnej wody destylowanej. Dodatek wody powoduje wypadanie osadu aspiryny z roztworu (zmniejsza się rozpuszczalność aspiryny w roztworze wodno-alkoholowym). Wydzielone kryształy odsączyć na lejku sitowym i suszyć na powietrzu. |
Brak odpowiedzi na to pytanie.
Po zmieszaniu wszystkie pierwotne próbki danej partii materiału tworzą próbkę
Brak odpowiedzi na to pytanie.
Podczas pomiaru masy substancji w naczyniu wagowym na wadze technicznej, dla zrównoważenia ciężaru na szalce umieszczono odważniki: 20 g, 2 g, 500 mg, 200 mg, 20 mg, 10 mg, 10 mg oraz 5 g. Całkowita masa substancji z naczynkiem wyniosła
Brak odpowiedzi na to pytanie.
Na diagramie przedstawiającym proces pobierania prób środowiskowych do analizy literą Y oznaczono próbkę
Brak odpowiedzi na to pytanie.
Podstawowy zestaw do filtracji, oprócz statywu i sączka, obejmuje
Brak odpowiedzi na to pytanie.
Podaj kolejność odczynników chemicznych według rosnącego stopnia czystości?
Brak odpowiedzi na to pytanie.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Jakie proporcje objętościowe powinny być zastosowane do zmieszania roztworu etanolu o stężeniu 30% (V/V) z roztworem o stężeniu 70% (V/V), aby uzyskać roztwór o stężeniu 50% (V/V)?
Brak odpowiedzi na to pytanie.
Jakie są zalecenia dotyczące postępowania z odpadowymi roztworami kwasów oraz zasad?
Brak odpowiedzi na to pytanie.
W trakcie reakcji estryfikacji opisanej równaniem CH3COOH + C2H5OH ↔ CH3COOC2H5 + H2O użyto molowego stosunku alkoholu do kwasu wynoszącego 1:10. W rezultacie tego
Brak odpowiedzi na to pytanie.
Proces nitrowania najczęściej realizuje się, stosując organiczny substrat
Brak odpowiedzi na to pytanie.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Substancje pomocnicze wykorzystywane do realizacji podstawowych analiz jakościowych i ilościowych, które nie wymagają wysokiej czystości, są oznaczane na opakowaniach symbolem
Brak odpowiedzi na to pytanie.
Przedstawiony zestaw stosowany jest w laboratorium do przeprowadzenia procesu
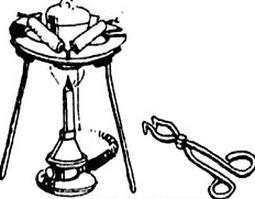
Brak odpowiedzi na to pytanie.
Proces usuwania substancji z cieczy lub wydobywania składnika z mieszanin cieczy, oparty na równowadze fazowej ciecz-gaz, nazywa się
Brak odpowiedzi na to pytanie.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Proces, w którym woda jest usuwana z zamrożonego materiału poprzez sublimację lodu
(czyli bezpośrednie przejście do stanu pary z pominięciem stanu ciekłego) nazywa się
Brak odpowiedzi na to pytanie.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
W chemicznym laboratorium apteczka pierwszej pomocy powinna zawierać
Brak odpowiedzi na to pytanie.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Aby oddzielić mieszankę etanolu i wody, konieczne jest przeprowadzenie procesu
Brak odpowiedzi na to pytanie.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Który z poniższych sposobów homogenizacji próbki jest najbardziej odpowiedni do przygotowania próbki gleby do analizy chemicznej?
Brak odpowiedzi na to pytanie.