Pytanie 1
W przypadku kontaktu ze stężonym roztworem zasady, co należy zrobić jak najszybciej?
Wynik: 25/40 punktów (62,5%)
Wymagane minimum: 20 punktów (50%)
W przypadku kontaktu ze stężonym roztworem zasady, co należy zrobić jak najszybciej?
Sączków o najmniejszych średnicach, nazywanych "twardymi" i oznaczonych kolorem niebieskim, używa się do filtracji osadów?
Część partii pobrana w sposób jednorazowy z jednego źródła towaru zapakowanego lub z jednego opakowania jednostkowego określana jest mianem próbki
Sód metaliczny powinien być przechowywany w laboratorium
W urządzeniu Soxhleta wykonuje się
Jaką objętość w warunkach standardowych zajmie 1,7 g amoniaku (masa molowa amoniaku wynosi 17 g/mol)?
Jakie czynniki wpływają na zmiany jakościowe w składzie próbki?
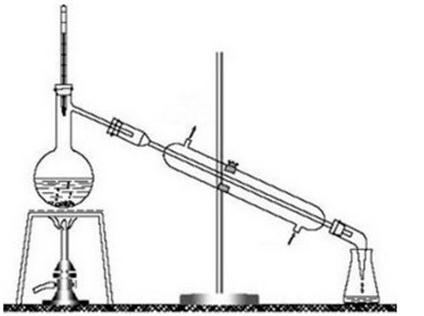
Na rysunku przedstawiono zestaw do
Podczas pipetowania menisk górny określa się dla roztworów
Jakim kolorem oznacza się instalację gazową w laboratorium analitycznym?
Opis w ramce przedstawia sposób oczyszczania substancji poprzez
| Próbke substancji stałej należy umieścić w kolbie kulistej, zaopatrzonej w chłodnicę zwrotną, dodać rozpuszczalnika - etanolu i delikatnie ogrzewać do wrzenia. Po lekkim ostudzeniu dodać do roztworu niewielką ilość węgla aktywnego, zagotować i przesączyć na gorąco. Przesącz pozostawić do ostygnięcia, a wydzielony osad odsączyć pod zmniejszonym ciśnieniem, przemyć niewielką ilością rozpuszczalnika, przenieść na szalkę, pozostawić do wyschnięcia, a następnie zważyć. |
Po przeprowadzeniu krystalizacji z 120 g kwasu szczawiowego uzyskano 105 g produktu o wysokiej czystości. Jaki był poziom zanieczyszczeń w kwasie szczawiowym?
Nie należy używać do czyszczenia szklanych naczyń laboratoryjnych
Rozpuszczalność siarczanu(VI) potasu przy temperaturze 30oC wynosi 13 g na 100 g wody. Jaką masę tego związku należy dodać do wody, aby uzyskać 500 g roztworu nasyconego?
Na etykiecie odważki analitycznej znajduje się napis: Z odważki tej można przygotować
Odważka analityczna azotan(V) srebra(I) AgNO3 0,1 mol/dm3 |
W celu uzyskania 500 g mieszaniny oziębiającej o temperaturze -18oC należy zmieszać
| Tabela. Mieszaniny oziębiające | ||
|---|---|---|
| Temperatura mieszaniny [°C] | Skład mieszaniny | Stosunek masowy |
| -2 | Woda + chlorek amonu | 10 : 3 |
| -15 | Woda + rodanek amonu | 10 : 13 |
| -18 | Lód + chlorek amonu | 10 : 3 |
| -21 | Lód + chlorek sodu | 3 : 1 |
| -22 | Lód + chlorek amonu + azotan(V) amonu | 25 : 5 : 11 |
| -25 | Lód + azotan(V) amonu | 1 : 1 |
Aby przygotować 250 cm3 roztworu wodorotlenku potasu o stężeniu 0,25 mola, potrzebne będzie
Zapis "20°C" umieszczony na pipecie oznacza, że

Do grupy reagentów o szczególnym zastosowaniu nie wlicza się
Określ, jakie informacje powinny być zarejestrowane w ewidencji wydania substancji niebezpiecznych, stosowanych w badaniach laboratoryjnych?
Próbkę uzyskaną z próbki ogólnej poprzez jej zmniejszenie nazywa się
Po zmieszaniu wszystkie pierwotne próbki danej partii materiału tworzą próbkę
Podstawowy zestaw do filtracji, oprócz statywu i sączka, obejmuje
Dla cieczy bezbarwnej odczyt w biurecie pokazanej na rysunku wynosi

Substancje, które wykorzystuje się do ustalania miana roztworu, to
Technika oddzielania płynnych mieszanin, w której wykorzystuje się różnice w prędkości migracji składników przez odpowiednią bibułę, nazywa się
Jakie proporcje objętościowe powinny być zastosowane do zmieszania roztworu etanolu o stężeniu 30% (V/V) z roztworem o stężeniu 70% (V/V), aby uzyskać roztwór o stężeniu 50% (V/V)?
Pierwotna próbka jest zbierana
Który z etapów przygotowania próbek do analizy opisano w ramce?
| Proces polegający na usuwaniu wody z zamrożonego materiału na drodze sublimacji lodu, tzn. bezpośredniego jego przejścia w stan pary z pominięciem stanu ciekłego. |
Z próbki zawierającej siarczany(VI) należy najpierw wydzielić metodą filtracji zanieczyszczenia, które są nierozpuszczalne w wodzie. Dokładność wypłukania tych zanieczyszczeń weryfikuje się za pomocą roztworu
Proces nitrowania najczęściej realizuje się, stosując organiczny substrat
Podczas oznaczania kwasu siarkowego zachodzi reakcja:
H2SO4 + 2NaOH → Na2SO4 + 2H2OZgodnie z zamieszczoną instrukcją, roztwór poreakcyjny należy
| Fragmenty instrukcji zbierania, utylizacji i eliminacji odpadów chemicznych | |
|---|---|
| Lista substancji, które mogą być usunięte z odpadami komunalnymi w postaci stałej, lub wprowadzone do systemu kanalizacyjnego w postaci rozcieńczonych roztworów wodnych, o ile ich ilość nie przekracza jednorazowo 100 g. | |
| Związki nieorganiczne Siarczany sodu, potasu, magnezu, wapnia, amonu | |
| Kwasy nieorganiczne Stężone kwasy ostrożnie rozcieńczyć przez wkroplenie z równoczesnym mieszaniem do wody z lodem, a następnie zneutralizować roztworem wodorotlenku sodowego. Po neutralizacji doprowadzić pH roztworu do zakresu 6-8 przelać do pojemnika S. Małe ilości kwasów takich jak siarkowy, solny, azotowy czy fosforowy (nie więcej niż 10 g) po rozcieńczeniu wodą i neutralizacji roztworem wodorotlenku sodowego oraz doprowadzeniu pH takiego roztworu do zakresu 6-8 można wylać do zlewu i obficie spłukać wodą. | |
| Sole nieorganiczne Stałe sole nieorganiczne – pojemnik N. Obojętne roztwory soli nieorganicznych pojemnik S. Sole metali ciężkich, sole o właściwościach toksycznych – pojemnik TN. |
Ogrzewanie organicznych substancji w atmosferze powietrza w otwartym naczyniu, mające na celu przemianę tych substancji w związki nieorganiczne, określa się jako mineralizacja?
W tabeli przestawiono dane dotyczące wybranych roztworów wodnych wodorotlenku sodu.
Oblicz masę wodorotlenku sodu, jaką należy rozpuścić w 200,0 cm3 wody, aby otrzymać roztwór o gęstości 1,0428 g/cm3.
| d420 [g/cm3] | masa NaOH [g/100 cm3] |
|---|---|
| 1,0095 | 1,01 |
| 1,0207 | 2,04 |
| 1,0428 | 4,17 |
| 1,0648 | 6,39 |
| 1,0869 | 8,70 |
| 1,1089 | 11,09 |
Z etykiety wynika, że dany związek mógł być

Próbkę wody przeznaczoną do oznaczenia zawartości metali poddaje się utrwalaniu za pomocą
| Sposoby utrwalania i przechowywania próbek wody przeznaczonych do badań fizykochemicznych. | |
|---|---|
| Oznaczenie | Sposób utrwalania i przechowywania |
| Barwa | Przechowywać w ciemności |
| Mętność | Przechowywać w ciemności |
| Twardość | pH = 3 z użyciem HNO₃ |
| OWO | 0,7 ml HCl/30 ml próbki |
| ChZT | pH 1-2 z użyciem H₂SO₄ |
| Fosfor | Przechowywać w temperaturze 1-5°C |
| Glin | pH 1-2 z użyciem HNO₃ |
| Żelazo | pH 1-2 z użyciem HNO₃ |
| Utlenialność | pH1-2 z użyciem H₂SO₄. Przechowywać w ciemności |
Ilustracja przedstawia fragment szklanej pipety wielomiarowej

Na ilustracji przedstawiono sprzęt stosowany do sączenia osadu
W celu wydania świadectwa kontroli jakości odczynnika chemicznego - jodku potasu cz.d.a. przeprowadzono jego analizę. Wymagania oraz wyniki badań zapisano w tabeli:
Z analizy danych zawartych w tabeli wynika, że jodek potasu cz.d.a.
| Wymagania | Wynik badania | |
|---|---|---|
| Zawartość KI | min. 99,5% | 99,65% |
| Wilgoć | max. 0,1% | 0,075% |
| Substancje nierozpuszczalne w wodzie | max. 0,005% | 0,002% |
| pH (5%, H2O) | 6 ÷ 8 | 6,8 |
| Azot ogólny (N) | max. 0,001% | 0,0007% |
| Chlorki i bromki (j. Cl) | max. 0,01% | 0,004% |
| Fosforany (PO4) | max. 0,001% | 0,0006% |
| Jodany (IO3) | max. 0,0003% | 0,0001% |
| Siarczany (SO4) | max. 0,001% | 0,0004% |
| Metale ciężkie (j. Pb) | max. 0,0005% | 0,00025% |
| Arsen (As) | max. 0,00001% | 0,000006% |
| Magnez (Mg) | max. 0,001% | 0,0004% |
| Sód (Na) | max. 0,05% | 0,015% |
| Wapń (Ca) | max. 0,001% | 0,0006% |
| Żelazo (Fe) | max. 0,0003% | 0,0003% |
Jakie jest stężenie molowe roztworu, jeśli w 100 cm3 roztworu znajduje się 5,6 g KOH?
MK = 39 g/mol, MO = 16 g/mol, MH = 1 g/mol