Pytanie 1
Obrazy DDR są tworzone w trakcie
Wynik: 34/40 punktów (85,0%)
Wymagane minimum: 20 punktów (50%)
Obrazy DDR są tworzone w trakcie
Zdjęcie zatok przynosowych wykonuje się w pozycji
Na radiogramie czaszki strzałką zaznaczono
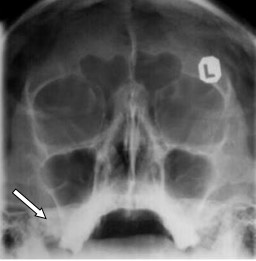
Zamieszczony obraz został wykonany metodą
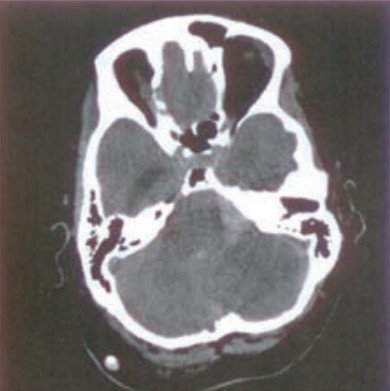
Który detektor w radiografii wymaga laserowego czytnika obrazu?
Jak zgodnie ze standardem należy ustawić pacjenta do badania rentgenowskiego w skosie tylnym prawym?
Jaki czas należy ustawić do wykonania zdjęcia rentgenowskiego dwójki górnej lewej?
| Tabela ekspozycji | |||
|---|---|---|---|
| wartości | czasu (s) | napięcia (kV) | natężenia (mA) |
| zęby przedtrzonowe i kły | 0,160 | 60 | 8 |
| siekacze | 0,120 | 60 | 8 |
| zęby trzonowe | 0,200 | 60 | 8 |
| ekspozycja zgryzowo-skrzydełkowa | 0,180 | 66 | 6 |
Rutynowe badanie koronarografii prawej tętnicy wieńcowej wykonywane jest w rzucie skośnym przednim
Który środek kontrastujący stosuje się w badaniu metodą rezonansu magnetycznego?
Która struktura może być oknem akustycznym w badaniu ultrasonograficznym?
Radiogram przedstawia
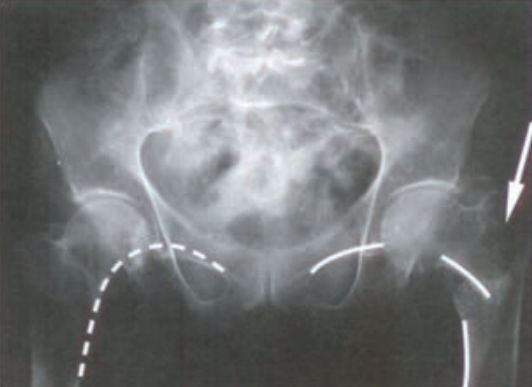
Promieniowanie rentgenowskie powstaje w wyniku hamowania
Skrótem HRCT (High Resolution Computed Tomography) określa się tomografię komputerową
W badaniu cystografii wstępującej środek kontrastowy należy podać
Na radiogramie uwidoczniono złamanie
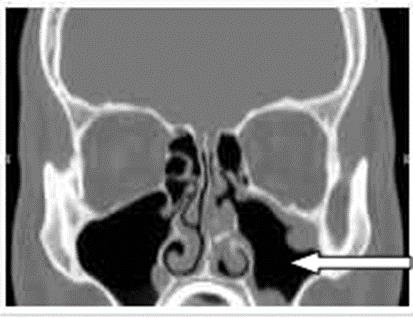
Na zamieszczonym obrazie TK strzałką zaznaczono zatokę
Technik elektroadiolog do badania MR kręgosłupa lędźwiowego powinien ułożyć pacjenta
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
Badanie polegające na wprowadzeniu cewnika przez pęcherz moczowy do moczowodu i miedniczki nerkowej i podaniu środka kontrastującego to
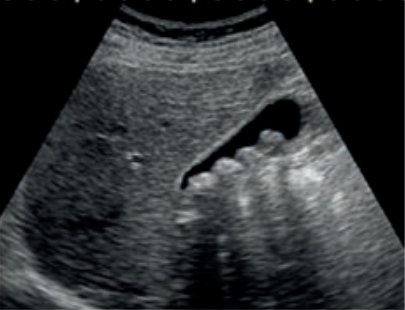
Jakie struktury anatomiczne uwidoczniono na obrazie USG?
Po zakończeniu badania angiograficznego należy zapisać w dokumentacji medycznej pacjenta:
Standardowo do wykonania których zdjęć należy zastosować kratkę przeciwrozproszeniową?
Parametrem krwi, który powinien zostać oznaczony u pacjenta przed wykonaniem badania MR z kontrastem, jest
Jaki kolor ma warstwa korowa kości w badaniu MR na obrazie T1- zależnym?
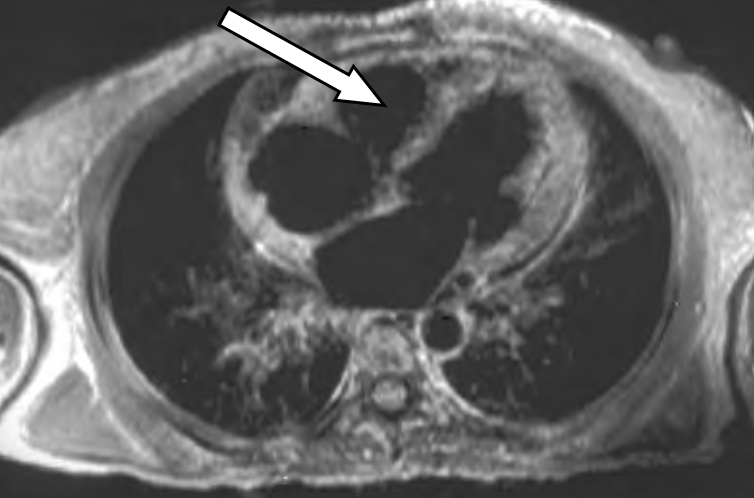
Na skanie rezonansu magnetycznego serca oznaczono
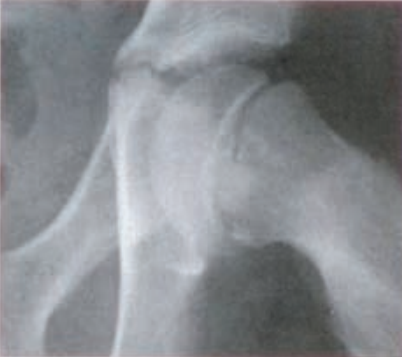
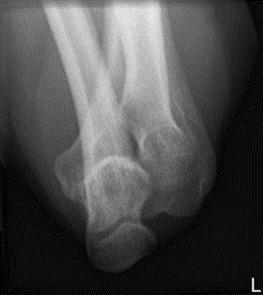
Na rentgenogramie przedstawione jest złamanie Saltera-Harrisa typu
Która metoda diagnostyczna służy do określenia gęstości minerału kostnego w ujęciu objętościowym g/cm³?
Która sekwencja obrazowania MR wykorzystuje impulsy RF o częstotliwości rezonansowej tłuszczu do tłumienia sygnału pochodzącego z tkanki tłuszczowej?
Który parametr ekspozycji ma decydujący wpływ na kontrast obrazu rentgenowskiego?
Którą strukturę anatomiczną i w jakiej projekcji uwidoczniono na radiogramie?
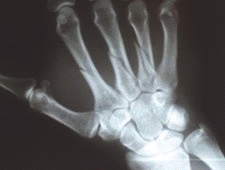
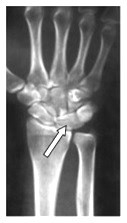
Na obrazie radiologicznym nadgarstka strzałką zaznaczona jest kość
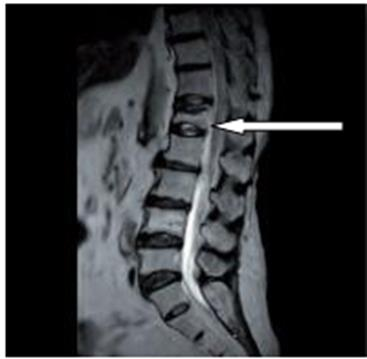
Na obrazie rezonansu magnetycznego strzałką wskazano patologiczny kręg
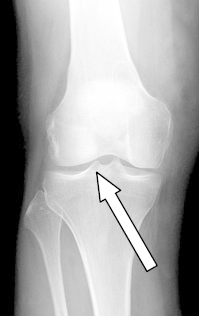
Którą strukturę anatomiczną oznaczono strzałką na radiogramie stawu kolanowego?
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
Na obrazie rezonansu magnetycznego głowy strzałką wskazano zatokę
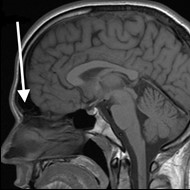
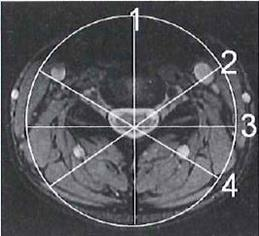
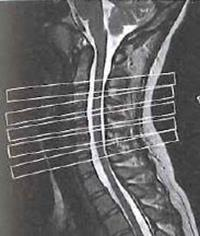
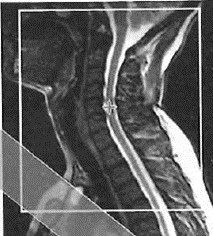
Na którym obrazie MR jest widoczne pasmo saturacji?

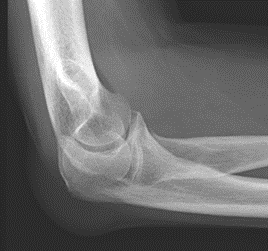
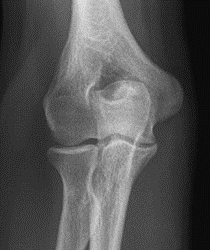
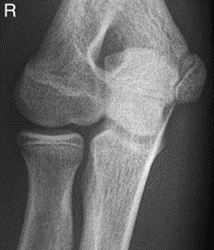
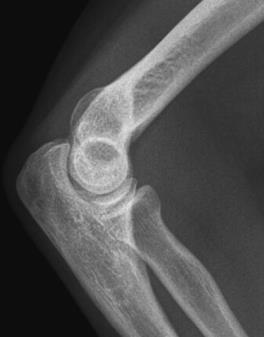
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
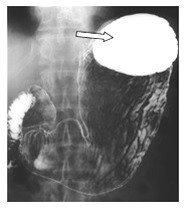
Który element żołądka zaznaczono strzałką na zdjęciu rentgenowskim?
Które zdjęcie RTG stawu łokciowego zostało wykonane w projekcji skośnej w rotacji zewnętrznej?