Pytanie 1
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
Wynik: 28/40 punktów (70,0%)
Wymagane minimum: 20 punktów (50%)
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
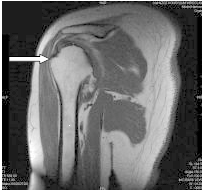
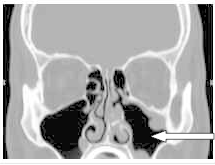
Który narząd został oznaczony strzałką na obrazie rezonansu magnetycznego?
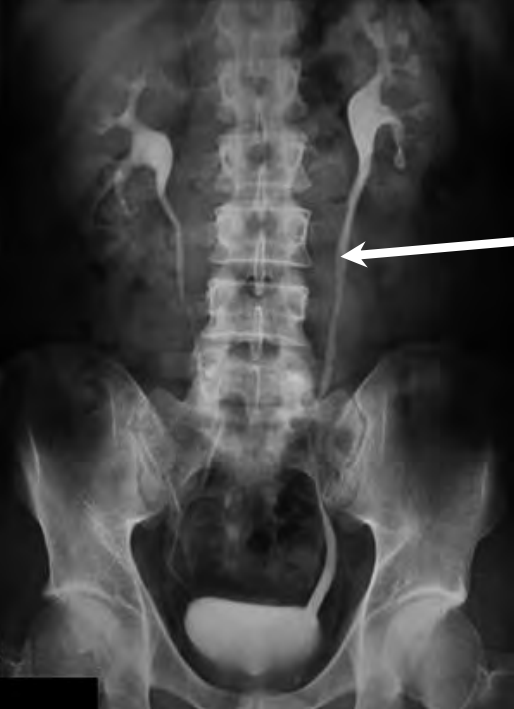
Na prawidłowo przedstawionym radiogramie badania kontrastowego strzałką zaznaczono
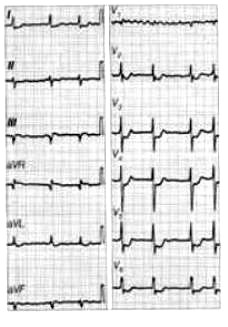
Odprowadzenie EKG mierzące różnicę potencjałów między lewym podudziem a prawym przedramieniem oznacza się jako
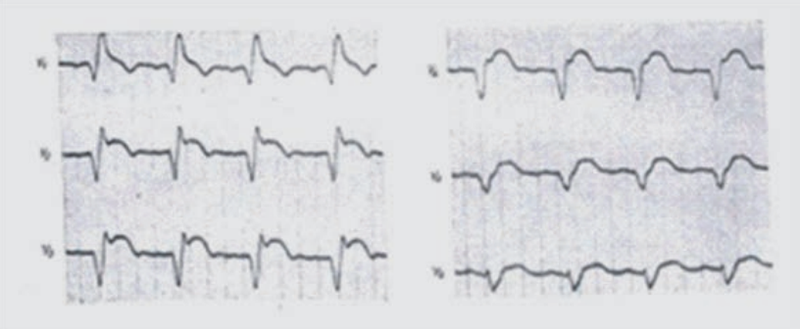
Na elektrokardiogramie uwidoczniono
Przemiana promieniotwórcza radu w ren opisana wzorem \( {}_{88}^{226}\text{Ra} \to {}_{86}^{222}\text{Rn} + {}_{2}^{4}\text{He} \) jest rozpadem
Którą strukturę anatomiczną oznaczono na obrazie rezonansu magnetycznego?
Wskaż osłonę radiologiczną, która jest stosowana w pracowniach radiodiagnostyki stomatologicznej.




Zdjęcie rentgenowskie nadgarstka w przywiedzeniu dołokciowym jest wykonywane w celu uwidocznienia kości
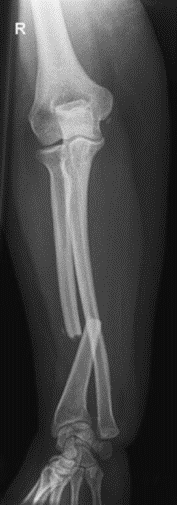
Na radiogramie uwidoczniono złamanie
Dawka graniczna wyrażona jako dawka skuteczna (efektywna), dla osób zawodowo narażonych na działanie promieniowania jonizującego wynosi w ciągu roku kalendarzowego
Teleradioterapia 4D na etapie planowania leczenia wykorzystuje obrazy
W którym miejscu, zgodnie z zasadami wykonywania badania EKG, należy umocować żółtą elektrodę przedsercową V2?
W radiografii mianem SID określa się
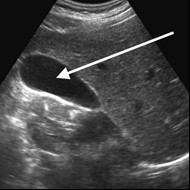
Na obrazie ultrasonograficznym jamy brzusznej strzałką wskazano
Do wczesnych odczynów popromiennych po radioterapii zalicza się
Bezwzględnym przeciwwskazaniem do wykonania badania rezonansem magnetycznym jest
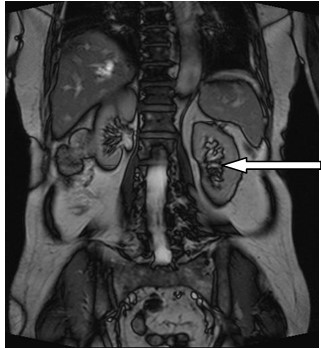
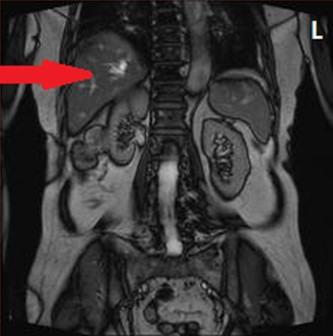
Na obrazie MR jamy brzusznej strzałką wskazano
W leczeniu izotopowym tarczycy podaje się
Pozytywny środek cieniujący najczęściej stosowany w rentgenodiagnostyce powinien charakteryzować się
W których projekcjach podstawowych wykonuje się standardowe badanie mammograficzne?
W standardowym badaniu EEG elektrody P3, P4 i Pz umieszcza się na skórze głowy pacjenta nad płatami
Która składowa prawidłowej krzywej EKG odpowiada powolnej repolaryzacji komór mięśnia sercowego?
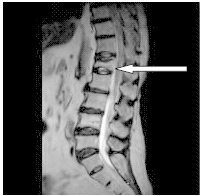
Na obrazie rezonansu magnetycznego strzałką oznaczono patologiczny kręg
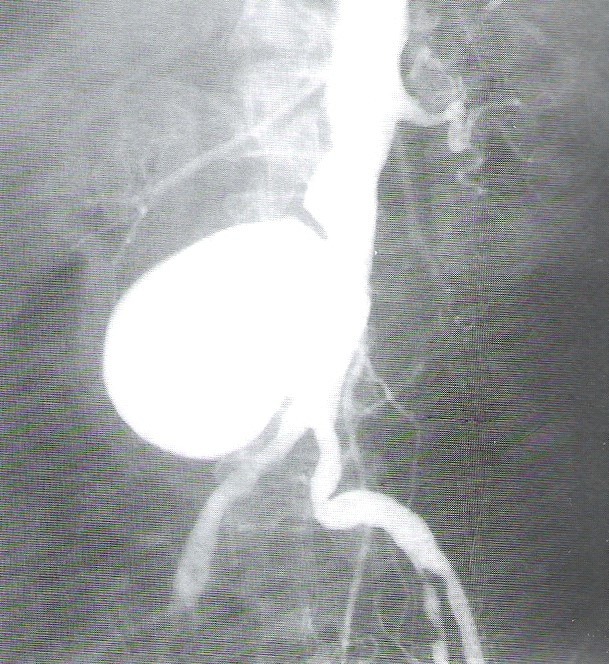
Na obrazie rentgenowskim strzałką zaznaczono
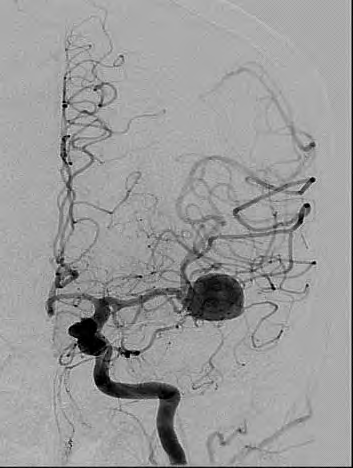
Którą patologię uwidoczniono w badaniu angiograficznym?
Elementem pomocniczym w radioterapii, zapewniającym powtarzalność ułożenia w pozycji terapeutycznej, a także unieruchomienie pacjenta, jest
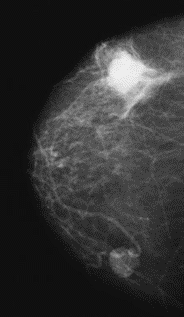
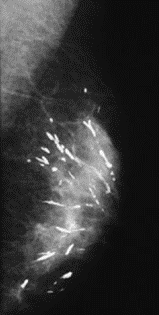
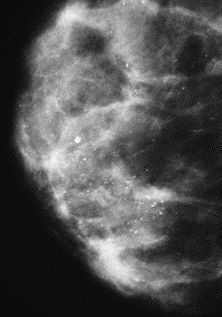
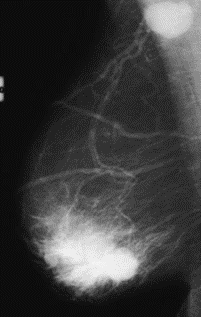
Na którym obrazie rentgenowskim sutka uwidoczniono zmianę patologiczną w obrębie węzłów chłonnych?
Którą strukturę anatomiczną zaznaczono strzałką na rentgenogramie?
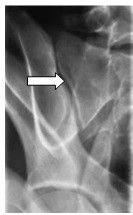
Do badania mammograficznego w projekcji skośnej przyśrodkowo-bocznej kąt lampy powinien być ustawiony w zakresie
Który radioizotop stosuje się do badania scyntygraficznego kości?
Na obrazie TK zaznaczono zatokę
W badaniu EKG elektrodę przedsercową V4 należy umocować
Promieniowanie rentgenowskie jest
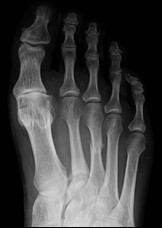
Na radiogramie stopy uwidocznione jest złamanie trzonu
„Ognisko zimne” w obrazie scyntygraficznym określa się jako
W której technice obrazowania zostają zarejestrowane jednocześnie dwa przeciwbieżne kwanty promieniowania gamma o równej energii 511 keV?
Na elektrokardiogramie zarejestrowano
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
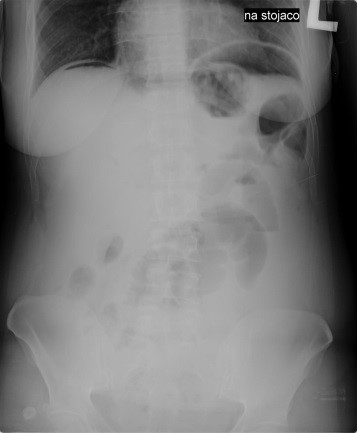
Radiogram jamy brzusznej uwidacznia