Pytanie 1
Jak oznacza się w systemie międzynarodowym czwarty górny ząb mleczny po stronie prawej?
Wynik: 30/40 punktów (75,0%)
Wymagane minimum: 20 punktów (50%)
Jak oznacza się w systemie międzynarodowym czwarty górny ząb mleczny po stronie prawej?
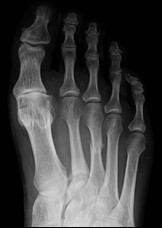
Na radiogramie stopy uwidocznione jest złamanie trzonu
Promieniowanie jonizujące pośrednio to
Obszary napromieniania w technice IMRT w trakcie wykonywania zabiegu radioterapeutycznego wyznacza
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
Zgodnie z procedurą wzorcową w badaniu MR należy ułożyć pacjenta na brzuchu do diagnostyki
Do zdjęcia rentgenowskiego żeber w projekcji skośnej tylnej pacjenta należy ustawić
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
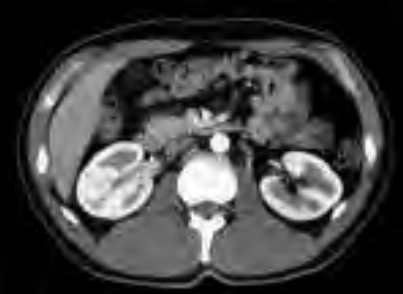
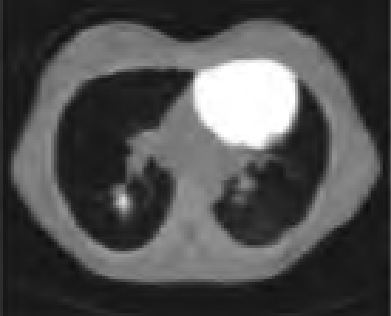
Na którym obrazie zarejestrowano badanie scyntygraficzne?
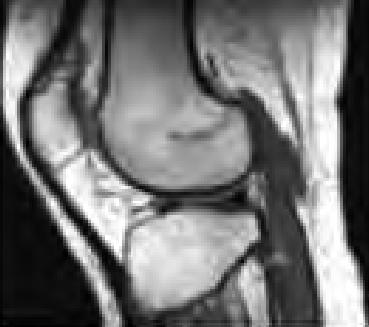
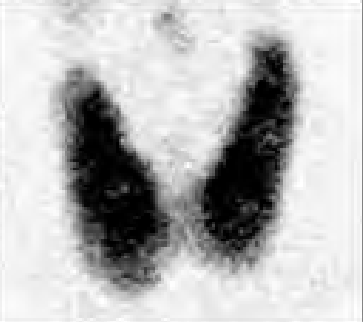
Pracownia radioterapii z przyspieszaczem liniowym jest obszarem
W badaniu EEG w systemie „10-20” elektrody w okolicy skroniowej oznaczone są literą
W scyntygrafii perfuzyjnej płuc pacjentowi podawany jest radioizotop
Który typ głowicy ultrasonograficznej przedstawiono na ilustracji?

W radiologii analogowej lampy rentgenowskiej z tubusem używa się do wykonania zdjęcia
Które znaczniki są wykorzystywane w scyntygrafii tarczycy?
Hiperfrakcjonowanie dawki w radioterapii oznacza napromienienie pacjenta
Źródłem promieniowania protonowego stosowanego w radioterapii jest
Na którym obrazie rentgenowskim sutka uwidoczniono zmianę patologiczną w obrębie węzłów chłonnych?
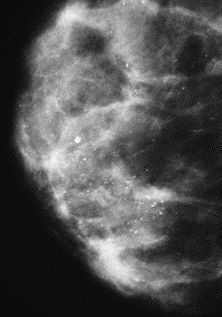
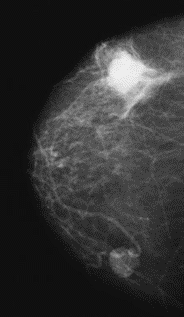
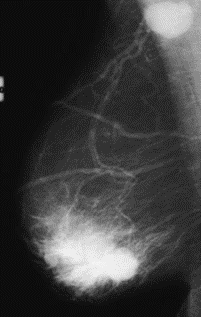
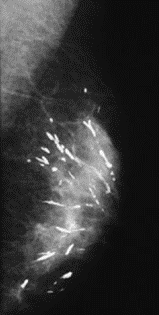
Po podaniu kontrastu obraz zmian nowotworowych w badaniu MR najlepiej uwidacznia się w sekwencji
Ile razy i jak zmieni się wartość natężenia promieniowania X przy zwiększeniu odległości OF ze 100 cm do 200 cm?
W medycynie nuklearnej wykorzystuje się:
Zaznaczona strzałką struktura anatomiczna na obrazie rezonansu magnetycznego to
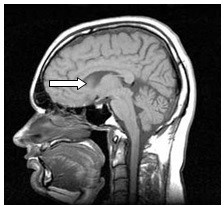
Czas repetycji w obrazowaniu metodą rezonansu magnetycznego to
Który środek kontrastujący stosuje się w badaniu metodą rezonansu magnetycznego?
Proces chemicznego wywoływania radiogramów polega na
Które ciało obce w obszarze badania nie stanowi przeciwwskazania do wykonania MR?
Wskazaniem do wykonania scyntygrafii perfuzyjnej jest
Brachyterapia wewnątrzjamowa jest wykorzystywana podczas leczenia nowotworu
Przemiana promieniotwórcza radu w ren opisana wzorem \( {}_{88}^{226}\text{Ra} \to {}_{86}^{222}\text{Rn} + {}_{2}^{4}\text{He} \) jest rozpadem
Co określa M₀ w systemie klasyfikacji nowotworów TNM?
Który załamek w zapisie EKG odpowiada zjawisku depolaryzacji przedsionków mięśnia sercowego?
W której technice brachyterapii stosuje się źródła promieniowania o mocy dawki 2-12 Gy/h?
Wskazaniem do wykonania przesiewowego badania densytometrycznego jest
Zdjęcie którego zęba górnego zlecił na skierowaniu lekarz stomatolog?
W badaniu mammograficznym jedną z podstawowych projekcji jest projekcja
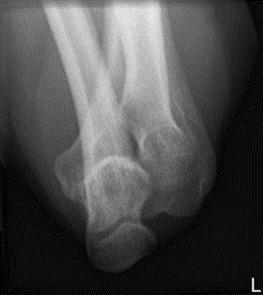
Które zdjęcie RTG stawu łokciowego zostało wykonane w projekcji skośnej w rotacji zewnętrznej?
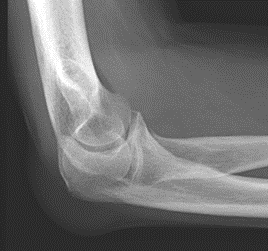
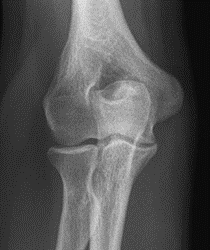
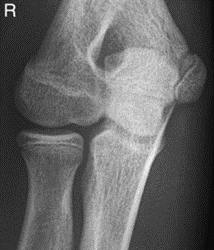
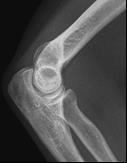
Które odprowadzenie w badaniu EKG rejestruje różnice potencjałów pomiędzy lewym a prawym przedramieniem?
Jaki kolor ma warstwa korowa kości w badaniu MR na obrazie T1- zależnym?
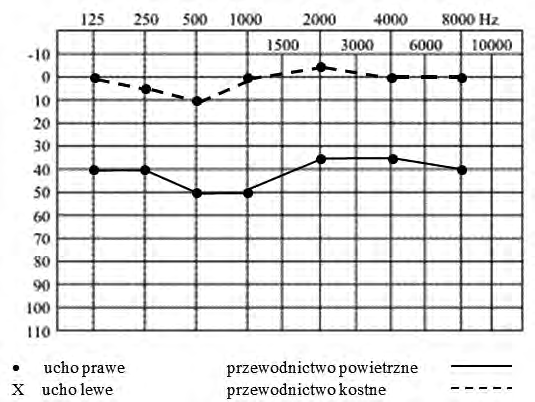
Na podstawie zapisu badania audiometrycznego rozpoznano u pacjenta uszkodzenie słuchu
Którą strukturę anatomiczną i w jakiej projekcji uwidoczniono na radiogramie?