Pytanie 1
Wskaż osłonę radiologiczną, która jest stosowana w pracowniach radiodiagnostyki stomatologicznej.




Wynik: 35/40 punktów (87,5%)
Wymagane minimum: 20 punktów (50%)
Wskaż osłonę radiologiczną, która jest stosowana w pracowniach radiodiagnostyki stomatologicznej.




Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest
W scyntygrafii dynamiczne badanie najczęściej rozpoczyna się
Badanie cewki moczowej polegające na wstecznym wprowadzeniu środka kontrastowego to
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
W obrazowaniu MR wykorzystuje się moment magnetyczny
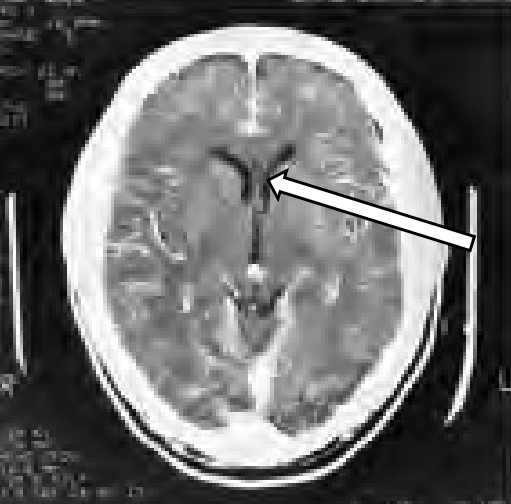
Którą strukturę anatomiczną oznaczono na skanie TK głowy?
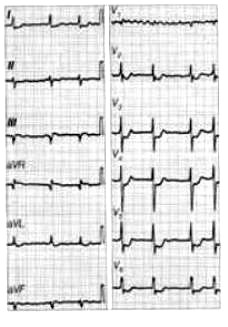
Na elektrokardiogramie uwidoczniono
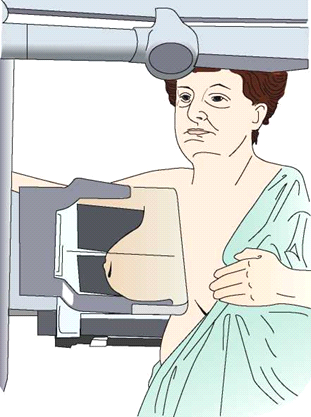
Ilustracja przedstawia pozycjonowanie pacjentki do badania mammograficznego w projekcji
Do zadań technika elektroradiologa w pracowni hemodynamicznej należy
DSA to cyfrowa
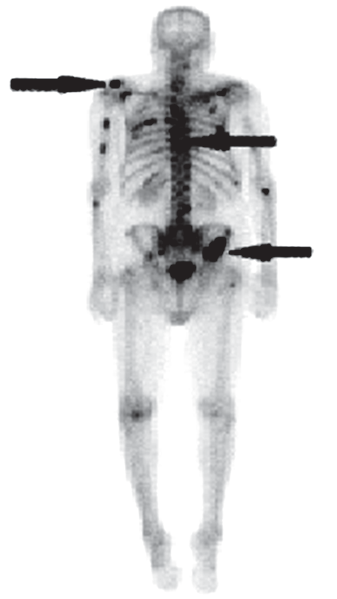
Na scyntygramie kości strzałkami oznaczono ogniska
Świeżo wynaczyniona krew na obrazach TK głowy bez podania środka kontrastowego ukazuje się jako obszar
Jednostką indukcji magnetycznej jest
Zdjęcie zatok przynosowych wykonuje się w pozycji
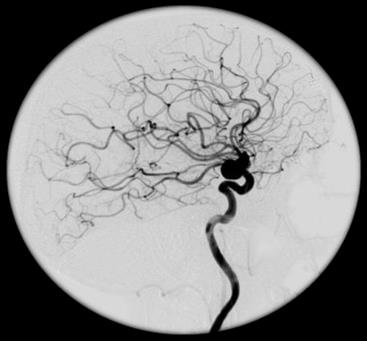
W przedstawionym na ilustracji obrazie badania angiograficznego uwidoczniono
Pielografia to badanie układu
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
Kasety do pośredniej radiografii cyfrowej CR są wyposażone
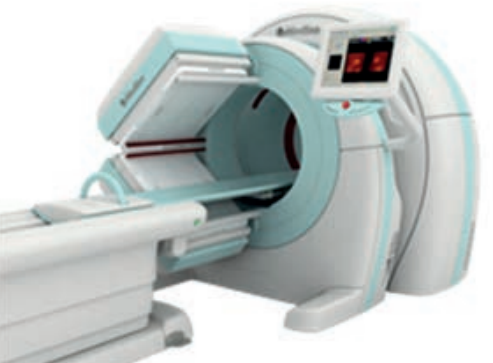
Które urządzenie zostało przedstawione na fotografii i w jakiej pracowni znajduje zastosowanie?
Podczas wykonywania badania EKG czarną elektrodę kończynową należy umieścić na kończynie dolnej
Technikę bramkowania oddechowego stosuje się w badaniu MR
Która sekwencja obrazowania MR wykorzystuje impulsy RF o częstotliwości rezonansowej tłuszczu do tłumienia sygnału pochodzącego z tkanki tłuszczowej?
Standardowe badanie USG średniej wielkości piersi wykonuje się głowicą w zakresie częstotliwości
Do badania MR nadgarstka pacjenta należy ułożyć
W pozytonowej tomografii emisyjnej PET zostaje zarejestrowane promieniowanie powstające podczas
Rytm alfa i beta rejestruje się podczas badania
W technice napromieniania SSD mierzona jest odległość źródła promieniowania
Za wyrównanie ciśnienia między uchem środkowym a otoczeniem odpowiada
Który system informatyczny jest wykorzystywany do archiwizowania i przesyłania obrazów na stacje diagnostyczne w standardzie DICOM?
Który środek ochrony radiologicznej należy zastosować podczas badania czaszki 53-letniego pacjenta za pomocą tomografii komputerowej?
W zapisie EKG załamek U występuje bezpośrednio po załamku
W badaniu PETCT radioizotop ulega
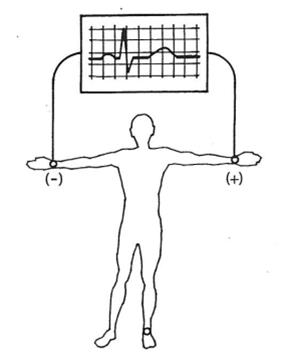
Które odprowadzenie elektrokardiograficzne przedstawiono na ilustracji?
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
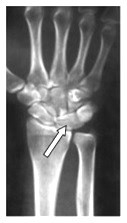
Na obrazie radiologicznym nadgarstka strzałką zaznaczona jest kość
Do zadań technika elektroradiologa w pracowni hemodynamicznej należy
Skrótem HRCT (High Resolution Computed Tomography) określa się tomografię komputerową
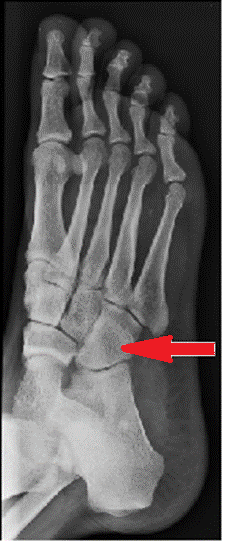
Na radiogramie stopy strzałką wskazano kość