Pytanie 1
Metoda analityczna, która polega na wyznaczaniu masy osadzonej substancji z roztworu z wykorzystaniem azotanu(V) srebra, to
Wynik: 23/40 punktów (57,5%)
Wymagane minimum: 20 punktów (50%)
Metoda analityczna, która polega na wyznaczaniu masy osadzonej substancji z roztworu z wykorzystaniem azotanu(V) srebra, to
Wszelkie działania, które powinny zostać podjęte w celu usunięcia zidentyfikowanej niezgodności CCP (krytyczne punkty kontroli) w systemie HACCP, to działania
System HACCP – System Analizy Zagrożeń i Krytycznych Punktów Kontroli, stanowi zbiór wzajemnie powiązanych ze sobą procedur, które w całości tworzą system zarządzania bezpieczeństwem żywności.
W mikrobiologii metoda sterylizacji przy użyciu suchego, gorącego powietrza zalicza się do
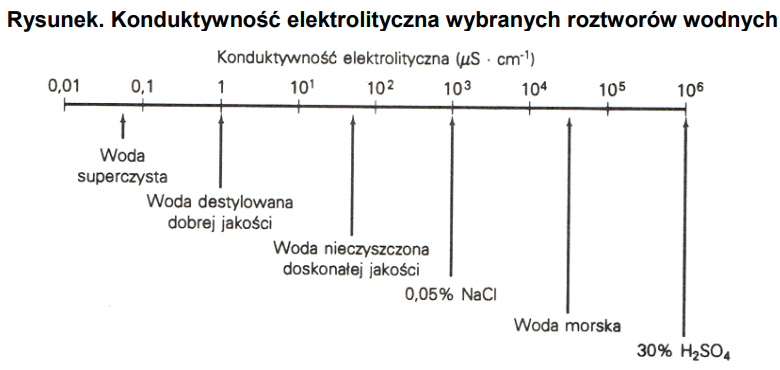
Twardość całkowita wody
Konduktywność elektrolityczna wody destylowanej stosowanej w laboratorium chemicznym wynosi 0,001 mS cm-1. Z analizy danych przedstawionych na rysunku wynika, że woda ta jest
Badanie szczegółowej struktury komórek roślinnych oraz zwierzęcych, jak również rozmieszczenia atomów w kryształach metali i minerałów, jest możliwe dzięki wykorzystaniu mikroskopu
Na rysunku przedstawiono

Oznaczanie wagowe substancji jest możliwe, kiedy analizowany związek jest
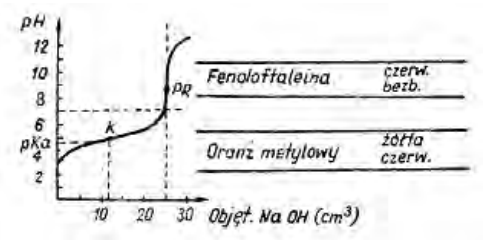
Rolę wskaźnika w oznaczeniu opisanym w ramce pełni
| Do kolby miarowej o pojemności 250 cm3 odpipetować 25 cm3 3% wody utlenionej i dopełnić wodą do kreski. Do kolby stożkowej o pojemności 250 cm3 odpipetować 20 cm3 próbki rozcieńczonej wody utlenionej, dodać 25 cm3 kwasu siarkowego(VI) (1+4) i miareczkować roztworem manganianu(VII) potasu o stężeniu 0,02 mol/dm3 do pojawienia się trwałego różowego zabarwienia. |
Zgodnie z klasyfikacją Bunsena, aniony przypisywane są do jednej z 7 grup analitycznych na podstawie różnic w ich zachowaniu względem jonów
W ramce zamieszczono opis wykonania oznaczenia metodą
| Oznaczenie aktywności amylaz opiera się na pomiarze ilości rozpuszczonej skrobi, co określa się na podstawie zmiany intensywności zabarwienia w mieszaninie reakcyjnej, w skład której wchodzi jod. |
Znając zasadę działania polarymetru i wzór - można oznaczyć stężenie
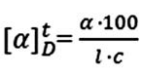
W celu identyfikacji cukru sporządzono jego roztwór i przelano do trzech probówek. Następnie przeprowadzono doświadczenia, których wyniki zapisano w tabeli:
Badanym cukrem była
| Badany roztwór | Dodany odczynnik | Obserwacje |
|---|---|---|
| Probówka 1. | Cu(OH)2 | Zawiesina Cu(OH)2 rozpuściła się, a roztwór przyjął szafirową barwę |
| Cu(OH)2 | Po ogrzaniu probówki pojawił się ceglasto-czerwony osad | |
| Probówka 2. | [Ag(NH3)2]+ | Po ogrzaniu na ściankach probówki pojawiło się srebro metaliczne |
| Probówka 3. | Br2(aq) + roztwór NaHCO3 | Woda bromowa uległa odbarwieniu |
W celu przeprowadzenia bezpośredniego testu ELISA należy postąpić zgodnie z procedurą

Jak nazywana jest technika analityczna, która polega na pomiarze przewodnictwa roztworu umieszczonego pomiędzy dwiema elektrodami, do których doprowadzany jest prąd przemienny?
W jakiej metodzie analizy instrumentalnej wykorzystuje się zdolność substancji optycznie aktywnej do skręcania płaszczyzny światła spolaryzowanego?
Przy pomocy polarymetru wykonuje się pomiar
Zamieszczony wykres przedstawia krzywą miareczkowania
W próbce wody, w której stwierdzono obecność 60,0 mg żelaza, dokonano oznaczenia jego zawartości za pomocą spektrofotometrii, uzyskując wynik 59,1 mg. Jaki jest błąd względny tego oznaczenia?
Na podstawie danych zawartych w tabeli, wskaż zestaw substancji uporządkowanych według rosnącej temperatury topnienia.
| Substancja | pirydyna | benzen | etanol |
|---|---|---|---|
| Temperatura wrzenia [°C] | 115,5 | 80,1 | 78,3 |
| Temperatura topnienia [°C] | -41,6 | 5,5 | -114,1 |
Określ typ destylacji, który polega na przemianie składnika mieszaniny substancji organicznych w stan pary w temperaturze niższej od jego temperatury wrzenia.
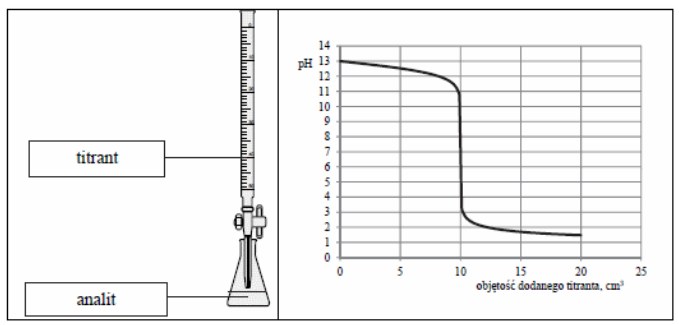
Na podstawie rysunku analitem może być roztwór
Podłoża o płynnej konsystencji stosuje się w celu
Na zmiareczkowanie odważki KOH zużyto 30,0 cm3 roztworu HCl o stężeniu 0,1 mol/dm3. Ile gramów KOH zawierała odważka?
| MKOH = 56 g/mol |
Do zmiareczkowania próbki wodorotlenku sodu o objętości 25 cm3 wykorzystano 20 cm3 roztworu kwasu solnego o stężeniu 0,1020 mol/dm3. Jakie jest stężenie molowe roztworu NaOH?
Jakie urządzenie wykorzystuje się do pomiaru zasolenia wody?
Na jakich materiałach wykonuje się podłoża mikrobiologiczne?
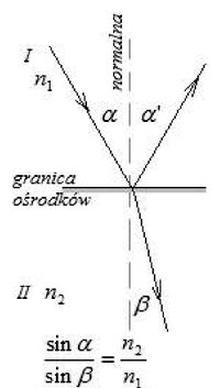
Na rysunku przedstawiono graficzną interpretację zależności wynikających z prawa
Właściwością jakościową produktów technologicznych jest
Jakie substancje stosuje się do barwienia preparatów mikroskopowych według metody Grama?
W tabeli przedstawiono gęstość wodnych roztworów gliceryny w temperaturze 20°C w zależności od jej stężenia wyrażonego w % wagowych.
Z informacji zawartych w tabeli wynika, że stężenie gliceryny o gęstości 1,10 g/cm³ wynosi
| % wagowy gliceryny | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
|---|---|---|---|---|---|---|---|---|---|---|
| [g/cm3] gęstość | 1,022 | 1,047 | 1,072 | 1,099 | 1,126 | 1,153 | 1,180 | 1,208 | 1,235 | 1,261 |
Kwasowość mleka można zmierzyć w stopniach Soxhleta-Henkla [oSH], co oznacza liczbę cm3 roztworu NaOH o stężeniu 0,25 mol/dm3 używaną do zmiareczkowania 100 cm3 próbki. Jeśli na zmiareczkowanie mleka o objętości 50 cm3 potrzeba 3,25 cm3 roztworu NaOH o stężeniu 0,25 mol/dm3, to kwasowość mleka wynosi
Nie można wytworzyć roztworu mianowanego, wykorzystując jako substancję wyjściową naważkę
Proces kondensacji i osuszania substancji termolabilnych, takich jak białka oraz kwasy nukleinowe, za pomocą suszenia zamrożonego materiału w obniżonym ciśnieniu poprzez sublimację lodu, określany jest jako
Do metod instrumentalnych w analizach jakościowych nie zaliczają się techniki
Jakim wskaźnikiem posługujemy się w miareczkowaniu redoksometrycznym?
Próbkę żywności poddano ogrzewaniu w suszarce laboratoryjnej, a następnie obliczono X według wzoru. Wartość liczbowa X określa
$$ X = \frac{b - c}{a - c} \times 100\% $$gdzie:
\( a \) – masa naczyńka z badaną próbką przed ogrzewaniem [g]
\( b \) – masa naczyńka z badaną próbką po ogrzewaniu [g]
\( c \) – masa pustego naczyńka [g]
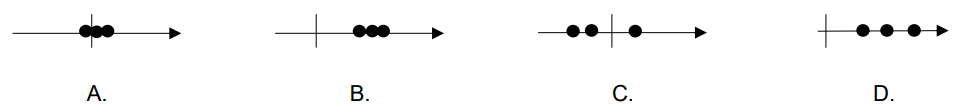
Na którym rysunku przedstawiono schemat metody dokładnej i nieprecyzyjnej?
Na zamieszczonym wykresie cyfrą 2 oznaczono odchylenie

Jakie składniki są potrzebne do przygotowania pożywki, która pozwala na hodowlę bakterii?