Pytanie 1
Który detektor w radiografii wymaga laserowego czytnika obrazu?
Wynik: 36/40 punktów (90,0%)
Wymagane minimum: 20 punktów (50%)
Który detektor w radiografii wymaga laserowego czytnika obrazu?
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
W badaniu PETCT radioizotop ulega
Zgodnie ze standardami do wykonania zdjęcia bocznego czaszki, należy zastosować kasetę o wymiarze
W badaniu PET CT wykorzystuje się radioizotopy emitujące promieniowanie
Promieniowanie rentgenowskie powstaje w wyniku hamowania
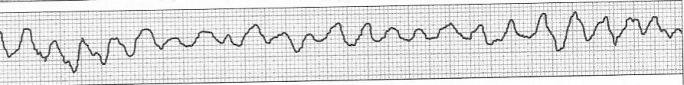
Zamieszczony elektrokardiogram przedstawia
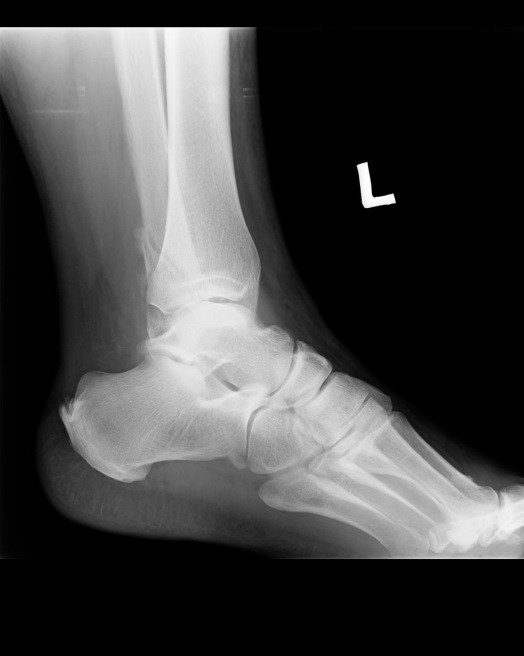
Na obrazie radiologicznym uwidoczniono złamanie kości
Badanie gęstości mineralnej kości metodą DXA należy wykonać
Warstwa półchłonna (WP) służy do obliczania
Pomiar densytometryczny BMD metodą DXA z kręgosłupa powinien obejmować kręgi
Jak konwencjonalnie frakcjonuje się dawkę w teleradioterapii?
Zastosowana w badaniu radiologicznym kratka przeciwrozproszeniowa powoduje
Więzka promieniowania X to
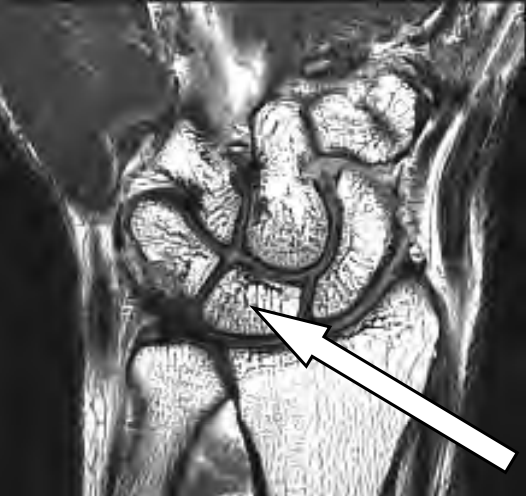
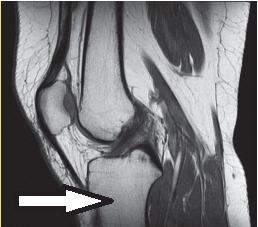
Na obrazie RM nadgarstka lewego strzałką oznaczono kość
Teleradioterapia 4D na etapie planowania leczenia wykorzystuje obrazy
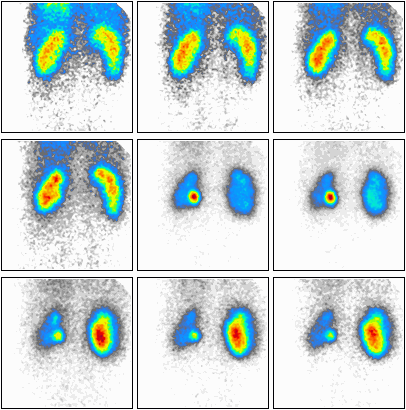
Podczas którego badania zostały zarejestrowane przedstawione obrazy?
Jak zgodnie ze standardem należy ustawić pacjenta do badania rentgenowskiego w skosie tylnym prawym?
Na którym obrazie rentgenowskim sutka uwidoczniono zmianę patologiczną w obrębie węzłów chłonnych?
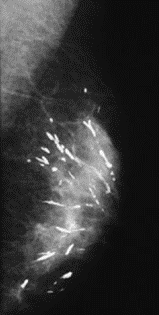
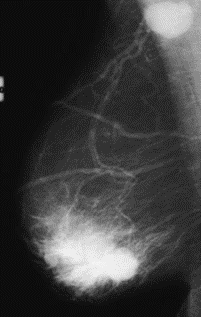
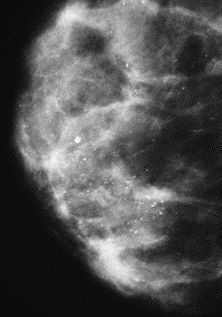
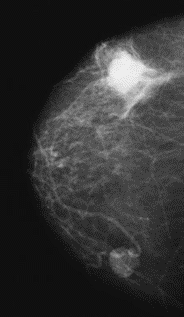
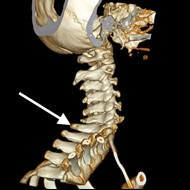
Na obrazie TK kręgosłupa strzałką wskazano wyrostek
Którą kość oznaczono na obrazie rezonansu magnetycznego?
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
Który środek ochrony radiologicznej należy zastosować podczas badania czaszki 53-letniego pacjenta za pomocą tomografii komputerowej?
Podczas wykonywania zdjęcia rentgenowskiego klatki piersiowej w celu ochrony radiologicznej pacjenta należy zastosować
Do wczesnych odczynów popromiennych po radioterapii zalicza się
W medycynie nuklearnej wykorzystuje się:
Jednym z kryteriów poprawnie wykonanego badania spirometrycznego jest czas trwania natężonego wydechu, który powinien wynosić u osób powyżej 10 roku życia co najmniej
W której technice brachyterapii stosuje się źródła promieniowania o mocy dawki 2-12 Gy/h?
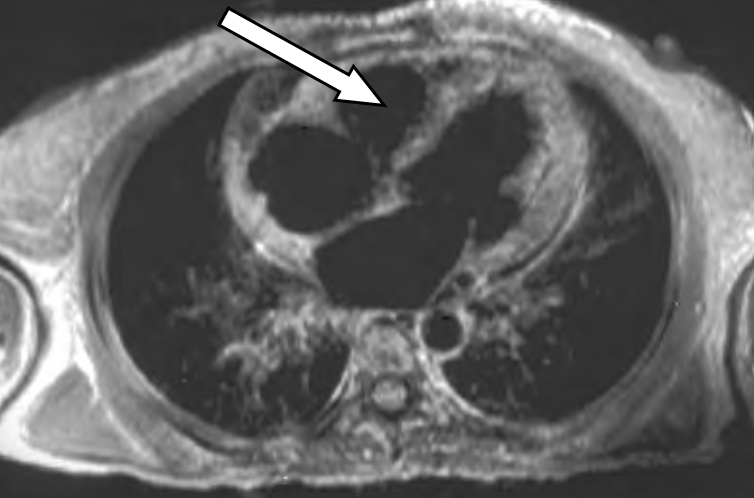
Na skanie rezonansu magnetycznego serca oznaczono
W zapisie EKG załamki P dodatnie w odprowadzeniu I i II, a ujemne w aVR oraz częstotliwość rytmu mniejsza niż 60/min wskazują na
Na radiogramie uwidoczniono
W scyntygrafii kośćca „ogniska gorące” oznaczają miejsca
Która struktura może być oknem akustycznym w badaniu ultrasonograficznym?
Kiedy w procesie terapii wykonuje się badanie CBCT (cone beam computed tomography)?
Pozytywny środek cieniujący najczęściej stosowany w rentgenodiagnostyce powinien charakteryzować się
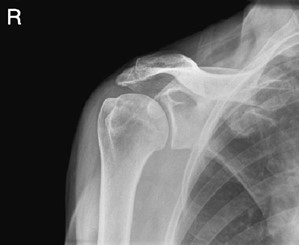
Na radiogramie stawu barkowego strzałką wskazano
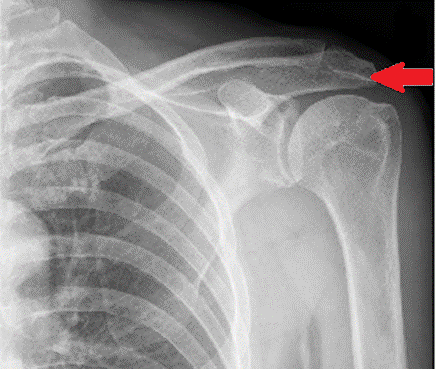
Która właściwość promieniowania X pozwala na skierowanie promienia centralnego na wybrany punkt topograficzny podczas wykonywania badania radiologicznego?
Obiektywną metodą badania słuchu jest audiometria
Wynik badania słuchu metodą audiometrii tonalnej wskazuje na
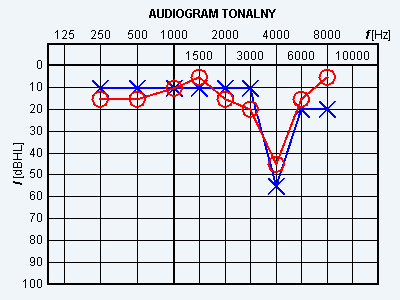
Zadaniem technika elektroradiologii w pracowni badań naczyniowych jest