Pytanie 1
Piktogram nie jest konieczny dla
Wynik: 25/40 punktów (62,5%)
Wymagane minimum: 20 punktów (50%)
Piktogram nie jest konieczny dla
Do pojemników na odpady stałe, które są przeznaczone do utylizacji, nie można wprowadzać bezpośrednio cyjanków oraz związków kompleksowych zawierających jony cyjankowe z powodu
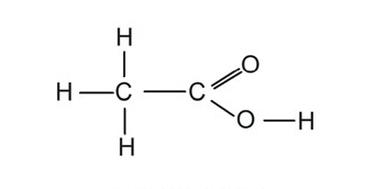
Związek o podanym wzorze to kwas
Jakie urządzenie jest wykorzystywane do procesu ekstrakcji?
Na rysunku przedstawiono przyrząd do pobierania próbek

Aby uzyskać roztwór CuSO4 o stężeniu 15%, w jakim stosunku należy połączyć roztwory 10% oraz 20%?
Aby wykonać czynności analityczne wskazane w ramce, należy użyć:
| Otrzymaną do badań próbkę badanego roztworu rozcieńczyć wodą destylowaną w kolbie miarowej o pojemności 100 cm3 do kreski i dokładnie wymieszać. Następnie przenieść pipetą 10 cm3 tego roztworu do kolby stożkowej, dodać ok. 50 cm3 wody destylowanej. |
Jakie roztwory chemiczne powinny być stanowczo pobierane przy włączonym dygestorium?
Którego odczynnika należy użyć do przygotowania roztworu wzorcowego, zawierającego jony \( \text{Fe}^{3+} \)?
Jaką masę chlorku sodu można znaleźć w 150 g roztworu soli o stężeniu 5% (m/m)?
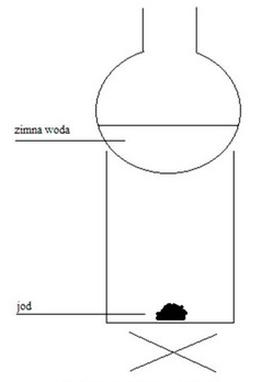
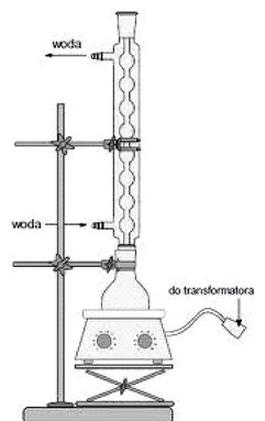
Na rysunku przedstawiono zestaw do oczyszczania jodu w procesie
Aby obliczyć gęstość cieczy przy użyciu metody hydrostatycznej, należy zastosować
Zaleca się schładzanie próbek wody transportowanych do laboratorium do temperatury
Wskaź sprzęt laboratoryjny, który znajduje się w zestawie do filtracji pod obniżonym ciśnieniem?
Czy odpady laboratoryjne zawierające jony metali ciężkich powinny zostać poddane obróbce przed umieszczeniem ich w odpowiednio oznaczonej pojemności?
Jaką masę siarczanu(VI) miedzi(II)-woda(1/5) należy poddać suszeniu, aby otrzymać 300 g soli bezwodnej?
| CuSO4 · 5H2O → CuSO4 + 5H2O |
| (MCuSO4·5H2O = 249,5 g/mol, MCuSO4 = 159,5 g/mol, MH2O = 18,0 g/mol) |
Rozpuszczalność siarczanu(VI) potasu przy temperaturze 30oC wynosi 13 g na 100 g wody. Jaką masę tego związku należy dodać do wody, aby uzyskać 500 g roztworu nasyconego?
Na ilustracji zobrazowano urządzenie do
Resztki szkła, osadników czy inne odpady stałe powstałe w laboratorium analitycznym powinny być umieszczone
Do grupy reagentów o szczególnym zastosowaniu nie wlicza się
Na etykietach substancji chemicznych można znaleźć oznaczenia literowe R i S (zgodnie z regulacjami CLP: H i P), które wskazują
W próbkach obecne są składniki, które znacznie różnią się pod względem zawartości. Składnik, którego procentowy udział w próbce jest niższy od 0,01%, nazywamy
Jakie środki stosuje się do czyszczenia szkła miarowego, które zostało zanieczyszczone substancjami tłustymi?
Na diagramie przedstawiającym proces pobierania prób środowiskowych do analizy literą Y oznaczono próbkę
Dla cieczy bezbarwnej odczyt w biurecie pokazanej na rysunku wynosi

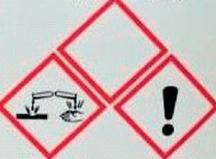
Według zasady pierwszeństwa, znajdując na opakowaniu zbiorczym odczynnika piktogramy pokazane na rysunku, należy zwrócić szczególną uwagę na to, że substancja jest
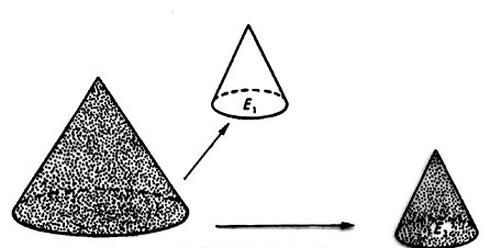
Rysunek przedstawia etapy zmniejszania próbki ogólnej. Jest to metoda
Przeprowadzono reakcję 13 g cynku z kwasem solnym zgodnie z równaniem: Zn + 2 HCl → ZnCl2 + H2↑. Otrzymano 1,12 dm3 wodoru (w warunkach normalnych). Masy molowe to: MZn = 65 g/mol, MH = 1g/mol, MCl = 35,5g/mol. Jaka jest wydajność tego procesu?
Na rysunku przedstawiono zestaw
Analiza technicznego kwasu solnego dała następujące wyniki: 30% HCl, 0,008% H2SO4, 0,04% Fe.
Korzystając z zamieszczonej tabeli wymagań, określ gatunek kwasu, pamiętając, że decyduje o nim najgorszy wskaźnik.
| Wymagania chemiczne dotyczące kwasu siarkowego | ||||
| Wymagania | Gatunki | |||
| I | II | III | IV | |
| Chlorowodór, % | > 33 | > 29 | > 28 | > 27 |
| Kwas siarkowy(VI) w przel. na SO42-, % | < 0,009 | < 0,5 | < 1,6 | < 1,8 |
| Żelazo (Fe3+), % | < 0,005 | < 0,03 | < 0,03 | < 0,05 |
Przedstawiony na rysunku sprzęt służy do

Podaj nazwę reagentu chemicznego, który w specyficznych warunkach reaguje tylko z jednym jonem, pierwiastkiem lub związkiem chemicznym?
W celu uzyskania czystej substancji próbkę zawierającą nitroanilinę poddano krystalizacji. Oblicz masę odważki nitroaniliny, pobranej do krystalizacji, jeśli uzyskano 1,5 g czystego związku, a wydajność krystalizacji wynosiła 75%.
Aby otrzymać roztwór AgNO3 (masa molowa AgNO3 to 169,8 g/mol) o stężeniu 0,1 mol/dm3, należy
Jakie urządzenie wykorzystuje się do pobierania próbek gazów?
Transportuje się pobrane próbki wody do analiz fizykochemicznych
Który sposób przechowywania próbek żywności jest niezgodny z Rozporządzeniem Ministra Zdrowia?
| Fragment Rozporządzenia Ministra Zdrowia w sprawie pobierania i przechowywania próbek żywności przez zakłady żywienia zbiorowego typu zamkniętego |
| (...) Zakład przechowuje próbki, przez co najmniej 3 dni, licząc od chwili, kiedy cała partia została spożyta w miejscu wyłącznym właściwym do tego celu oraz w warunkach zapewniających utrzymanie temperatury +4°C lub niższej, w zależności od przechowywanego produktu. Miejsce przechowywania próbek musi być tak zabezpieczone, aby dostęp do niego posiadał tylko kierujący zakładem lub osoba przez niego upoważniona. |
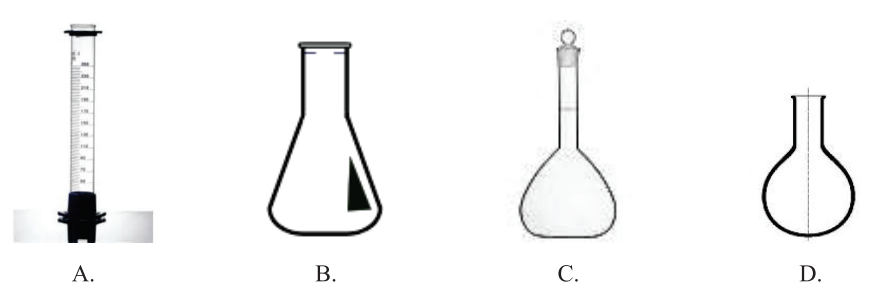
W celu przygotowania roztworu mianowanego należy użyć sprzętu przedstawionego na rysunku
Oblicz masę wapienia, który został rozłożony, jeśli w trakcie reakcji uzyskano 44,8 dm3 CO2 (w warunkach standardowych).
MC = 12 g/mol, MCa = 40 g/mol, MO = 16 g/mol
W tabeli zamieszczono temperatury wrzenia niektórych składników powietrza. Na podstawie tych danych podaj, który ze składników oddestyluje jako ostatni.
| Temperatura wrzenia °C | Składniki |
|---|---|
| -245,9 | Neon |
| -182,96 | Tlen |
| -195,8 | Azot |
| -185,7 | Argon |