Pytanie 1
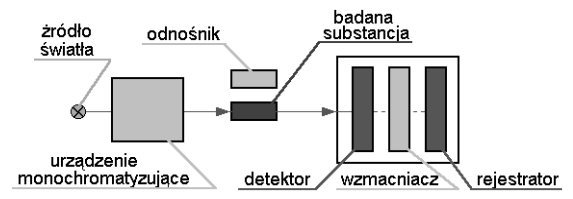
Schemat blokowy przedstawia
Wynik: 18/40 punktów (45,0%)
Wymagane minimum: 20 punktów (50%)
Schemat blokowy przedstawia

Na podstawie informacji zawartych w tabeli wskaż, który adsorbent należy zastosować podczas oznaczania karotenów.
| Podział adsorbentów według zastosowania | |
|---|---|
| Adsorbent | Przykłady zastosowania |
| Tlenek glinu zasadowy | aminy, węglowodory, alkaloidy, zasady heterocykliczne |
| Tlenek glinu obojętny | aminy, amidy, alkaloidy, glikozydy |
| Tlenek glinu kwasowy | barwniki, związki kwasowe |
| Żel krzemionkowy | aminy, kwasy karboksylowe, amidy, węglowodory, inne związki obojętne |
Zjawisko opisane w zamieszczonej informacji to
| Jeżeli w wodzie zostanie rozpuszczona α-D-glukopiranoza, to roztwór tuż po rozpuszczeniu wykazuje skręcalność właściwą [α]D = +112,2°, lecz w miarę upływu czasu skręcalność ta stopniowo spada do wartości charakterystycznej w stanie równowagi, mianowicie [α]D = +52,7° |
W tabeli przedstawiono charakterystykę
| |||||||||||||||
Przeprowadzano analizę jakościową próbki według schematu:
Badana próbka zawierała kation
| badany roztwór zawierający jony X2+ | |
| + roztwór HCl | |
| XCl2↓ biały osad | |
| + H2O: ogrzać | |
| roztwór X2+: podzielić na 2 części | |
| + roztwór KI | oziębić |
| XI2 żółty osad | XCl2↓ biały osad |
W celu preparatywnego rozdzielania aminokwasów wykorzystuje się metodę elektroforezy, która bazuje na
Jedną z kluczowych cech enzymów jest
W ramce scharakteryzowano odczynniki
| Łączą się z danym jonem ubocznym, wiążąc go w trwałe zespoły i tym samym wyłączają go z udziału w roztworze lub obniżają znacznie jego stężenie. |
Do początkowych zanieczyszczeń atmosferycznych zalicza się
Przedstawiony na rysunku zestaw jest stosowany podczas oznaczania
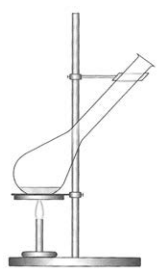
Aby przygotować oznaczenia spektrofotometryczne kwasu acetylosalicylowego w zakresie nadfioletu, należy sporządzić cztery wzorce o objętości 50 cm3 każdy. Wzorce te powinny być stworzone poprzez odważenie kwasu salicylowego z dokładnością do 0,0001 g oraz rozpuszczenie odważonych ilości w 0,1000 mol/dm3 roztworze NaOH. Jaki sprzęt oraz w jakiej ilości, oprócz wagi analitycznej i łyżeczki, trzeba użyć do przygotowania tych wzorców?
Analiza wody basenowej w celu wykrycia bakterii polega na podgrzewaniu próbki w inkubatorze przez 48 godzin w temperaturze 36±2°C. Jaki proces jest opisany?
Której z metod nie wykorzystuje się do pomiaru stężenia soli w solankach?
Jakim urządzeniem mierzy się zasolenie gleby?
Jakie badanie chemiczne dotyczące wody przeprowadza się przy użyciu miareczkowania kompleksometrycznego?
Jakie właściwości mierzą wiskozymetry?
Rysunek przedstawia krzywą miareczkowania
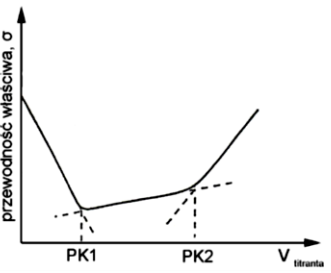
Gęstość wody w temperaturze 25oC wynosi
| T [K] | ||
|---|---|---|
| T [K] | d [g/cm³] | η [cP] |
| 293 | 0,99823 | 1,0050 |
| 298 | 0,99707 | 0,8937 |
| 303 | 0,99567 | 0,8007 |
| 308 | 0,99406 | 0,7225 |
| 313 | 0,99222 | 0,6560 |
| 318 | 0,99025 | 0,5988 |
| 323 | 0,98807 | 0,5494 |
| 328 | 0,98573 | 0,5064 |
| 333 | 0,98324 | 0,4688 |
Obecność jasnofioletowego zabarwienia płomienia palnika podczas analiz chemicznych wskazuje na obecność w roztworze jonów
Na zamieszczonym schemacie biosensora literą A oznaczono
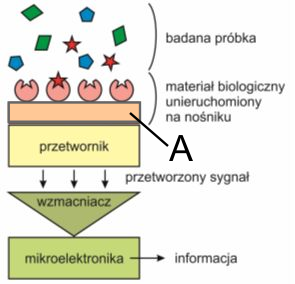
Z uwagi na niską zawartość żelaza w wodzie, najbardziej adekwatną metodą określania całkowitej ilości jonów żelaza(II) oraz (III) w próbkach wody pitnej jest
W naczyniu rozdzielającym umieszczono wodę oraz eter etylowy (d20 = 0,7138 g/cm3) i dokładnie je wymieszano.
Po chwili można zauważyć
Ile wynosi refrakcja molowa kwasu octowego o gęstości równej 1,0498 g/cm3, jeżeli współczynnik załamania światła wynosi 1,3874, a masa molowa kwasu octowego jest równa 60,054 g/mol?
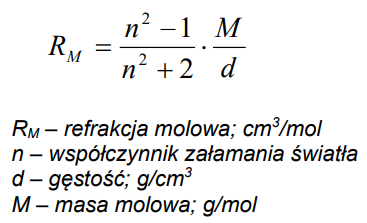
Podział anionów na grupy analityczne według Bunsena obejmuje ile grup?
Czym jest efekt wspólnego jonu?
Podłoże do izolacji i identyfikacji bakterii hemolizujących powinno zawierać
Lepkość dynamiczna wody
| Tabela. Gęstość (d) i lepkość dynamiczna wody (η) w danej temperaturze (T). | ||
| T [K] | d [g/cm3] | η [cP] |
| 293 | 0,99823 | 1,0050 |
| 298 | 0,99707 | 0,8937 |
| 303 | 0,99567 | 0,8007 |
| 308 | 0,99406 | 0,7225 |
| 313 | 0,99222 | 0,6560 |
| 318 | 0,99025 | 0,5988 |
| 323 | 0,98807 | 0,5494 |
| 328 | 0,98573 | 0,5064 |
| 333 | 0,98324 | 0,4688 |
Jakim odczynnikiem grupowym IV grupy analitycznej kationów jest?
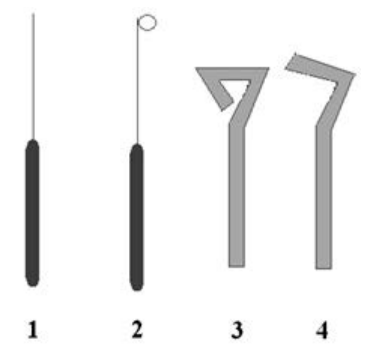
Schematyczny rysunek ezy, przyrządu używanego w laboratoriach mikrobiologicznych, został oznaczony na rysunku cyfrą
Reakcja, na której opiera się oznaczenie liczby zmydlania (LZ) tłuszczów, to
Jakie pH ma roztwór buforu węglanowego występującego we krwi, którego wartość wynosi 6,6, oraz jaki jest jego odczyn?
Wskaźnik zanieczyszczenia wody bakterią jelitową - miano coli równe 10 - oznacza, że
Na schemacie przedstawiającym sposób pobierania hodowli do badań ze skosu agarowego literą D oznaczono
Który z wskaźników wskazuje na zawartość minerałów w ściekach?
W zamieszczonej informacji przedstawiono równania reakcji zachodzące podczas oznaczania chlorków metodą
| Ag+ + Cl- → AgCl ↓ Ag+ + SCN- → AgSCN ↓ Fe3+ + SCN- → Fe(SCN)2+ |
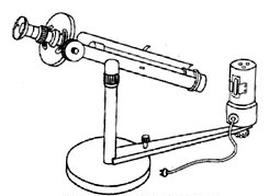
Na rysunku przedstawiono
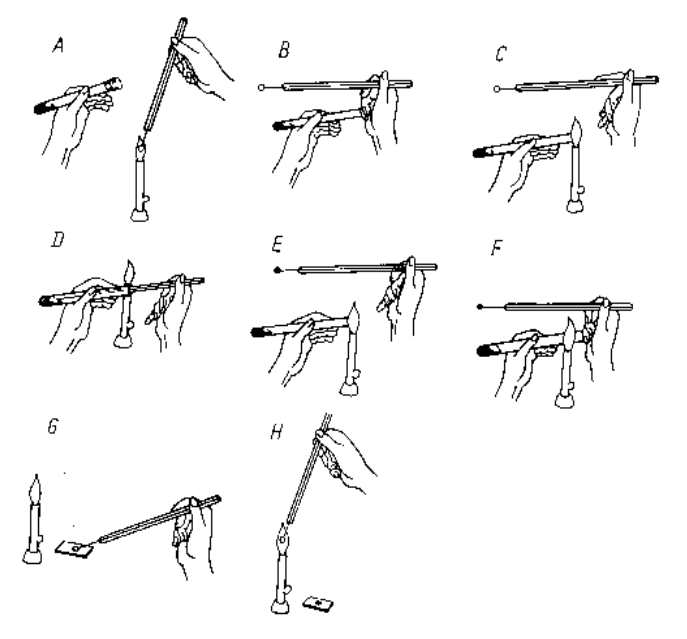
Jak należy ogrzewać probówkę z roztworem w trakcie wykrywania kationów II grupy analitycznej, gdy powstaje H2S?
Zjawisko alkalizacji gleby jest spowodowane
Odczynnikiem grupowym kationów IV grupy analitycznej jest
| A. | H2S w roztworze NH3(aq) i NH4Cl. |
| B. | roztwór HCl o stężeniu 2 mol/dm3. |
| C. | (NH4)2CO3 w roztworze NH3(aq) i NH4Cl. |
| D. | H2S w roztworze HCl o stężeniu 0,3 mol/dm3. |
Jaki wskaźnik jest używany do oceny kontaktu między wodami naturalnymi a fekaliami?