Pytanie 1
Przy transporcie próbek wody zaleca się, aby próbki były
Wynik: 35/40 punktów (87,5%)
Wymagane minimum: 20 punktów (50%)
Przy transporcie próbek wody zaleca się, aby próbki były
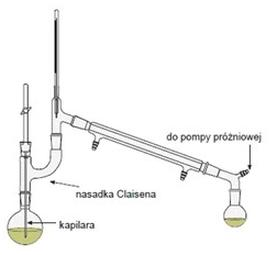
Przedstawiony na rysunku zestaw służy do destylacji
Zamieszczony piktogram odnosi się do substancji o klasie i kategorii zagrożenia:
Korzystając z danych w tabeli wskaż, ile cm3 36% roztworu HCl należy użyć, aby przygotować 250 cm3 0,1-molowego roztworu tego kwasu.
| % wagowy [%] | d420 [g/cm3] | m HCl w 100 cm3 [g/100cm3] | CM HCl [mol/dm3] |
|---|---|---|---|
| 30 | 1,1492 | 34,48 | 9,46 |
| 32 | 1,1593 | 37,10 | 10,17 |
| 34 | 1,1691 | 39,75 | 10,90 |
| 36 | 1,1789 | 42,44 | 11,64 |
Roztwór, który jest dodawany z biurety w formie kropli do roztworu substancji, którą analizujemy, określamy mianem
Sączenie osadów kłaczkowatych odbywa się przy użyciu sączków
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Aby uzyskać roztwór CuSO4 o stężeniu 15%, w jakim stosunku należy połączyć roztwory 10% oraz 20%?
Jaką metodą nie można rozdzielać mieszanin?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Wykorzystując pipetę gazową, pobrano próbkę azotu (Mn2 = 28 g/mol) o objętości 250 cm3 w standardowych warunkach. Jaką masę ma zmierzony azot?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Wskaź sprzęt laboratoryjny, który znajduje się w zestawie do filtracji pod obniżonym ciśnieniem?
Po połączeniu 50 cm3 wody z 50 cm3 alkoholu etylowego, objętość otrzymanej mieszanki jest poniżej 100 cm3. Zjawisko to jest spowodowane
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Wszystkie pojemniki z odpadami, zarówno stałymi, jak i ciekłymi, które są przekazywane do służby zajmującej się utylizacją, powinny być opatrzone informacjami
Aby rozpuścić próbkę tłuszczu o wadze 5 g, wykorzystuje się 50 cm3 mieszanki 96% alkoholu etylowego oraz eteru dietylowego, połączonych w proporcji objętościowej 1 : 2. Jakie ilości cm3 każdego ze składników są potrzebne do przygotowania 150 cm3 tej mieszanki?
Próbkę uzyskaną z próbki ogólnej poprzez jej zmniejszenie nazywa się
Wagi laboratoryjne można klasyfikować według nośności oraz precyzji na
Do 200 g roztworu NaOH (M = 40 g/mol) o stężeniu 10 % dodano wodę destylowaną w kolbie miarowej o pojemności 500 cm3 do znaku. Jakie jest stężenie molowe powstałego roztworu?
Na etykiecie kwasu siarkowego(VI) znajduje się zapis:
Określ gęstość kwasu siarkowego(VI).
KWAS SIARKOWY MIN. 95% CZ.D.A. H2SO4 M = 98,08 g/mol 1 l – 1,84 kg |
Aby przygotować 500 g roztworu o stężeniu 10% (m/m), ile substancji należy odważyć?
Na podstawie zmierzonej temperatury topnienia można określić związek organiczny oraz ustalić jego
Ekstrakcję w trybie ciągłym przeprowadza się
Jakie proporcje objętościowe powinny być zastosowane do zmieszania roztworu etanolu o stężeniu 30% (V/V) z roztworem o stężeniu 70% (V/V), aby uzyskać roztwór o stężeniu 50% (V/V)?
Piktogramem przedstawionym na rysunku znakuje się opakowanie substancji

Zgodnie z danymi zawartymi w tabeli wskaźników roztwór obojętny będzie miał barwę
| Wskaźnik | Zakres zmiany barwy (w jednostkach pH) | Barwa w środowisku | |
|---|---|---|---|
| kwaśnym | zasadowym | ||
| błękit tymolowy | 1,2 – 2,8 | czerwona | żółta |
| oranż metylowy | 3,1 – 4,4 | czerwona | żółta |
| czerwień metylowa | 4,8 – 6,0 | czerwona | żółta |
| czerwień chlorofenolowa | 5,2 – 6,8 | żółta | czerwona |
| błękit bromotymolowy | 6,0 – 7,6 | żółta | niebieska |
| czerwień fenolowa | 6,6 – 8,0 | żółta | czerwona |
| błękit tymolowy | 8,0 – 9,6 | żółta | niebieska |
| fenoloftaleina | 8,2 – 10,0 | bezbarwna | czerwona |
| żółcień alizarynowa | 10,1 – 12,0 | żółta | zielona |
Przedstawiony na rysunku sprzęt służy do

Reagent, który reaguje wyłącznie z jednym konkretnym jonem lub związkiem, nazywamy reagente
Przedstawiony schemat ideowy ilustruje proces syntezy z propanu C3H8 → C3H7Cl → C3H6 → C3H6(OH)2 → C3H5(OH)2Cl → C3H5(OH)3
Z etykiety wynika, że dany związek mógł być

W celu rozdrabniania niewielkich ilości bardzo twardego materiału wykorzystuje się moździerze
Aby przeprowadzić analizę jakościową, próbkę mosiądzu należy roztworzyć w stężonym kwasie
Jakie jest stężenie procentowe roztworu HCl (M=36,46 g/mol) o gęstości 1,19 g/cm3 oraz stężeniu molowym 12 mol/dm3?
W celu wydania świadectwa kontroli jakości odczynnika chemicznego - jodku potasu cz.d.a. przeprowadzono jego analizę. Wymagania oraz wyniki badań zapisano w tabeli:
Z analizy danych zawartych w tabeli wynika, że jodek potasu cz.d.a.
| Wymagania | Wynik badania | |
|---|---|---|
| Zawartość KI | min. 99,5% | 99,65% |
| Wilgoć | max. 0,1% | 0,075% |
| Substancje nierozpuszczalne w wodzie | max. 0,005% | 0,002% |
| pH (5%, H2O) | 6 ÷ 8 | 6,8 |
| Azot ogólny (N) | max. 0,001% | 0,0007% |
| Chlorki i bromki (j. Cl) | max. 0,01% | 0,004% |
| Fosforany (PO4) | max. 0,001% | 0,0006% |
| Jodany (IO3) | max. 0,0003% | 0,0001% |
| Siarczany (SO4) | max. 0,001% | 0,0004% |
| Metale ciężkie (j. Pb) | max. 0,0005% | 0,00025% |
| Arsen (As) | max. 0,00001% | 0,000006% |
| Magnez (Mg) | max. 0,001% | 0,0004% |
| Sód (Na) | max. 0,05% | 0,015% |
| Wapń (Ca) | max. 0,001% | 0,0006% |
| Żelazo (Fe) | max. 0,0003% | 0,0003% |
Metodą, która nie służy do utrwalania próbek wody, jest
Wskaż metodę rozdzielenia układu, w którym fazą rozproszoną jest ciało stałe, a fazą rozpraszającą gaz.
| faza rozproszona | faza rozpraszająca | ||
|---|---|---|---|
| gaz | ciecz | ciało stałe | |
| gaz | - | piana | piana stała |
| ciecz | aerozol ciekły | emulsja | emulsja stała |
| ciało stałe | aerozol stały | zol | zol stały |