Pytanie 1
W standardowym układzie destylacyjnym, który ma ukośną chłodnicę, wykorzystuje się chłodnicę
Wynik: 37/40 punktów (92,5%)
Wymagane minimum: 20 punktów (50%)
W standardowym układzie destylacyjnym, który ma ukośną chłodnicę, wykorzystuje się chłodnicę
Jakie jest przeznaczenie pieca muflowego?
Niemetal o kolorze fioletowoczarnym, który łatwo przechodzi w stan gazowy, to
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Do szklanych narzędzi laboratoryjnych wielomiarowych używanych w analizach ilościowych należy
Zjawisko fizyczne, które polega na rozkładaniu struktury krystalicznej substancji stałej oraz przenikaniu jej cząsteczek lub jonów do cieczy, nosi nazwę
Przykładem piany stałej jest
| faza rozproszona | faza rozpraszająca | ||
|---|---|---|---|
| gaz | ciecz | ciało stałe | |
| gaz | - | piana | piana stała |
| ciecz | aerozol ciekły | emulsja | emulsja stała |
| ciało stałe | aerozol stały | zol | zol stały |
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Który z poniższych sposobów homogenizacji próbki jest najbardziej odpowiedni do przygotowania próbki gleby do analizy chemicznej?
Wskaż metodę rozdzielenia układu, w którym fazą rozproszoną jest ciało stałe, a fazą rozpraszającą gaz.
| faza rozproszona | faza rozpraszająca | ||
|---|---|---|---|
| gaz | ciecz | ciało stałe | |
| gaz | - | piana | piana stała |
| ciecz | aerozol ciekły | emulsja | emulsja stała |
| ciało stałe | aerozol stały | zol | zol stały |
Aby podnieść stężenie mikroelementów w roztworze, próbkę należy poddać
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Naczynia miarowe, skalibrowane "na wlew" (IN) to:
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Jak przebiega procedura unieszkodliwiania rozlanego kwasu siarkowego(VI)?
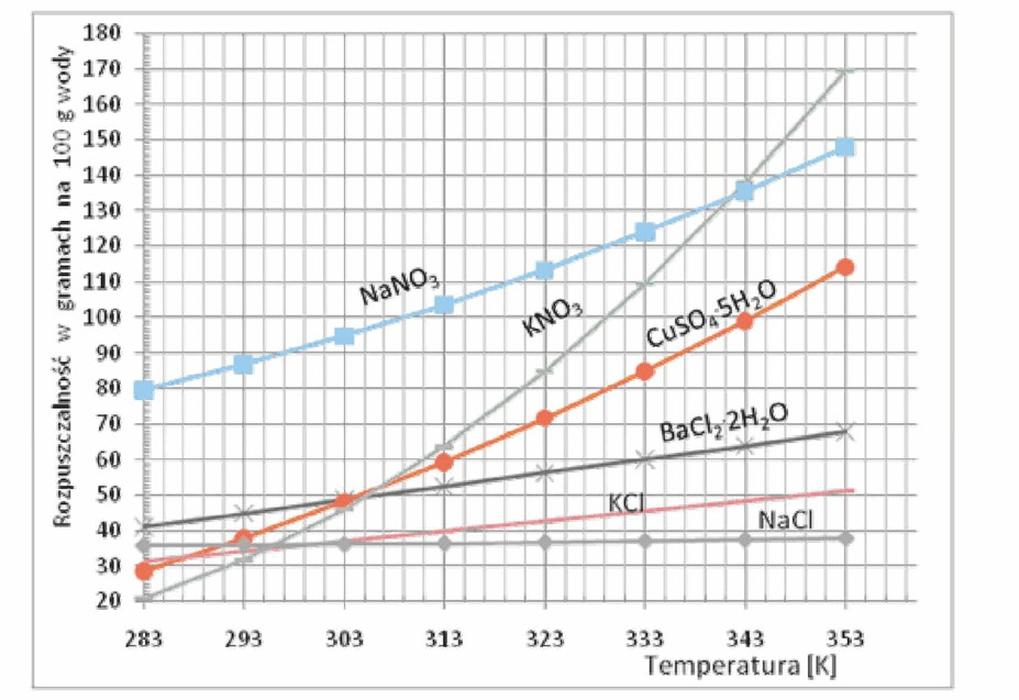
Korzystając z wykresu określ, w jakiej temperaturze należy rozpuszczać azotan(V) potasu, aby całkowicie rozpuścić 110 g soli w 100 g wody.
Na podstawie zamieszczonych informacji, wskaż ilości odczynników, które są niezbędne do przygotowania skali wzorców do kolorymetrycznego oznaczania rozpuszczalnych fosforanów(V).
| Przygotowanie skali wzorców do kolometrycznego oznaczania fosforanów(V) | ||||||||
| Do ośmiu cylindrów Nesslera o pojemności 100 cm3 odmierzyć kolejno wzorcowy roztwór roboczy KH2PO4 według poniższej tabeli SKALA WZORCÓW (PO43-) i uzupełnić wodą do kreski. Do każdego cylindra dodać 2 cm3 roztworu molibdenianu amonu (heksaamonoheptamolibdenian(VI)), wymieszać, dodać 0,2 cm3 roztworu SnCl2 i ponownie wymieszać. | ||||||||
| SKALA WZORCÓW (PO43-) | ||||||||
| Wzorcowy roztwór roboczy [cm3] | 0,0 | 0,5 | 1,0 | 2,0 | 3,0 | 5,0 | 7,0 | 10,0 |
| Zawartość PO43- [mg] | 0,0 | 0,005 | 0,01 | 0,02 | 0,03 | 0,05 | 0,07 | 0,10 |
| Roztwór | KH₂PO₄ | (NH₄)₆Mo₇O₂₄ | SnCl₂ |
|---|---|---|---|
| A. | 28,5 cm³ | 8,0 cm³ | 0,16 cm³ |
| B. | 0,285 cm³ | 16,0 cm³ | 1,6 cm³ |
| C. | 28,5 cm³ | 16,0 cm³ | 1,6 cm³ |
| D. | 0,285 cm³ | 8,0 cm³ | 16 cm³ |
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Aby otrzymać 200 g roztworu siarczanu(VI) sodu o stężeniu 12%, należy wykorzystać
(Na – 23 g/mol; S – 32 g/mol; H – 1 g/mol; O – 16 g/mol)
Etykiety chemikaliów zawierają zwroty H, które informują o rodzaju zagrożenia. Cyfra "3" pojawiająca się po literze "H" w oznaczeniu, definiuje rodzaj zagrożenia?
Na etykietach substancji chemicznych można znaleźć oznaczenia literowe R i S (zgodnie z regulacjami CLP: H i P), które wskazują
Co oznacza skrót AKT?
Eliminacja substancji organicznych z próbki poprzez jej spalenie nazywa się
Gęstość cieczy w próbce określa się bezpośrednio za pomocą
Do 200 g roztworu NaOH (M = 40 g/mol) o stężeniu 10 % dodano wodę destylowaną w kolbie miarowej o pojemności 500 cm3 do znaku. Jakie jest stężenie molowe powstałego roztworu?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Jaki jest błąd względny pomiaru na wadze o precyzji 0,1 g dla próbki o wadze 1 g?
W laboratorium chemicznym systemy wodne zazwyczaj oznacza się kolorem zielonym
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Z podanych w tabeli danych wybierz sprzęt potrzebny do zmontowania zestawu do destylacji z parą wodną.
| 1 | 2 | 3 | 4 | 5 |
| manometr | kociołek miedziany | chłodnica powietrzna | kolba destylacyjna | odbieralnik |
Na ilustracji przedstawiono sprzęt stosowany do sączenia osadu
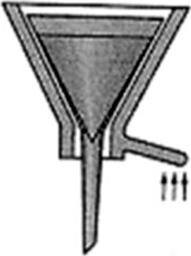
Na zdjęciu przedstawiono proces

Z uwagi na higroskopijne właściwości tlenku fosforu(V) powinien on być przechowywany w warunkach bez dostępu
Odlanie cieczy z nad osadu to
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Zamieszczony piktogram odnosi się do substancji o klasie i kategorii zagrożenia:
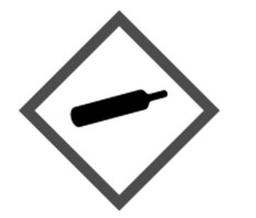
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.