Pytanie 1
Aby przygotować zestaw do filtracji, należy zebrać
Wynik: 38/40 punktów (95,0%)
Wymagane minimum: 20 punktów (50%)
Aby przygotować zestaw do filtracji, należy zebrać
W trakcie destylacji cieczy wykorzystuje się tzw. kamienie wrzenne, ponieważ
Który z etapów przygotowania próbek do analizy opisano w ramce?
| Proces polegający na usuwaniu wody z zamrożonego materiału na drodze sublimacji lodu, tzn. bezpośredniego jego przejścia w stan pary z pominięciem stanu ciekłego. |
Wskaż, do jakiego typu należą zamieszczone równania reakcji.
| I. 2 Mg + O2 → 2 MgO |
| II. 2 KMnO4 → K2MnO4 + MnO2 + O2 |
| III. BaCl2 + H2SO4→ BaSO4 + 2 HCl |
W standardowym układzie destylacyjnym, który ma ukośną chłodnicę, wykorzystuje się chłodnicę
W procesie oddzielania osadu od roztworu, po przeniesieniu osadu na sączek, najpierw należy go
Który z poniższych sposobów homogenizacji próbki jest najbardziej odpowiedni do przygotowania próbki gleby do analizy chemicznej?
Rozdział składników mieszaniny w chromatografii odbywa się dzięki ich różnym
Próbki wody, które mają być badane pod kątem zawartości krzemu, powinny być przechowywane w pojemnikach
Wskaź sprzęt laboratoryjny, który znajduje się w zestawie do filtracji pod obniżonym ciśnieniem?
Aparat przedstawiony na ilustracji służy do

W karcie charakterystyki chemikaliów znajduje się informacja o przechowywaniu dichromianu(VI) potasu: .. powinien być przechowywany w odpowiednio oznakowanych, szczelnie zamkniętych pojemnikach, w chłodnym, suchym i dobrze wentylowanym magazynie, który posiada instalację elektryczną i wentylacyjną. Z tego opisu wynika, że ten chemikal może być przechowywany
Na rysunku przedstawiono przyrząd do pobierania próbek

Którego związku chemicznego, z uwagi na jego silne właściwości higroskopijne, nie powinno się używać w analizie miareczkowej jako substancji podstawowej?
Które z wymienionych reakcji chemicznych stanowi reakcję redoks?
Z uwagi na higroskopijne właściwości tlenku fosforu(V) powinien on być przechowywany w warunkach bez dostępu
W celu rozdrabniania niewielkich ilości bardzo twardego materiału wykorzystuje się moździerze
Podczas przewozu próbek wody, które mają być badane pod kątem właściwości fizykochemicznych, zaleca się, aby te próbki były
Jaka minimalna pojemność powinna mieć miarka, aby jednorazowo zmierzyć 60,0 cm3 wody?
Wody pobrane ze studni powinny być przewożone w szczelnie zamkniętych butelkach z przezroczystego materiału
Do przechowywania zamrożonych próbek wody stosuje się naczynia wykonane
Reagenty o najwyższej czystości to reagenty
Aby przyspieszyć reakcję, należy zwiększyć stężenie substratów
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
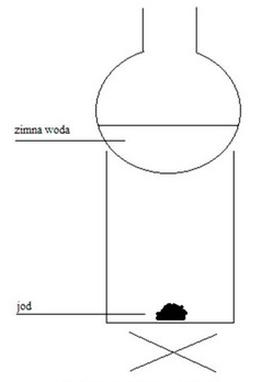
Na rysunku przedstawiono zestaw do oczyszczania jodu w procesie
W celu wydania świadectwa kontroli jakości odczynnika chemicznego - jodku potasu cz.d.a. przeprowadzono jego analizę. Wymagania oraz wyniki badań zapisano w tabeli:
Z analizy danych zawartych w tabeli wynika, że jodek potasu cz.d.a.
| Wymagania | Wynik badania | |
|---|---|---|
| Zawartość KI | min. 99,5% | 99,65% |
| Wilgoć | max. 0,1% | 0,075% |
| Substancje nierozpuszczalne w wodzie | max. 0,005% | 0,002% |
| pH (5%, H2O) | 6 ÷ 8 | 6,8 |
| Azot ogólny (N) | max. 0,001% | 0,0007% |
| Chlorki i bromki (j. Cl) | max. 0,01% | 0,004% |
| Fosforany (PO4) | max. 0,001% | 0,0006% |
| Jodany (IO3) | max. 0,0003% | 0,0001% |
| Siarczany (SO4) | max. 0,001% | 0,0004% |
| Metale ciężkie (j. Pb) | max. 0,0005% | 0,00025% |
| Arsen (As) | max. 0,00001% | 0,000006% |
| Magnez (Mg) | max. 0,001% | 0,0004% |
| Sód (Na) | max. 0,05% | 0,015% |
| Wapń (Ca) | max. 0,001% | 0,0006% |
| Żelazo (Fe) | max. 0,0003% | 0,0003% |
Aby wykonać chromatografię cienkowarstwową, należy przygotować eluent składający się z toluenu, acetonu oraz kwasu mrówkowego w proporcjach objętościowych 10:4:1. Jakie ilości poszczególnych składników powinny być wykorzystane do uzyskania 300 cm3 eluentu?
Jakie urządzenie jest wykorzystywane do oczyszczania próbki gazowej?
Na podstawie informacji zawartych w tabeli określ, który parametr spośród podanych należy oznaczyć w pierwszej kolejności.
| Tabela. Sposoby utrwalania próbek wody i ścieków, miejsce analizy, dopuszczalny czas przechowywania próbek | ||||
|---|---|---|---|---|
| Oznaczany parametr | Rodzaj naczynia do przechowywania próbki | Sposób utrwalania próbki | Miejsce wykonania analizy | Dopuszczalny czas przechowywania próbki |
| Chlorki | szklane lub polietylenowe | - | laboratorium | 96 godzin |
| Chlor pozostały | szklane | - | w miejscu pobrania próbki | - |
| ChZT | szklane | zakwaszenie do pH<2, schłodzenie do temperatury 2-5°C | laboratorium | 24 godziny |
| Kwasowość | szklane lub polietylenowe | schłodzenie do temperatury 2-5°C | laboratorium | 4 godziny |
| Mangan | szklane lub polietylenowe | zakwaszenie do pH<2, schłodzenie do temperatury 2-5°C | laboratorium | 48 godziny |
Jakiego koloru nabierze lakmus w roztworze NaOH?
Odważka analityczna wodorotlenku sodu, przygotowana fabrycznie, zawiera 0,1 mola NaOH. Jaką objętość wody destylowanej należy dodać w kolbie miarowej, aby uzyskać roztwór wodorotlenku sodu o stężeniu 0,0500 mol/dm3?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Podczas łączenia bezwodnego etanolu z wodą występuje zjawisko kontrakcji. Gdy zmieszamy 1000 cm3 wody oraz 1000 cm3 etanolu, otrzymujemy roztwór o objętości
Aby uzyskać Cr2O3, dichromian(VI) amonu został poddany rozkładowi. Po rozpoczęciu, egzotermiczna reakcja rozkładu przebiega samorzutnie.
(NH4)2Cr2O7 → Cr2O3 + 4 H2O + N2 Jak oceniasz zakończenie tej reakcji?
Ustalanie miana roztworu polega na
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Pobieranie próbek wody z zbiornika wodnego, który zasila system wodociągowy, powinno odbywać się
Na podstawie danych w tabeli wskaż, którego środka suszącego można użyć do osuszenia związku o wzorze (CH3)2CO
| Środek suszący | Stosowany do suszenia | Nie nadaje się do suszenia |
|---|---|---|
| Na | Eter, węglowodory, aminy trzeciorzędowe | Chlorowcopochodne węglowodorów |
| CaCl₂ | Węglowodory, aceton, eter, gazy obojętne | Alkohole, amoniak, aminy |
| Żel krzemionkowy | W eksykatorze | HF |
| H₂SO₄ | Gazy obojętne i kwasowe | Związki nienasycone, alkohole, substancje zasadowe |
Procedura oznaczenia kwasowości mleka. Do wykonania analizy, zgodnie z powyższą procedurą, potrzebne są
| Do kolby stożkowej o pojemności 300 cm3 pobrać dokładnie 25 cm3 badanego mleka i rozcieńczyć wodą destylowaną do objętości 50 cm3. Dodać 2-3 krople fenoloftaleiny i miareczkować mianowanym roztworem wodorotlenku sodu do uzyskania lekko różowego zabarwienia. |