Pytanie 1
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Wynik: 37/40 punktów (92,5%)
Wymagane minimum: 20 punktów (50%)
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Zamieszczony fragment procedury opisuje sposób otrzymywania
| „W zlewce o pojemności 250 cm3 rozpuść w 50 cm3 wody destylowanej 5 g uwodnionego siarczanu(VI) miedzi(II). Do roztworu dodaj 16,7 cm3 roztworu NaOH o stężeniu 6 mol/dm3. Następnie dodaj 10 g glukozy w celu przeprowadzenia reakcji redukcji jonów miedzi(II) do miedzi(I). Ostrożnie ogrzewaj zlewkę z mieszaniną reakcyjną do otrzymania czerwonego osadu (...)Osad odsącz, przemyj alkoholem i susz na bibule na powietrzu." |
Substancje kancerogenne to
Wskaż, do jakiego typu należą zamieszczone równania reakcji.
| I. 2 Mg + O2 → 2 MgO |
| II. 2 KMnO4 → K2MnO4 + MnO2 + O2 |
| III. BaCl2 + H2SO4→ BaSO4 + 2 HCl |
Wskaż jaka zawartość chlorków w próbce wody pozwala na wykorzystanie tej wody do produkcji betonu zgodnie z normą PN-EN 1008.
| Wymagania dotyczące zawartości chlorków w wodzie do produkcji betonu według normy PN-EN 1008 | |
| substancja | dopuszczalna wartość w mg/dm3 |
| chlorki | 1000 |
Laboratoryjny aparat szklany, który wykorzystuje kwasy do wytwarzania gazów w reakcji z metalem lub odpowiednią solą, to
Odczynnik, który w specyficznych warunkach reaguje wyłącznie z danym jonem, umożliwiając tym samym jego identyfikację w mieszance, to odczynnik
Zdjęcie przedstawia palnik

Czystość konkretnego odczynnika chemicznego wynosi: 99,9-99,99%. Jakiego rodzaju jest ten odczynnik?
Na podstawie danych zawartych w tabeli określ, do oznaczania którego parametru próbka musi być utrwalona w niskim pH.
| Oznaczany parametr | Rodzaj naczynia do przechowywania | Sposób utrwalania | Dopuszczalny czas przechowywania |
|---|---|---|---|
| barwa | szklane lub polietylenowe | - schłodzenie do temperatury 2-5°C | 24 h |
| fosforany ogólne | szklane lub polietylenowe | - zakwaszenie kwasem siarkowym(VI) - schłodzenie do temperatury 2-5°C | 4 h 48 h |
| BZT | szklane | - schłodzenie do temperatury 2-5°C - przechowywanie w ciemności | 24 h |
| azot azotanowy(V) | szklane lub polietylenowe | - schłodzenie do temperatury 2-5°C - dodanie 2 cm3 chloroformu do 1 dm3 próbki | 24 h 48 h |
Skalę wzorców do oznaczenia barwy przygotowano w cylindrach Nesslera o pojemności 100 cm3. Barwa oznaczona w tabeli jako X wynosi
| Skala wzorców do barwy | ||||
|---|---|---|---|---|
| Ilość wzorcowego roztworu podstawowego cm3 (c=500 mg Pt/dm3) | 0 | 1,0 | 2,0 | 3,0 |
| Barwa w stopniach mg Pt/dm3 | 0 | 5 | X | 15 |
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
W jakiej standardowej temperaturze są kalibrowane szklane naczynia pomiarowe?
Podczas reakcji chlorku żelaza(III) z wodorotlenkiem potasu dochodzi do wytrącenia wodorotlenku żelaza(III) w formie
Którego związku chemicznego, z uwagi na jego silne właściwości higroskopijne, nie powinno się używać w analizie miareczkowej jako substancji podstawowej?
Z przedstawionego opisu wynika, że kluczową właściwością próbki analitycznej jest jej
Próbka analityczna to fragment materiału stworzony z myślą o przeprowadzeniu badania lub obserwacji. Powinna odzwierciedlać przeciętny skład i cechy materiału, który jest badany.
Który z poniższych zestawów obejmuje jedynie sprzęt do pomiarów?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Na podstawie informacji zawartej na pipecie, została ona skalibrowana na
Kalibracja pH-metru nie jest potrzebna po
Po zmieszaniu wszystkie pierwotne próbki danej partii materiału tworzą próbkę
Na rysunku przedstawiającym płomień palnika gazowego najwyższa temperatura płomienia znajduje się w strefie
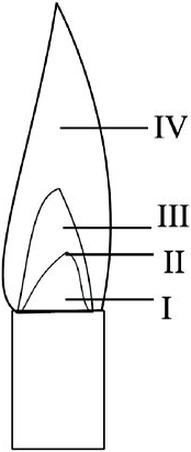
Na podstawie zmierzonej temperatury topnienia można określić związek organiczny oraz ustalić jego
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Jakim przyrządem nie jest możliwe określenie gęstości cieczy?
Które z wymienionych reakcji chemicznych stanowi reakcję redoks?
W trzech probówkach umieszczono roztwory: wodorotlenku sodu, chlorku sodu i kwasu octowego. W celu identyfikacji zbadano ich odczyn za pomocą uniwersalnego papierka wskaźnikowego, a następnie fenoloftaleiny. Barwy wskaźników w badanych roztworach przedstawiono w tabeli:
| Wskaźnik | Barwa wskaźnika | ||
|---|---|---|---|
| próbówka nr 1 | próbówka nr 2 | próbówka nr 3 | |
| uniwersalny papierek wskaźnikowy | żółty | czerwony | niebieski |
| fenoloftaleina | bezbarwny | bezbarwny | malinowa |
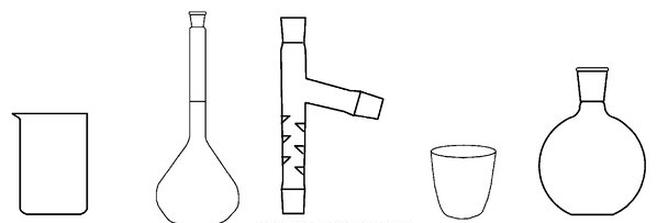
Wybierz zestaw, w którym znajdują się wyłącznie nazwy sprzętu laboratoryjnego pokazanego na rysunkach.
Jakie procedury powinny być stosowane podczas ustalania miana roztworu?
Który z wymienionych roztworów NaOH, o określonych stężeniach, nie jest roztworem mianowanym?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Który z wskaźników nie jest używany w alkacymetrii?
Temperatura wrzenia aniliny przy normalnym ciśnieniu wynosi 457,13 K. W trakcie jej oczyszczania metodą destylacji prostej pod ciśnieniem atmosferycznym należy zebrać frakcję wrzącą w przedziale temperatur
Które z poniższych równań ilustruje reakcję, w której powstają produkty gazowe?
Jakie pH ma roztwór buforowy otrzymany w wyniku zmieszania 0,2 M roztworu kwasu octowego i 0,2 M roztworu octanu sodu, w stosunku objętościowym 3 : 2?
| Bufor octanowy według Walpole'a | ||
|---|---|---|
| 0,2 M kwas octowy [ml] | 0,2 M octan sodu [ml] | pH |
| 7,0 | 3,0 | 4,39 |
| 6,0 | 4,0 | 4,58 |
| 5,0 | 5,0 | 4,75 |
| 4,0 | 6,0 | 4,94 |
| 3,0 | 7,0 | 5,13 |
Jakie substancje wykorzystuje się do wykrywania obecności jonów chlorkowych w wodzie mineralnej?
Jaką substancję wskaźnikową należy zastosować do ustalenia miana roztworu wodorotlenku sodu w reakcji z kwasem solnym, według przedstawionej procedury, która polega na odmierzeniu 25 cm3 roztworu HCl o stężeniu 0,20 mol/dm3 do kolby stożkowej, dodaniu 50 cm3 wody destylowanej, 2 kropli wskaźnika oraz miareczkowaniu roztworem NaOH do momentu zmiany koloru z czerwonego na żółty?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Na podstawie danych w tabeli określ, dla oznaczania którego parametru zalecaną metodą jest chromatografia jonowa.
| Parametr | Metoda podstawowa |
|---|---|
| pH | metoda potencjometryczna, kalibracja przy zastosowaniu minimum dwóch wzorców o pH zależnym od wartości oczekiwanych w próbkach wody |
| azotany(V) | chromatografia jonowa |
| fosforany(V) | spektrofotometria |
| Na, K, Ca, Mg | AAS (spektrometria absorpcji atomowej) |
| zasadowość | miareczkowanie wobec fenoloftaleiny oraz oranżu metylowego |
| tlen rozpuszczony, BZT₅ | metoda potencjometryczna |