Pytanie 1
Jakie symbole mają odprowadzenia kończynowe dwubiegunowe w badaniu EKG?
Wynik: 29/40 punktów (72,5%)
Wymagane minimum: 20 punktów (50%)
Jakie symbole mają odprowadzenia kończynowe dwubiegunowe w badaniu EKG?
Podczas badania EEG otwarcie oczu powoduje
Wskazaniem do wykonania badania spirometrycznego jest
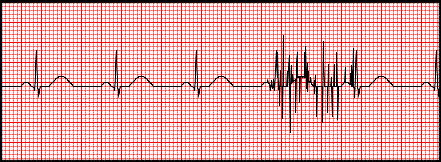
W przypadku migotania komór w zapisie EKG występuje
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
Do prób aktywacyjnych stosowanych w badaniu EEG zalicza się
W standardowym badaniu elektrokardiologicznym elektrodę C4 należy umocować
Odprowadzenie EKG mierzące różnicę potencjałów między lewym podudziem a prawym przedramieniem oznacza się jako
Który elektrokardiogram jest poprawny technicznie?
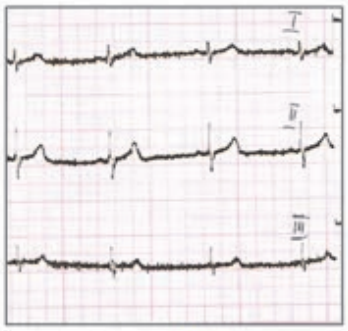
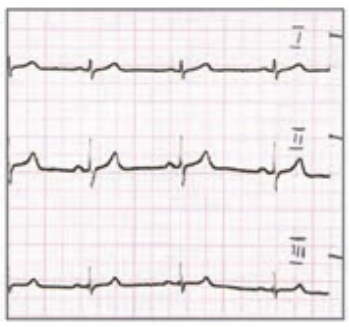
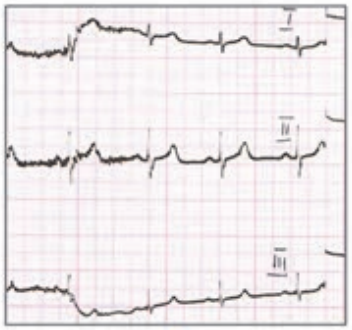
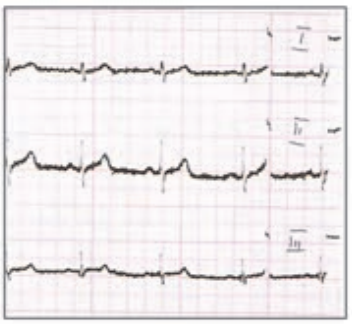
Które odprowadzenie w badaniu EKG rejestruje różnice potencjałów pomiędzy lewym a prawym przedramieniem?
Podczas badania EEG w systemie „10-20” literą A oznacza się elektrody
W badaniu EEG elektrody referencyjne przymocowane do płatka ucha to
W badaniu EKG różnice potencjałów pomiędzy lewym podudziem a lewym przedramieniem rejestruje odprowadzenie
Jednym z kryteriów poprawnie wykonanego badania spirometrycznego jest czas trwania natężonego wydechu, który powinien wynosić u osób powyżej 10 roku życia co najmniej
Zarejestrowane na elektrokardiogramie miarowe fale f w kształcie „zębów piły” poprzedzielane prawidłowymi zespołami QRS są charakterystyczne dla
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
Fotostymulacja wykonywana jest podczas badania
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
Audiogram przedstawia próbę
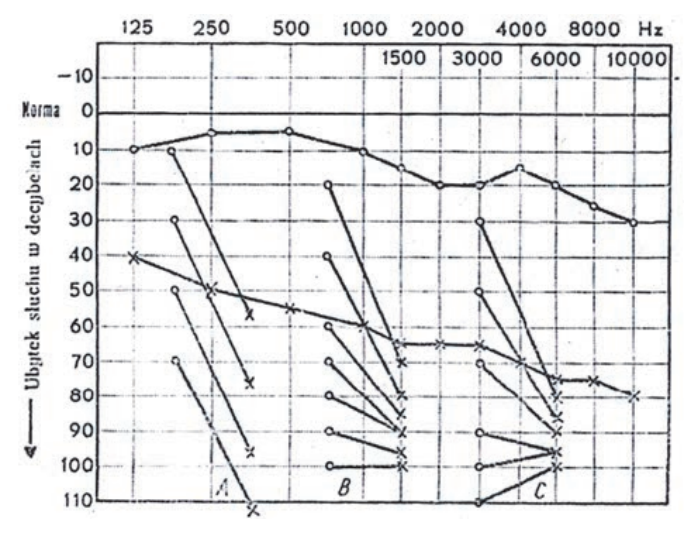
Fala głosowa rozchodzi się
Na elektrokardiogramie zarejestrowano
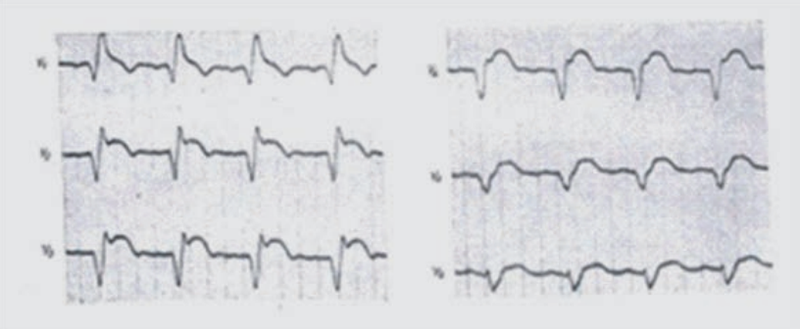
Obiektywną metodą badania słuchu jest audiometria
W badaniu audiometrycznym rezerwa ślimakowa to odległość między krzywą
Gdzie znajduje się węzeł zatokowo-przedsionkowy wywołujący rytmiczne skurcze mięśnia serca?
Który system informatyczny jest wykorzystywany do archiwizowania i przesyłania obrazów na stacje diagnostyczne w standardzie DICOM?
Który załamek odzwierciedla szybką repolaryzację komór w zapisie EKG?
W którym miejscu, zgodnie z zasadami wykonywania badania EKG, należy umocować żółtą elektrodę przedsercową V2?
Podczas wykonywania badania EEG elektrodę P4 umieszcza się w okolicy
Na elektrokardiogramie uwidoczniono
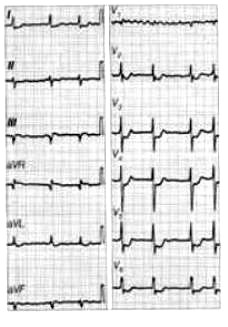
W audiometrii badanie polegające na maskowaniu (zagłuszaniu) tonów szumem białym to próba
Rytm alfa i beta rejestruje się podczas badania
Za wyrównanie ciśnienia między uchem środkowym a otoczeniem odpowiada
Jednym z kryteriów poprawnie wykonanego badania spirometrycznego jest czas trwania natężonego wydechu, który powinien wynosić u osób powyżej 10 roku życia co najmniej
Na podstawie zapisu badania audiometrycznego rozpoznano u pacjenta uszkodzenie słuchu
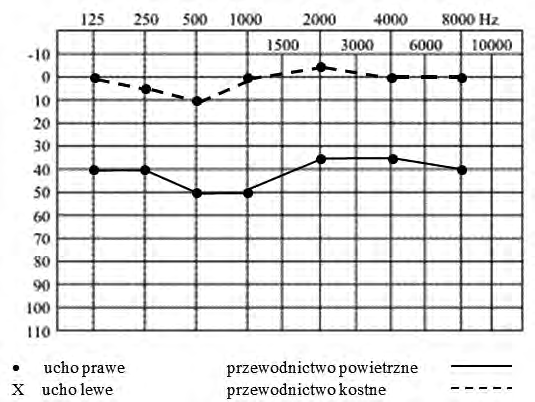
W badaniu EEG w systemie „10-20” elektrody w okolicy skroniowej oznaczone są literą
W jakich jednostkach mierzy się natężenie dźwięku?
Rytm alfa i beta rejestruje się podczas badania
Artefakty zarejestrowane na elektrokardiogramie zostały wywołane przez
Bezwzględnym przeciwwskazaniem do badania spirometrycznego jest
Wskazaniem do wykonania badania spirometrycznego jest