Pytanie 1
Zamieszczone na ilustracji obrazy dotyczą badania
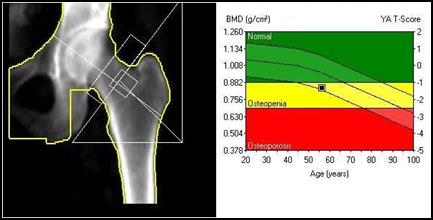
Wynik: 1/40 punktów (2,5%)
Wymagane minimum: 20 punktów (50%)
Zamieszczone na ilustracji obrazy dotyczą badania

Standardowe badanie USG średniej wielkości piersi wykonuje się głowicą w zakresie częstotliwości
Rutynowe badanie koronarografii prawej tętnicy wieńcowej wykonywane jest w rzucie skośnym przednim
Przy podejrzeniu ciała obcego w oczodole należy wykonać
Brak odpowiedzi na to pytanie.
W radiologii stomatologicznej ząb o numerze 23 to kieł
Brak odpowiedzi na to pytanie.
Na prawidłowo wykonanym zdjęciu zatok w projekcji PA górny zarys piramid rzutuje się
Brak odpowiedzi na to pytanie.
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
Brak odpowiedzi na to pytanie.
Audiometria impedancyjna polega na pomiarze
Brak odpowiedzi na to pytanie.
W leczeniu izotopowym tarczycy należy podać
Brak odpowiedzi na to pytanie.
W przedstawionym na ilustracji obrazie badania angiograficznego uwidoczniono
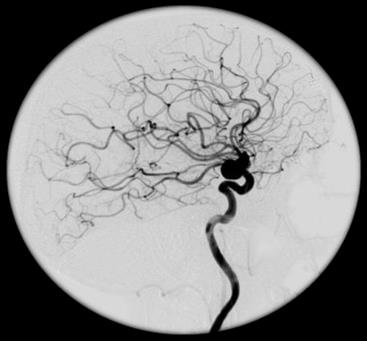
Brak odpowiedzi na to pytanie.
Który załamek w zapisie EKG odpowiada zjawisku depolaryzacji przedsionków mięśnia sercowego?
Brak odpowiedzi na to pytanie.
Zgodnie z procedurą wzorcową w badaniu MR należy ułożyć pacjenta na brzuchu do diagnostyki
Brak odpowiedzi na to pytanie.
Rak drobnokomórkowy i rak niedrobnokomórkowy to postacie organiczne nowotworów złośliwych
Brak odpowiedzi na to pytanie.
Zamieszczony elektrokardiogram przedstawia
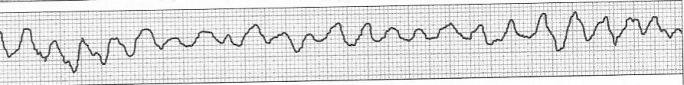
Brak odpowiedzi na to pytanie.
W celu oceny wieku kostnego u dziecka praworęcznego, wykonuje się pojedyncze zdjęcie w projekcji
Brak odpowiedzi na to pytanie.
Pozytywny środek cieniujący najczęściej stosowany w rentgenodiagnostyce powinien charakteryzować się
Brak odpowiedzi na to pytanie.
Który załamek odzwierciedla repolaryzację komór w zapisie EKG?
Brak odpowiedzi na to pytanie.
Dawka graniczna wyrażona jako dawka skuteczna (efektywna), dla osób zawodowo narażonych na działanie promieniowania jonizującego wynosi w ciągu roku kalendarzowego
Brak odpowiedzi na to pytanie.
Na rentgenogramie strzałką zaznaczono
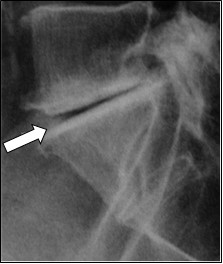
Brak odpowiedzi na to pytanie.
Który system informatyczny jest wykorzystywany do archiwizowania i przesyłania obrazów na stacje diagnostyczne w standardzie DICOM?
Brak odpowiedzi na to pytanie.
Na którym obrazie TK uwidoczniony jest artefakt spowodowany ruchami oddechowymi pacjenta?
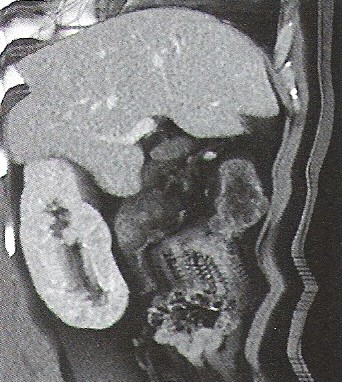
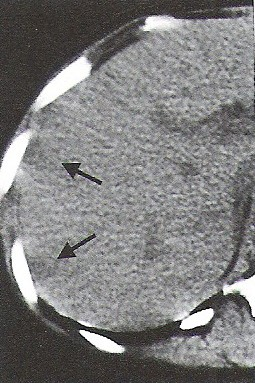

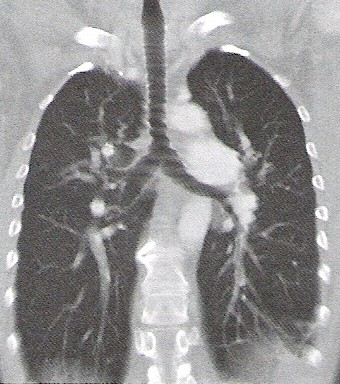
Brak odpowiedzi na to pytanie.
Gadolin jako dożylny środek kontrastowy stosowany w MR powoduje
Brak odpowiedzi na to pytanie.
W pracowni radioterapii wyświetlenie na ekranie monitora aparatu komunikatu „ROTATION” oznacza prowadzoną terapię
Brak odpowiedzi na to pytanie.
Jaka jest odległość pomiędzy źródłem promieniowania a powierzchnią ciała pacjenta w technice izocentrycznej radioterapii?
Brak odpowiedzi na to pytanie.
Na radiogramie uwidoczniono złamanie
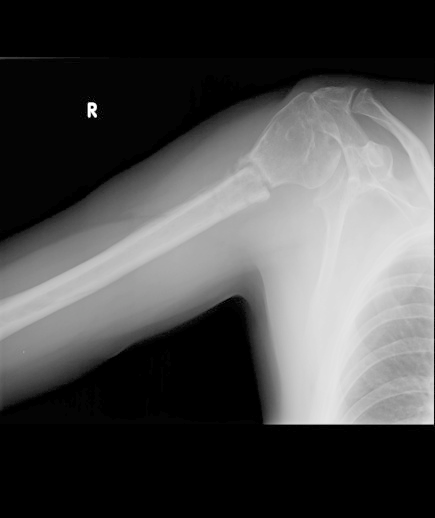
Brak odpowiedzi na to pytanie.
Na prawidłowo przedstawionym radiogramie badania kontrastowego strzałką zaznaczono
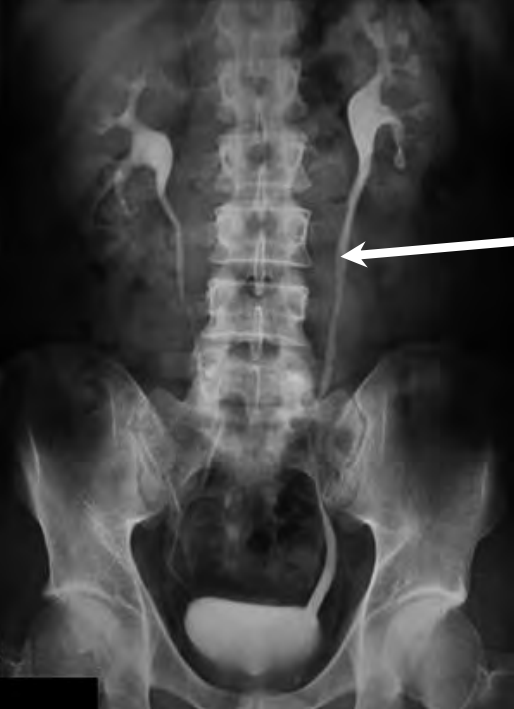
Brak odpowiedzi na to pytanie.
Do pomiaru dawek indywidualnych u osób narażonych zawodowo na promieniowanie rentgenowskie są stosowane
Brak odpowiedzi na to pytanie.
Do badania mammograficznego w projekcji skośnej przyśrodkowo-bocznej kąt lampy powinien być ustawiony w zakresie
Brak odpowiedzi na to pytanie.
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Brak odpowiedzi na to pytanie.
Zdjęcie którego zęba górnego zlecił na skierowaniu lekarz stomatolog?
Brak odpowiedzi na to pytanie.
Podczas teleradioterapii piersi lewej narządem krytycznym jest
Brak odpowiedzi na to pytanie.
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Brak odpowiedzi na to pytanie.
Hiperfrakcjonowanie dawki w radioterapii oznacza napromienienie pacjenta
Brak odpowiedzi na to pytanie.
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
Brak odpowiedzi na to pytanie.
Wskazaniem do wykonania badania spirometrycznego jest
Brak odpowiedzi na to pytanie.
Do środków kontrastujących negatywnych należą
Brak odpowiedzi na to pytanie.
Które zaburzenie rytmu serca zarejestrowano na elektrokardiogramie?
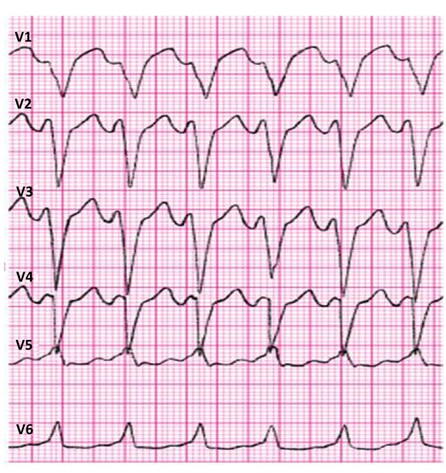
Brak odpowiedzi na to pytanie.
Na rentgenogramie przedstawione jest złamanie Saltera-Harrisa typu
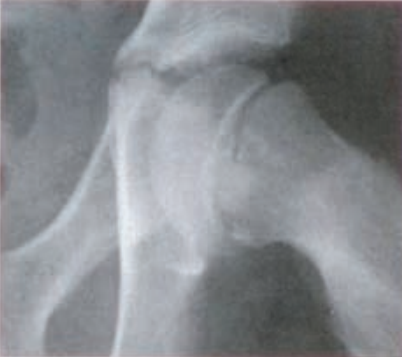
Brak odpowiedzi na to pytanie.
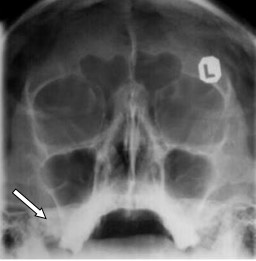
Na radiogramie czaszki strzałką zaznaczono
Brak odpowiedzi na to pytanie.
Pojawienie się w zapisie EKG patologicznego załamka Q lub QS może wskazywać na
Brak odpowiedzi na to pytanie.