Pytanie 1
Ligand stosuje się
Wynik: 37/40 punktów (92,5%)
Wymagane minimum: 20 punktów (50%)
Ligand stosuje się
Która sekwencja w obrazowaniu MR jest stosowana do uwidocznienia naczyń krwionośnych?
W radiologii stomatologicznej ząb o numerze 23 to kieł
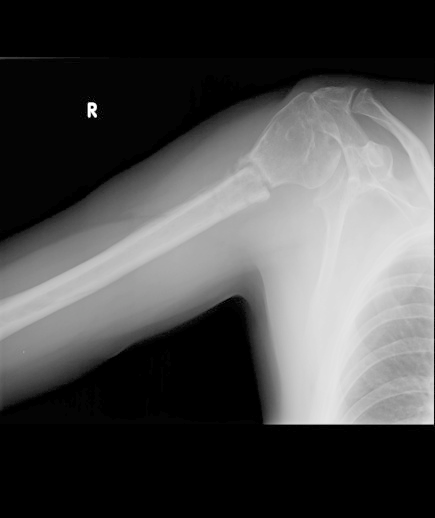
Jaki rozmiar kasety należy zastosować, wykonując standardowe zdjęcie stawu kolanowego w projekcji bocznej?
Jednym z kryteriów poprawnie wykonanego badania spirometrycznego jest czas trwania natężonego wydechu, który powinien wynosić u osób powyżej 10 roku życia co najmniej
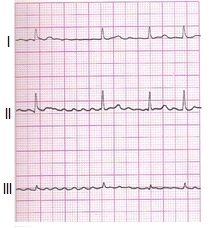
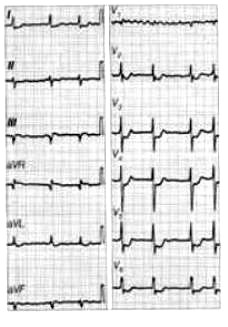
Zamieszczone badanie elektrokardiograficzne wykazało u pacjenta
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
W badaniu PET stosuje się tylko radioizotopy emitujące
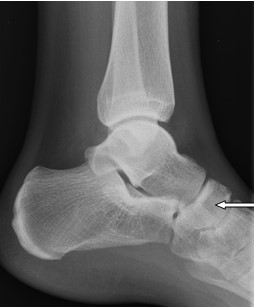
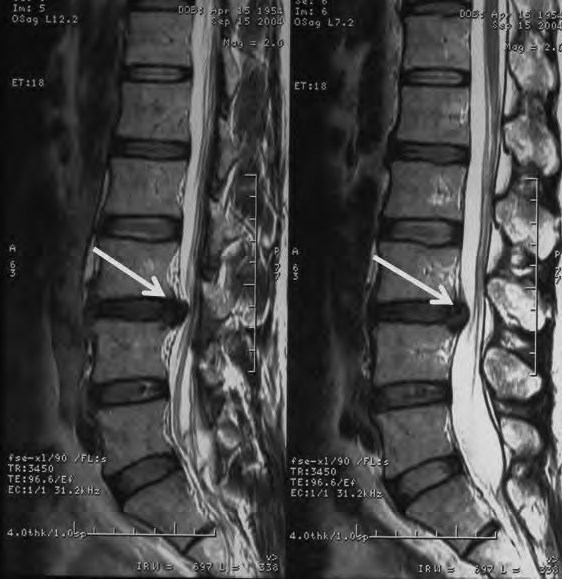
Na radiogramie strzałką oznaczono
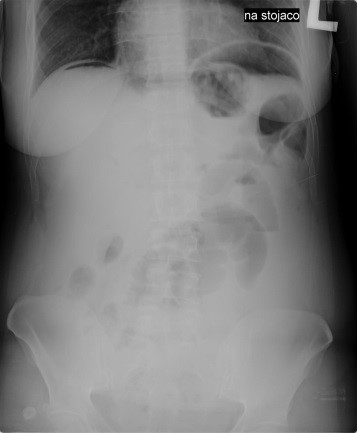
Radiogram jamy brzusznej uwidacznia
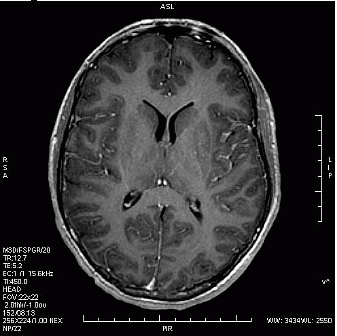
Który obraz MR mózgu został wykonany w sekwencji DWI?
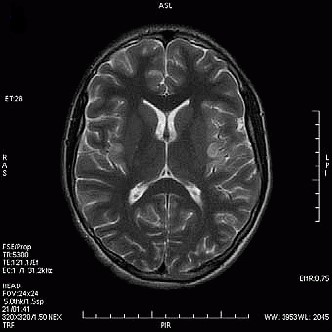
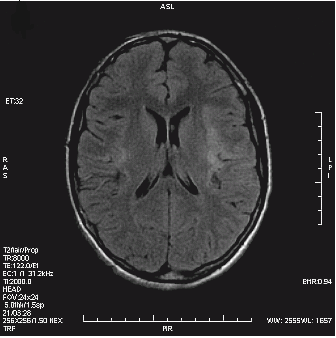
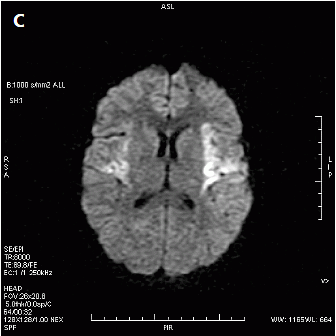
Badanie przewodu pokarmowego metodą podwójnego kontrastu wiąże się z podaniem pacjentowi
Zgodnie z procedurą wzorcową w badaniu MR należy ułożyć pacjenta na brzuchu do diagnostyki
Na rycinie rentgenogramu w projekcji AP symbolem X oznaczono
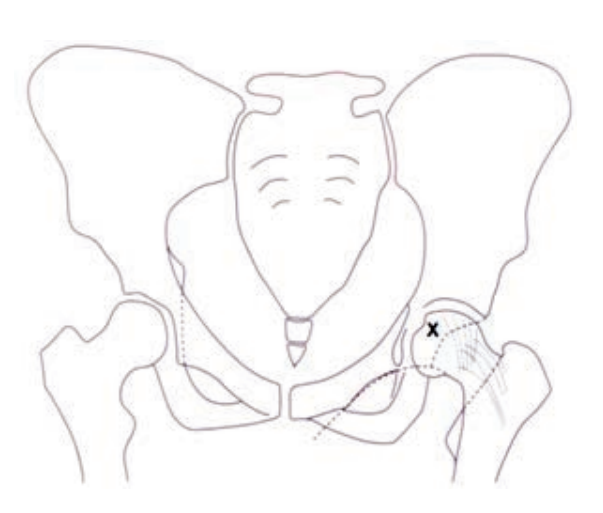
W systemie międzynarodowym ząb pierwszy przedtrzonowy po stronie lewej oznacza się symbolem
Głowica typu convex w USG służy do badania
W których projekcjach wykonuje się standardowe badanie mammograficzne?
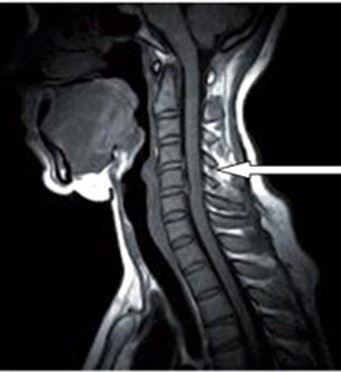
Na obrazie rezonansu magnetycznego strzałką oznaczono wyrostek kolczysty kręgu
Podczas wykonywania zdjęć wewnątrzustnych zębów górnych linia Campera powinna przebiegać w stosunku do płaszczyzny podłogi
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
W brachyterapii MDR stosowane są dawki promieniowania
Na radiogramie uwidoczniono złamanie
Na elektrokardiogramie uwidoczniono
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
W radioterapii konwencjonalnej pacjent jest leczony promieniowaniem pochodzącym
Na obrazie RM uwidoczniono odcinek kręgosłupa
Źródłem promieniowania protonowego stosowanego w radioterapii jest
Hiperfrakcjonowanie dawki w radioterapii oznacza napromieniowywanie pacjenta
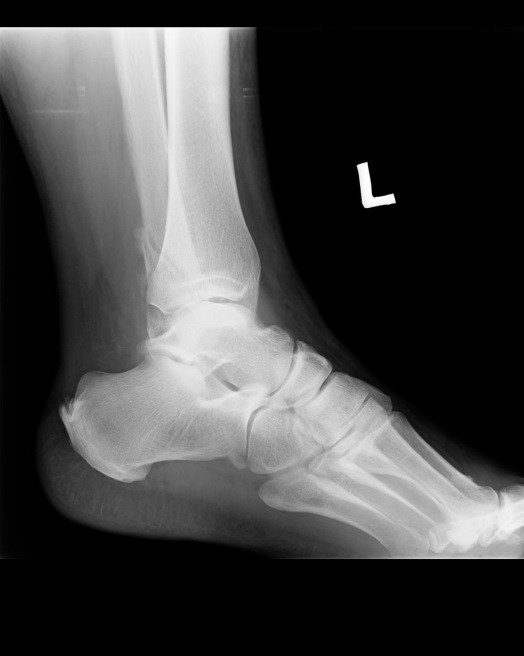
Na obrazie radiologicznym uwidoczniono złamanie kości
Diagnozowanie metodą PET oparte jest na zjawisku
Którą strukturę anatomiczną oznaczono na zamieszczonym obrazie rezonansu magnetycznego?
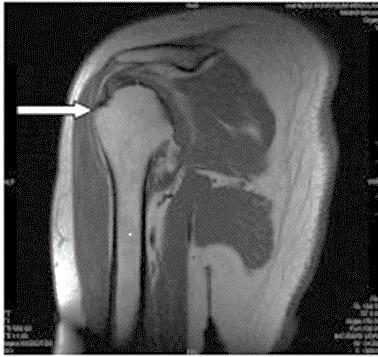
Który typ głowicy ultrasonograficznej przedstawiono na ilustracji?

Promieniowanie rentgenowskie jest
Jakie źródła promieniowania stosowane są w brachyterapii?
Skrótem CTV w radioterapii oznacza się
W trakcie obrazowania metodą rezonansu magnetycznego wykorzystywane jest zjawisko wysyłania sygnału emitowanego przez
Do zdjęcia prawych otworów międzykręgowych kręgosłupa szyjnego pacjent stoi w skosie
Standardowe badanie USG średniej wielkości piersi wykonuje się głowicą w zakresie częstotliwości
Który środek ochrony radiologicznej pacjenta należy zastosować podczas wykonywania zdjęcia bocznego kręgosłupa szyjnego?
W badaniu EKG odprowadzenie I rejestruje różnicę potencjałów między