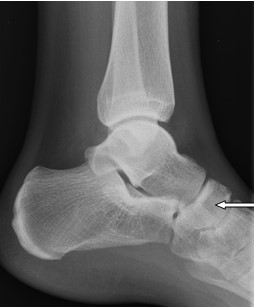
Pytanie 1
Na radiogramie czaszki strzałką zaznaczono
Wynik: 25/40 punktów (62,5%)
Wymagane minimum: 20 punktów (50%)
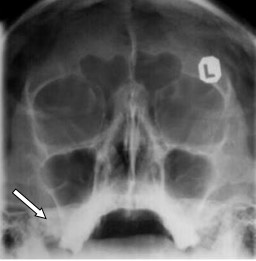
Na radiogramie czaszki strzałką zaznaczono

Którą strukturę anatomiczną uwidoczniono na zamieszczonym obrazie USG?
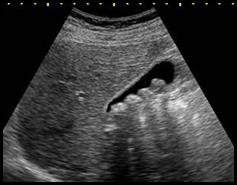
Z kratką przeciwrozproszeniową należy wykonać zdjęcie
Jakie są wielkości mocy dawki stosowanej w brachyterapii HDR?
Pracownia radioterapii z przyspieszaczem liniowym jest obszarem
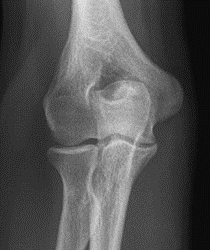
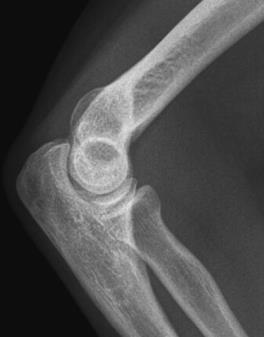
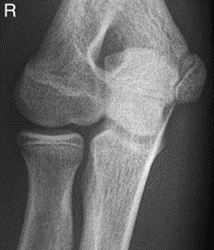
Które zdjęcie RTG stawu łokciowego zostało wykonane w projekcji skośnej w rotacji zewnętrznej?
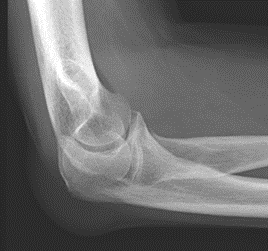
Odprowadzenie II rejestruje różnicę potencjałów między
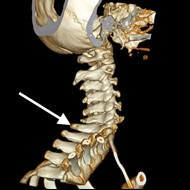
Na obrazie TK kręgosłupa strzałką wskazano wyrostek
Fala głosowa rozchodzi się
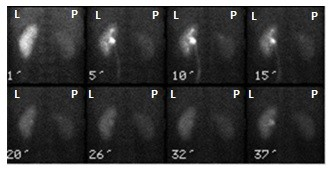
Na zarejestrowanych obrazach badania renoscyntygraficznego widać, że prawa nerka pacjenta
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz
W obrazowaniu metodą rezonansu magnetycznego T1 oznacza czas
Bezwzględnym przeciwwskazaniem do wykonania badania rezonansem magnetycznym jest
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
Dobierz dla standardowego pacjenta projekcję, pozycję i sposób ułożenia kasety o wymiarach 30 cm x 40 cm do zdjęcia przeglądowego układu moczowego.
| Projekcja | Pozycja | Ułożenie kasety | |||
|---|---|---|---|---|---|
| 1. | AP | 3. | stojąca | 5. | poprzeczne |
| 2. | PA | 4. | leżąca | 6. | podłużne |
W diagnostyce metodą rezonansu magnetycznego biorą udział
Na zamieszczonym przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano

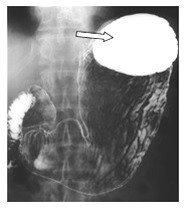
Który element żołądka zaznaczono strzałką na zdjęciu rentgenowskim?
Teleterapia polega na napromienowaniu
W standardowym badaniu elektrokardiograficznym elektrodę C4 należy umieścić
Zgodnie z procedurą wzorcową w badaniu MR należy ułożyć pacjenta na brzuchu do diagnostyki
W pracowni ultrasonograficznej technik elektroradiolog nie korzysta z przepisów dotyczących
W radiologii stomatologicznej ząb o numerze 23 to kieł
Wskazaniem do wykonania badania spirometrycznego jest
Który radiofarmaceutyk może zostać podany pacjentowi w scyntygrafii perfuzyjnej mózgu?
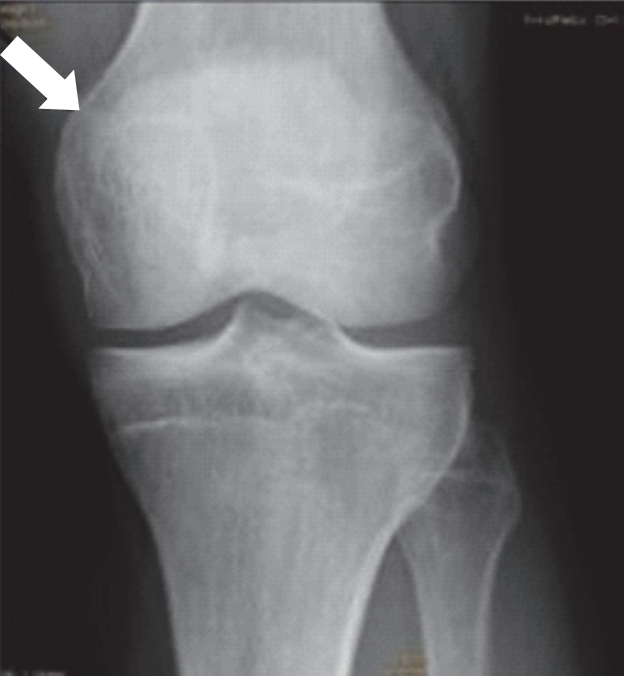
Którą strukturę anatomiczną zaznaczono na radiogramie stawu kolanowego?
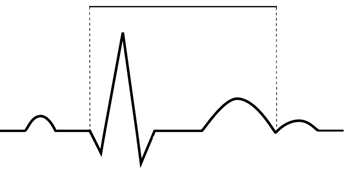
Na wykresie EKG zaznaczono
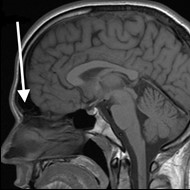
Na obrazie rezonansu magnetycznego głowy strzałką wskazano zatokę
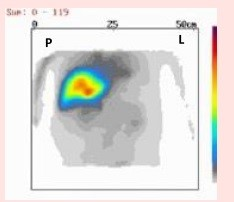
Który narząd został uwidoczniony na przedstawionym obrazie scyntygraficznym?
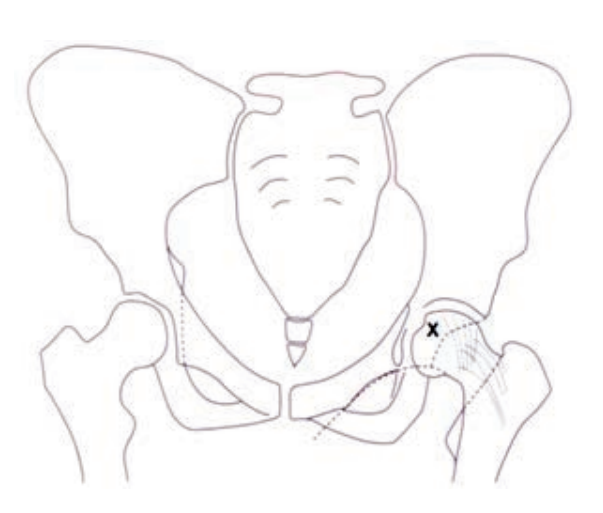
Na rycinie rentgenogramu w projekcji AP symbolem X oznaczono
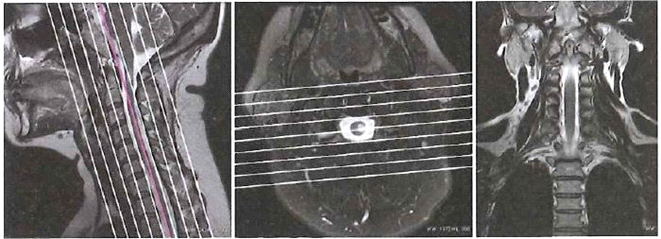
Obrazy MR kręgosłupa szyjnego przedstawiają etap planowania badania warstw
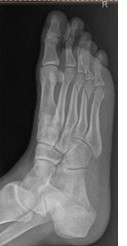
Na rentgenogramie stopy uwidocznione jest złamanie
Warstwa półchłonna (WP) jest wyrażona w mm Cu dla
Która struktura może być oknem akustycznym w badaniu ultrasonograficznym?
Przy ułożeniu do zdjęcia kręgów szyjnych CIII-CVII w projekcji przednio-tylnej lampa może być odchylona o kąt
Jak oznacza się w radioterapii obszar tkanek zawierający GTV i mikrorozsiewy w fazie niewykrywalnej klinicznie?
Brachyterapia wewnątrzprzewodowa jest stosowana w leczeniu
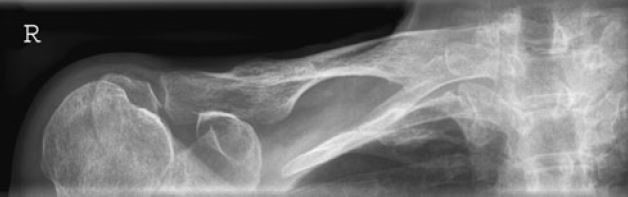
W jakiej projekcji i pod jakim kątem padania promienia centralnego został wykonany radiogram obojczyka?
Który radioizotop jest stosowany w scyntygrafii perfuzyjnej mózgu?
Na radiogramie strzałką oznaczono