Pytanie 1
Który radioizotop jest stosowany w diagnostyce i terapii raka tarczycy?
Wynik: 24/40 punktów (60,0%)
Wymagane minimum: 20 punktów (50%)
Który radioizotop jest stosowany w diagnostyce i terapii raka tarczycy?
Brachyterapia wewnątrzjamowa jest wykorzystywana podczas leczenia nowotworu
Gdzie znajduje się węzeł zatokowo-przedsionkowy wywołujący rytmiczne skurcze mięśnia serca?
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
Który materiał światłoczuły należy zastosować w rentgenodiagnostyce analogowej, by zminimalizować dawkę promieniowania jonizującego otrzymaną przez pacjenta?
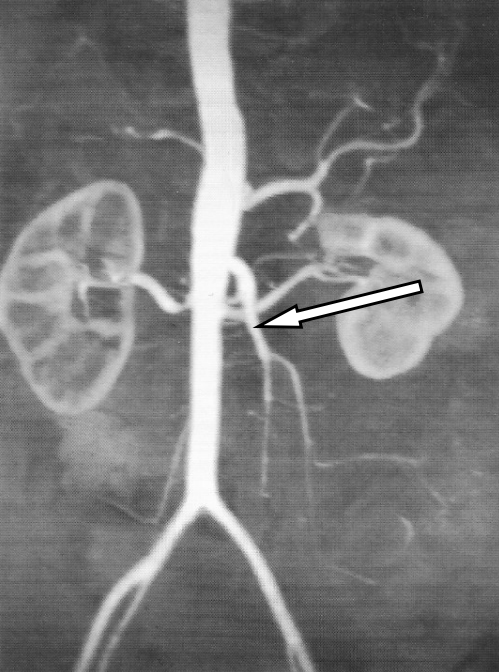
Którą tętnicę zaznaczono strzałką na obrazie MR?
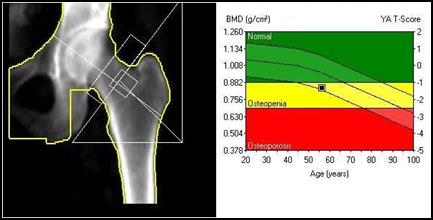
Zamieszczone na ilustracji obrazy dotyczą badania
Podczas badania EEG otwarcie oczu powoduje
Przy podejrzeniu ciała obcego w oczodole należy wykonać
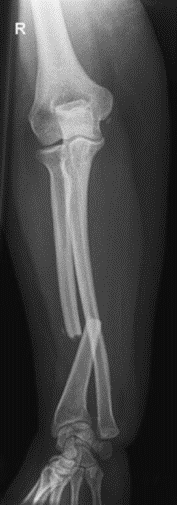
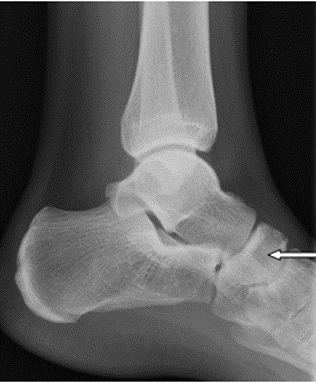
Na radiogramie uwidoczniono złamanie
W scyntygrafii wykorzystywane są głównie radioizotopy emitujące promieniowanie
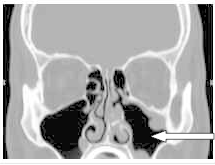
Na obrazie TK zaznaczono zatokę
Przemiana promieniotwórcza radu w ren opisana wzorem \( {}_{88}^{226}\text{Ra} \to {}_{86}^{222}\text{Rn} + {}_{2}^{4}\text{He} \) jest rozpadem
W badaniu MR czas repetycji TR jest parametrem określającym odstęp czasu między
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
W badaniu MR czas repetycji TR jest parametrem określającym odstęp czasu między
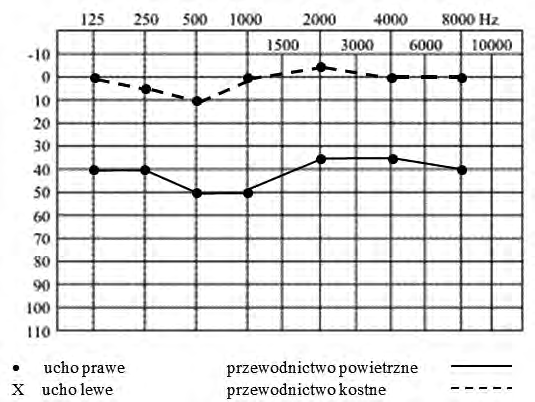
W badaniu audiometrycznym rezerwa ślimakowa to odległość między krzywą
Na podstawie zapisu badania audiometrycznego rozpoznano u pacjenta uszkodzenie słuchu
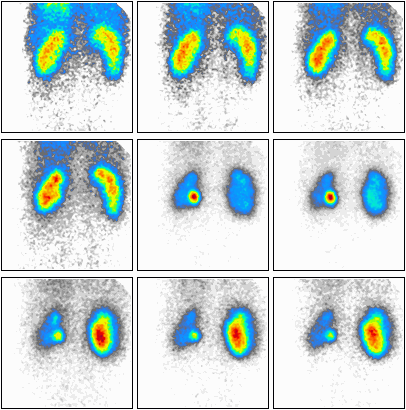
Podczas którego badania zostały zarejestrowane przedstawione obrazy?
Którym skrótem w badaniu spirometrycznym oznaczana jest pojemność życiowa płuc?
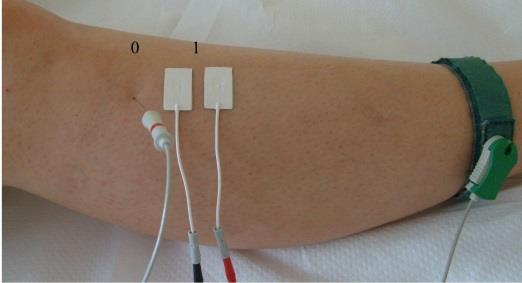
Na ilustracji przedstawiono przygotowanie pacjenta do badania
Przy ułożeniu do zdjęcia kręgów szyjnych CIII-CVII w projekcji przednio-tylnej lampa może być odchylona o kąt
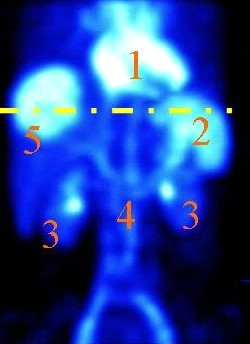
Który narząd na obrazie scyntygrafii znakowanej erytrocytami zaznaczono cyfrą 2?
Obszary napromieniania w technice IMRT w trakcie wykonywania zabiegu radioterapeutycznego wyznacza
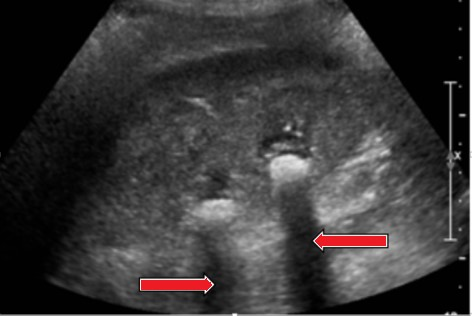
Który artefakt wskazano strzałkami na obrazie USG nerki?
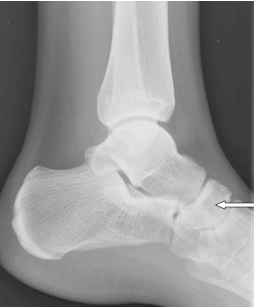
Na radiogramie strzałką oznaczono
Który program wtórnej rekonstrukcji obrazów TK pozwala na odwzorowanie wnętrza jelita grubego, tchawicy i oskrzeli?
W radiografii mianem SID określa się
Które odprowadzenie w badaniu EKG rejestruje różnice potencjałów pomiędzy lewym a prawym przedramieniem?
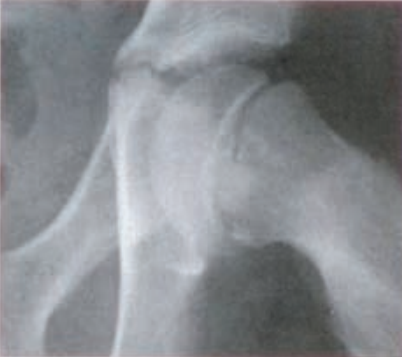
Na rentgenogramie przedstawione jest złamanie Saltera-Harrisa typu
Urografia polega na
Na zamieszczonym radiogramie strzałką oznaczono kość
Warstwa półchłonna (WP) służy do obliczania
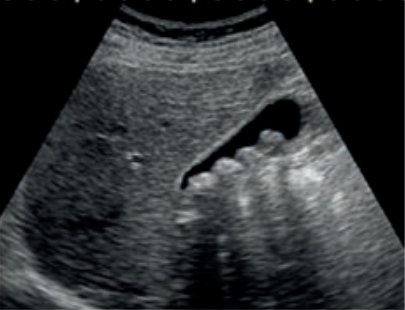
Jakie struktury anatomiczne uwidoczniono na obrazie USG?
Gadolin jako dożylny środek kontrastowy stosowany w MR powoduje
Dawka graniczna wyrażona jako dawka skuteczna (efektywna), dla osób zawodowo narażonych na działanie promieniowania jonizującego wynosi w ciągu roku kalendarzowego
Świeżo wynaczyniona krew na obrazach TK głowy bez podania środka kontrastowego ukazuje się jako obszar
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
Zastosowana w badaniu radiologicznym kratka przeciwrozproszeniowa powoduje