Pytanie 1
Zestaw rentgenogramów przedstawia
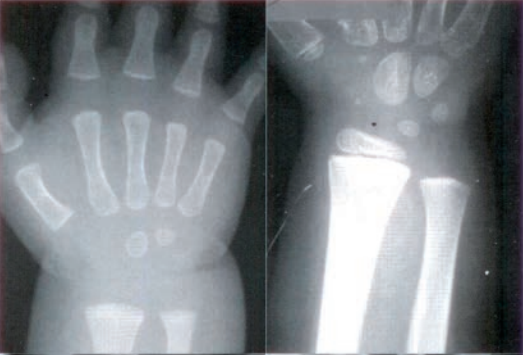
Wynik: 34/40 punktów (85,0%)
Wymagane minimum: 20 punktów (50%)
Zestaw rentgenogramów przedstawia

Na rentgenogramie przedstawione jest złamanie Saltera-Harrisa typu
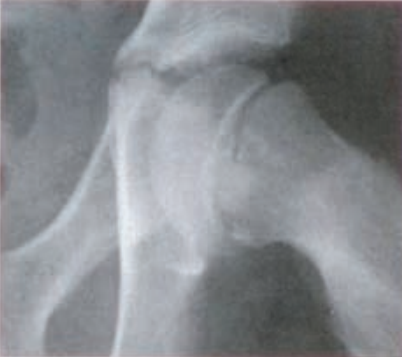
Co zostało uwidocznione na zamieszczonym radiogramie?
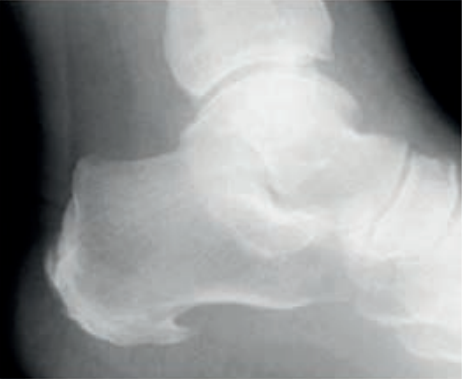
SPECT to
HRCT (high-resolution computed tomography) jest metodą obrazowania TK
Na rentgenogramie uwidoczniono badanie
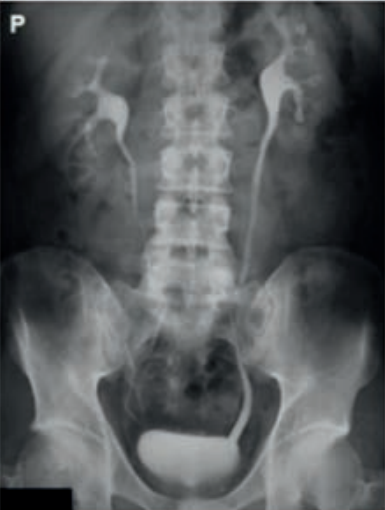
Który środek ochrony radiologicznej należy zastosować podczas badania czaszki 53-letniego pacjenta za pomocą tomografii komputerowej?
Zgodnie z obowiązującymi przepisami powierzchnia gabinetu rentgenowskiego, w którym jest zainstalowany zestaw rentgenowski do badań naczyniowych, powinna wynosić
W ułożeniu do rentgenografii AP stawu kolanowego promień główny pada
Czas repetycji w obrazowaniu metodą rezonansu magnetycznego to
Warstwa półchłonna (WP) jest wyrażona w mm Cu dla
W pracowni ultrasonograficznej technik elektroradiolog nie korzysta z przepisów dotyczących
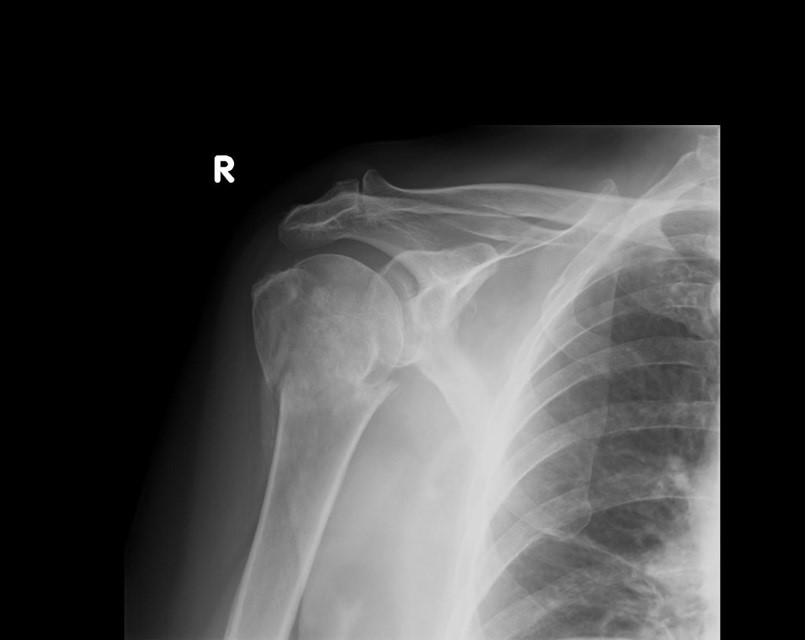
Na obrazie radiologicznym uwidoczniono złamanie kości
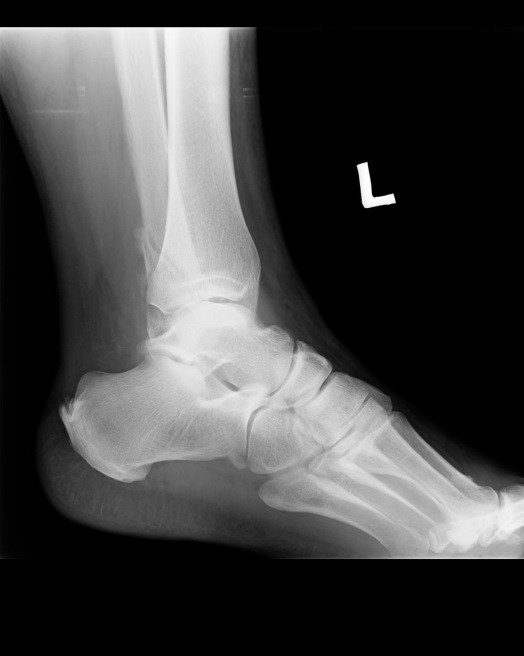
Na radiogramie uwidoczniono złamanie
Standardowe badanie urografii polega na podaniu pacjentowi środka kontrastującego
Podczas teleradioterapii piersi lewej narządem krytycznym jest
Kryterium rozpoznawczym dla fali δ (delta) w badaniu EKG jest
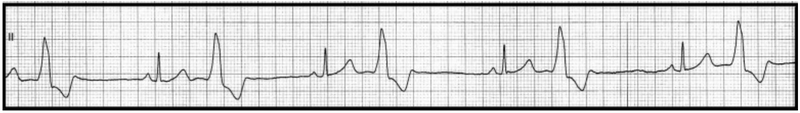
Który stan patologiczny został zarejestrowany podczas wykonywania badania EKG?
Podstawowym elementem diagnostycznym aparatury izotopowej wykorzystującej emisyjne metody pomiaru jest
Obrazy DDR są tworzone w trakcie
Do wykonania stomatologicznego zdjęcia rentgenowskiego techniką kąta prostego promień centralny należy ustawić prostopadle do
Który materiał światłoczuły należy zastosować w rentgenodiagnostyce analogowej, by zminimalizować dawkę promieniowania jonizującego otrzymaną przez pacjenta?
Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest
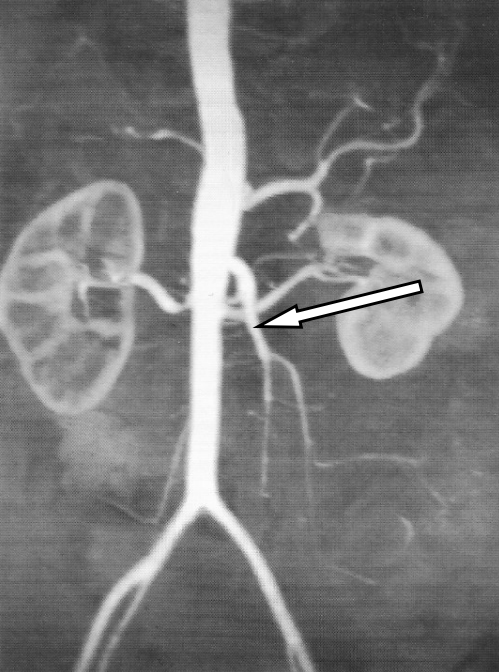
Którą tętnicę zaznaczono strzałką na obrazie MR?
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
W badaniu MR czas repetycji TR jest parametrem określającym odstęp czasu między
W pozytonowej emisyjnej tomografii komputerowej PET radioznacznik podawany jest pacjentowi najczęściej
Jak oznacza się w radioterapii obszar tkanek zawierający GTV i mikrorozsiewy w fazie niewykrywalnej klinicznie?
W brachyterapii MDR stosowane są dawki promieniowania
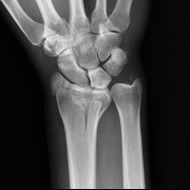
Na obrazie radiologicznym nadgarstka uwidoczniono złamanie nasady
Dawka graniczna wyrażona jako dawka skuteczna (efektywna), dla osób zawodowo narażonych na działanie promieniowania jonizującego wynosi w ciągu roku kalendarzowego
W celu maksymalnego ograniczenia dawki promieniowania badanie rentgenowskie u dzieci należy wykonać
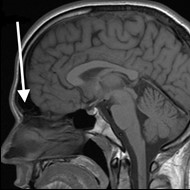
Na obrazie rezonansu magnetycznego głowy strzałką wskazano zatokę
Jednostką indukcji magnetycznej jest
W celu wykonania badania scyntygraficznego układu kostnego radiofarmaceutyk należy podać pacjentowi
Który radioizotop jest stosowany w scyntygrafii perfuzyjnej mózgu?
Wskazaniem do zastosowania brachyterapii w leczeniu radykalnym jest rak
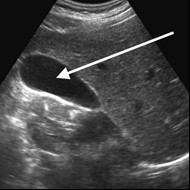
Na obrazie ultrasonograficznym jamy brzusznej strzałką wskazano
Objawem późnego odczynu popromiennego po teleradioterapii jest
W zapisie EKG zespół QRS odzwierciedla