Pytanie 1
W brachyterapii MDR stosowane są dawki promieniowania
Wynik: 28/40 punktów (70,0%)
Wymagane minimum: 20 punktów (50%)
W brachyterapii MDR stosowane są dawki promieniowania
Do badania MR nadgarstka pacjenta należy ułożyć
W której technice obrazowania zostają zarejestrowane jednocześnie dwa przeciwbieżne kwanty promieniowania gamma o równej energii 511 keV?
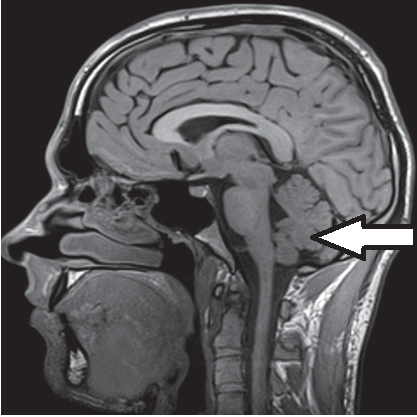
Którą strukturę anatomiczną oznaczono strzałką na obrazie rezonansu magnetycznego?
Które ciało obce w obszarze badania nie stanowi przeciwwskazania do wykonania MR?
W radiografii mianem SID określa się
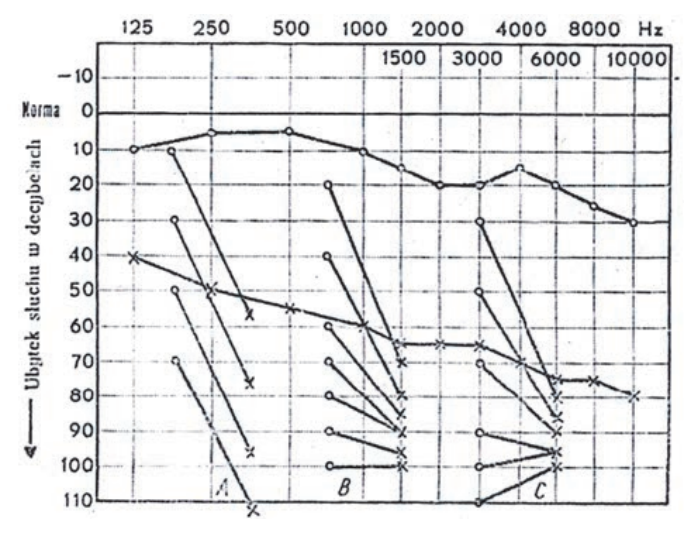
Audiogram przedstawia próbę
Jaki czas należy ustawić do wykonania zdjęcia rentgenowskiego dwójki górnej lewej?
| Tabela ekspozycji | |||
|---|---|---|---|
| wartości | czasu (s) | napięcia (kV) | natężenia (mA) |
| zęby przedtrzonowe i kły | 0,160 | 60 | 8 |
| siekacze | 0,120 | 60 | 8 |
| zęby trzonowe | 0,200 | 60 | 8 |
| ekspozycja zgryzowo-skrzydełkowa | 0,180 | 66 | 6 |
Jednym z kryteriów poprawnie wykonanego badania spirometrycznego jest czas trwania natężonego wydechu, który powinien wynosić u osób powyżej 10 roku życia co najmniej
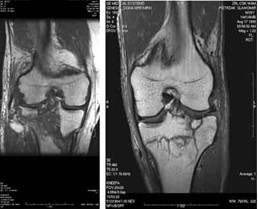
Którą metodą i w której płaszczyźnie zostało wykonane badanie stawu kolanowego zobrazowane na zdjęciach?
Limfografia to badanie kontrastowe
W którym okresie ciąży wykonanie u kobiety zdjęcia rentgenowskiego klatki piersiowej jest najbardziej szkodliwe dla płodu?
Ligand stosuje się
Droga przewodnictwa powietrznego fali akustycznej przebiega przez
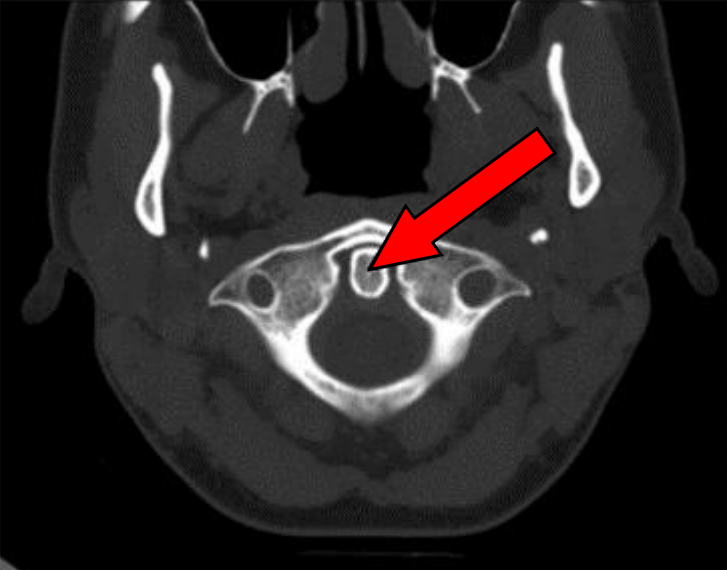
Na przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano
Rozpoczęcie badania TK nerek po 20-30 sekundach od początku podania środka kontrastowego umożliwia diagnostykę
W systemie międzynarodowym ząb pierwszy przedtrzonowy po stronie lewej oznacza się symbolem
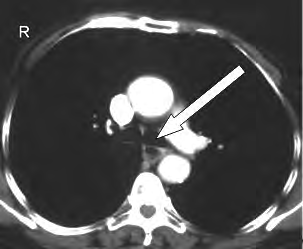
Na obrazie TK klatki piersiowej w przekroju poprzecznym strzałką oznaczono
Radioizotopowa terapia medycyny nuklearnej polega na wprowadzeniu do tkanek lub narządów radiofarmaceutyku
Wskazaniem do wykonania scyntygrafii perfuzyjnej jest
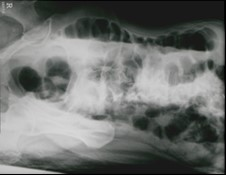
Które badanie zostało zarejestrowane na przedstawionym radiogramie?
Promieniowanie rentgenowskie jest
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz
Które ciało obce w obszarze badania nie stanowi przeciwwskazania do wykonania MR?
Zgodnie z procedurą wzorcową w badaniu MR należy ułożyć pacjenta na brzuchu do diagnostyki
Jak konwencjonalnie frakcjonuje się dawkę w teleradioterapii?
Pracownia radioterapii z przyspieszaczem liniowym jest obszarem
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
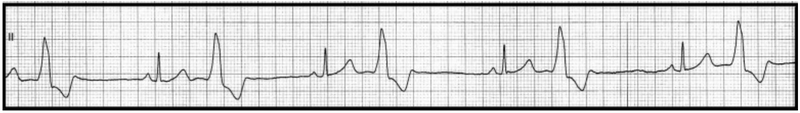
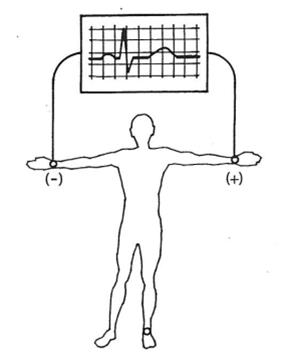
Które odprowadzenie elektrokardiograficzne przedstawiono na ilustracji?
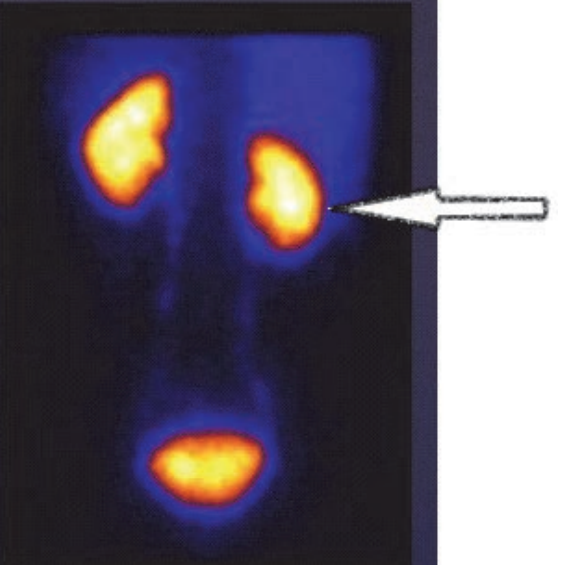
Na scyntygramie strzałką oznaczono
W standardowym badaniu elektrokardiograficznym elektrodę C4 należy umieścić
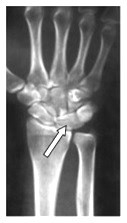
Na obrazie radiologicznym nadgarstka strzałką zaznaczona jest kość
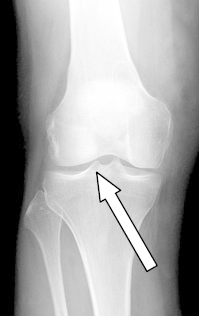
Którą strukturę anatomiczną oznaczono strzałką na radiogramie stawu kolanowego?
Po zakończeniu badania angiograficznego należy zapisać w dokumentacji medycznej pacjenta:
Hiperfrakcjonowanie dawki w teleradioterapii polega na napromienianiu 2 do 3 razy dziennie dawką frakcyjną
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
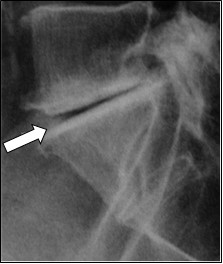
Na rentgenogramie strzałką zaznaczono
Którym skrótem oznacza się tomografię komputerową wysokiej rozdzielczości?
Który stan patologiczny został zarejestrowany podczas wykonywania badania EKG?