Pytanie 1
Po wykonanej radioterapii do dokumentacji pacjenta należy wpisać dawkę promieniowania w jednostce
Wynik: 33/40 punktów (82,5%)
Wymagane minimum: 20 punktów (50%)
Po wykonanej radioterapii do dokumentacji pacjenta należy wpisać dawkę promieniowania w jednostce
Jaki sposób frakcjonowania dawki jest stosowany w radioterapii konwencjonalnej?
Gruboziarnista folia wzmacniająca wpływa na zwiększenie na obrazie rentgenowskim nieostrości
Brachyterapia polega na napromieniowaniu pacjenta promieniowaniem
W badaniu PET CT wykorzystuje się radioizotopy emitujące promieniowanie
Odprowadzenie II rejestruje różnicę potencjałów między
Elementem pomocniczym w radioterapii, zapewniającym powtarzalność ułożenia w pozycji terapeutycznej, a także unieruchomienie pacjenta, jest
Zastosowana w badaniu radiologicznym kratka przeciwrozproszeniowa powoduje
W badaniu audiometrycznym rezerwa ślimakowa to odległość między krzywą
Celem radioterapii paliatywnej nie jest
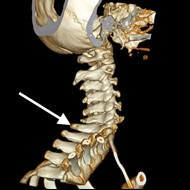
Na obrazie TK kręgosłupa strzałką wskazano wyrostek
W którym okresie ciąży wykonanie u kobiety zdjęcia rentgenowskiego klatki piersiowej jest najbardziej szkodliwe dla płodu?
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
Do zdjęcia rentgenowskiego żeber w projekcji skośnej tylnej pacjenta należy ustawić
Podczas badania EEG w systemie „10-20” literą A oznacza się elektrody
Droga przewodnictwa powietrznego fali akustycznej przebiega przez
Objawem późnego odczynu popromiennego po teleradioterapii jest
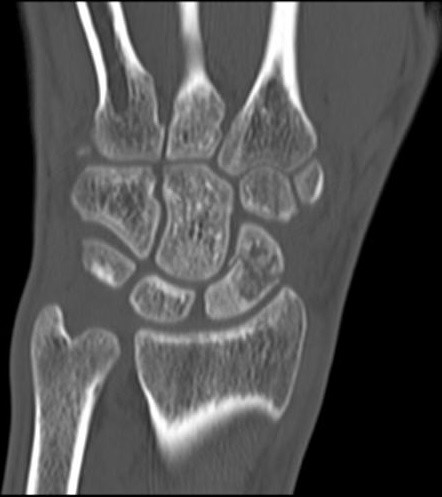
Na obrazie TK nadgarstka uwidocznione jest złamanie kości
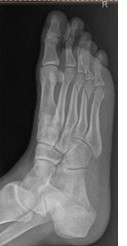
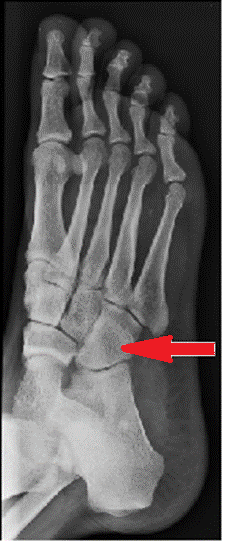
Na rentgenogramie stopy uwidocznione jest złamanie
Elementem systemu rejestracji obrazu, w którym fotony promieniowania X są bezpośrednio konwertowane na sygnał elektryczny, jest
Do zdjęcia prawych otworów międzykręgowych kręgosłupa szyjnego pacjent stoi w skosie
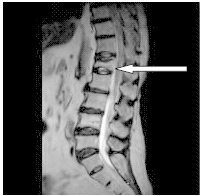
Na obrazie rezonansu magnetycznego strzałką oznaczono patologiczny kręg
Cholangiografia to badanie radiologiczne
Na radiogramie stopy strzałką wskazano kość
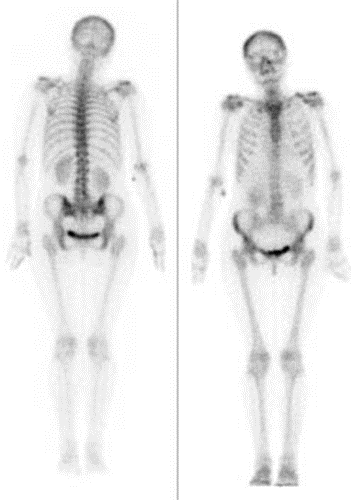
W której technice obrazowania zostają zarejestrowane jednocześnie dwa przeciwbieżne kwanty promieniowania gamma o równej energii 511 keV?
Do podstawowych projekcji stosowanych w diagnostyce mammograficznej należą
W leczeniu izotopowym tarczycy należy podać
Przedstawiony obraz został zarejestrowany podczas wykonania
W jaki sposób należy oprzeć stroik w audiometrycznym badaniu przewodnictwa kostnego?
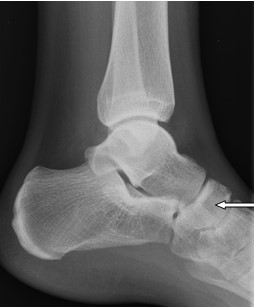
Na radiogramie strzałką oznaczono
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Limfografia to badanie kontrastowe
Jak przebiega promień centralny w projekcji AP czaszki?
Zadaniem technika elektroradiologii w pracowni badań naczyniowych jest
Jaki jest cel stosowania bolusa w radioterapii?
Wskazaniem do wykonania badania spirometrycznego jest
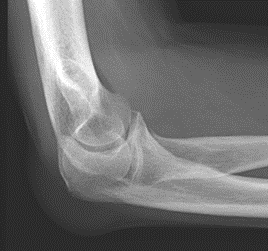
Które zdjęcie RTG stawu łokciowego zostało wykonane w projekcji skośnej w rotacji zewnętrznej?
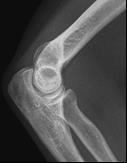
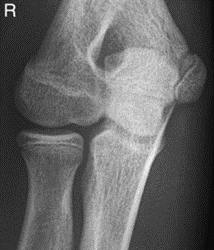
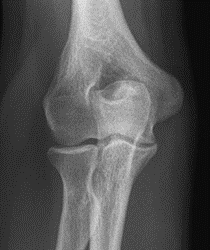
Więzka promieniowania X to
Technik elektroadiolog do badania MR kręgosłupa lędźwiowego powinien ułożyć pacjenta
Który środek ochrony radiologicznej pacjenta należy zastosować podczas wykonywania zdjęcia bocznego kręgosłupa szyjnego?