Pytanie 1
W radiografii mianem SID określa się
Wynik: 38/40 punktów (95,0%)
Wymagane minimum: 20 punktów (50%)
W radiografii mianem SID określa się
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
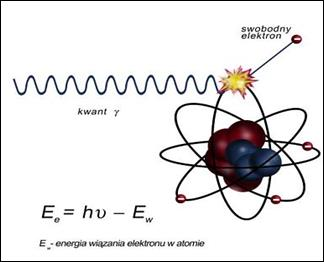
Na ilustracji przedstawiono zjawisko
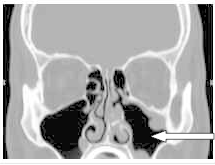
Na obrazie TK zaznaczono zatokę
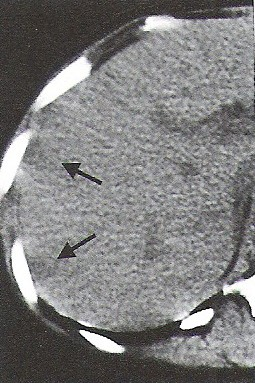
Świeżo wynaczyniona krew na obrazach TK głowy bez podania środka kontrastowego ukazuje się jako obszar
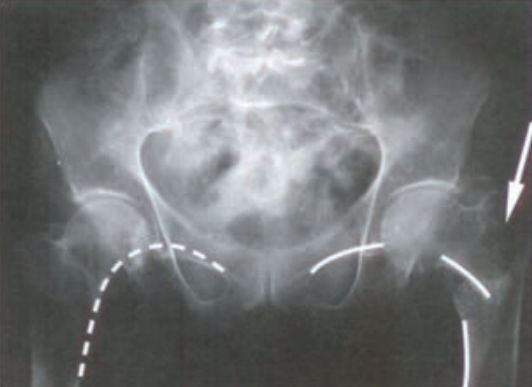
Radiogram przedstawia
Po zakończeniu badania angiograficznego należy zapisać w dokumentacji medycznej pacjenta:
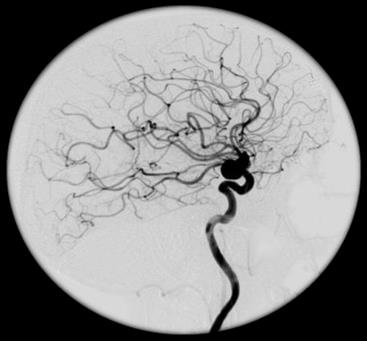
W przedstawionym na ilustracji obrazie badania angiograficznego uwidoczniono
W badaniu EKG punktem przyłożenia odprowadzenia przedsercowego C2 jest
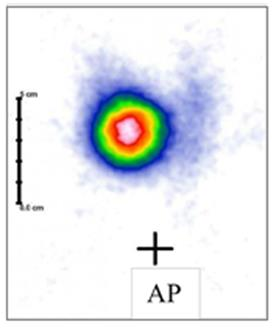
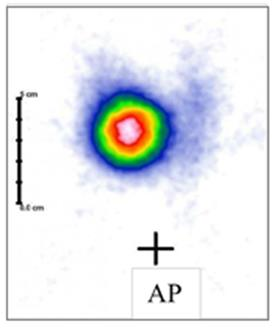
Na scyntygramie tarczycy uwidoczniono guzek
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
Które informacje należy zamieścić na strzykawce z radiofarmaceutykiem przygotowanym przez technika elektroradiologa?
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
Na zamieszczonym przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano

Co zostało uwidocznione na zamieszczonym radiogramie?
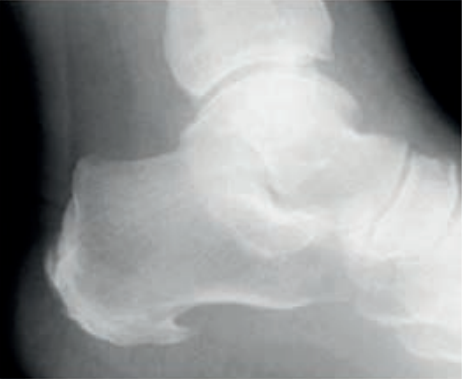
Przedstawiony obraz został zarejestrowany podczas wykonania
Technik elektroradiolog do badania MR kręgosłupa lędźwiowego powinien ułożyć pacjenta:
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
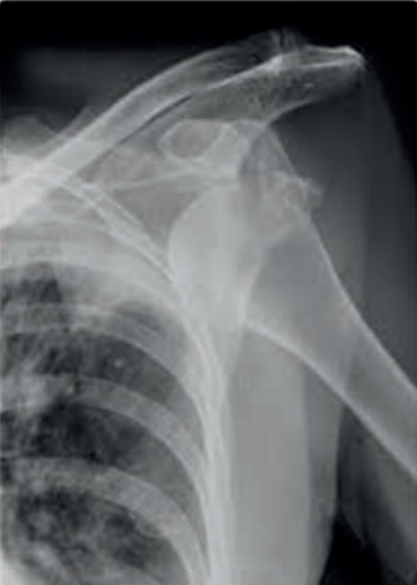
W jakiej projekcji i pod jakim kątem padania promienia centralnego został wykonany radiogram obojczyka?
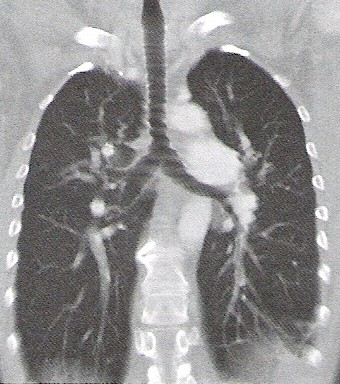
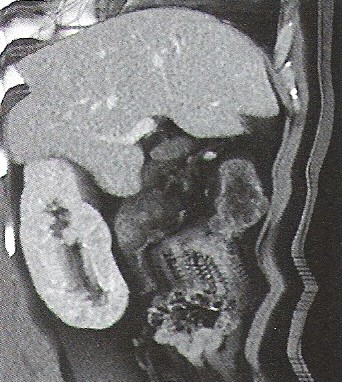
Na którym obrazie TK uwidoczniony jest artefakt spowodowany ruchami oddechowymi pacjenta?

W systemie międzynarodowym ząb pierwszy przedtrzonowy po stronie lewej oznacza się symbolem
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
Które znaczniki są wykorzystywane w scyntygrafii tarczycy?
Jaki jest cel stosowania bolusa w radioterapii?
Rutynowe badanie koronarografii prawej tętnicy wieńcowej wykonywane jest w rzucie skośnym przednim
W diagnostyce mammograficznej punktowy ucisk sutka stosuje się w projekcji
Odprowadzenie EKG mierzące różnicę potencjałów między lewym podudziem a prawym przedramieniem oznacza się jako
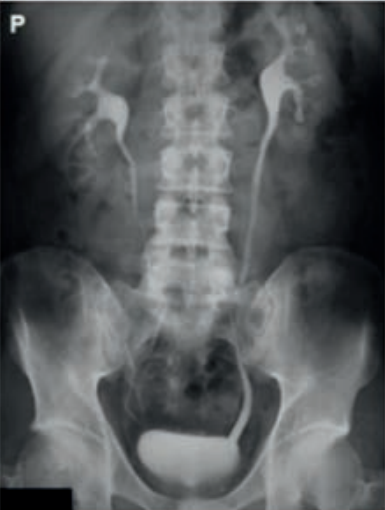
Na rentgenogramie uwidoczniono badanie
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
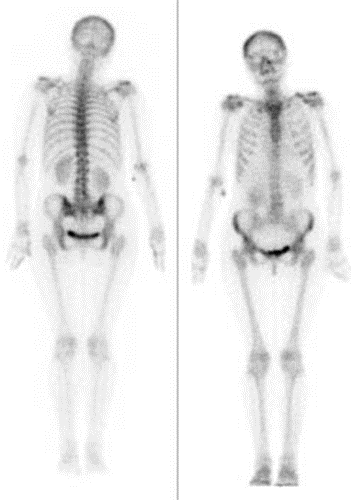
Wskazaniem do wykonania scyntygrafii perfuzyjnej jest
Rytm alfa i beta rejestruje się podczas badania
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
Jakie symbole mają odprowadzenia kończynowe dwubiegunowe w badaniu EKG?
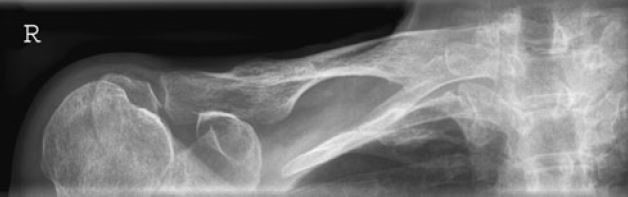
Którą patologię uwidoczniono na zamieszczonym rentgenogramie?
W której pozycji wykonuje się zdjęcie jamy brzusznej u pacjenta z podejrzeniem perforacji żołądka?
Na scyntygramie tarczycy został uwidoczniony guzek
Zgodnie ze standardami do wykonania zdjęcia bocznego czaszki, należy zastosować kasetę o wymiarze
Cholangiografia to badanie radiologiczne
Kasety do pośredniej radiografii cyfrowej CR są wyposażone