Pytanie 1
Którą masę etylenu o czystości 99,8% należy wprowadzić do reaktora polimeryzacji, aby otrzymać 19600 g polietylenu?
| Proces przebiega zgodnie z równaniem reakcji nH2C=CH2 → -[-CH2-CH2-]-n |
Wynik: 33/40 punktów (82,5%)
Wymagane minimum: 20 punktów (50%)
Którą masę etylenu o czystości 99,8% należy wprowadzić do reaktora polimeryzacji, aby otrzymać 19600 g polietylenu?
| Proces przebiega zgodnie z równaniem reakcji nH2C=CH2 → -[-CH2-CH2-]-n |
Jakie urządzenie jest używane do pomiaru wilgotności w materiałach stałych?
Zapotrzebowanie energetyczne dla elektrolitycznego otrzymania 1 tony Cl2 wynosi 9,72 GJ. Wartość opałowa gazu koksowniczego wynosi 17000 kJ/m3. Korzystając z danych zawartych w tabeli oblicz dobowe zapotrzebowanie linii produkcyjnych na gaz koksowniczy.
| Zapotrzebowanie energetyczne podczas elektrolitycznego otrzymywania Cl2 | 9,72 GJ/t |
| Wydajność elektrolitycznego otrzymywania Cl2 | 250 kg Cl2/h |
Surowcami w procesie otrzymywania chloroetenu (chlorku winylu) są
| Otrzymywanie chlorku winylu | ||
|---|---|---|
| Jedna z metod wytwarzania chlorku winylu opiera się na następujących reakcjach: | ||
| CH2=CH2 + Cl2 → CH2Cl-CH2Cl | ||
| CH2Cl-CH2Cl →500°C CH2=CHCl + HCl | ||
| CH ≡ CH + HCl → CH2=CHCl |
Jony Mg2+ w reakcji z roztworem EDTA tworzą charakterystyczne związki chelatowe. Tę właściwość wykorzystuje się w oznaczaniu ilościowym magnezu przy zastosowaniu metody
Jak przeprowadza się alkalimetryczne oznaczanie kwasu octowego?
Regulacja procesu destylacji rurowo-wieżowej odbywa się na podstawie wyników nieprzerwanych badań kontrolnych dotyczących parametrów różnych frakcji:
Ile gramów azotanu(V) srebra należy odważyć, aby przygotować 5 dm3 roztworu o stężeniu 0,15 mol/dm3?
| MAgNO3 = 170 g/mol |
W trakcie suszenia substancji stałej do atmosfery dostają się pewne ilości tej substancji. Które z poniższych urządzeń ma na celu ograniczenie strat tej substancji?
Zakład produkujący superfosfat stosuje surowiec, w którym zawartość tlenku fosforu(V) powinna wynosić 30%. Próbki pobierane z surowca wzbogacanego w procesie flotacji zawierają jedynie 25% tego tlenku. Jakie działania należy podjąć, aby uzyskać surowiec spełniający normy jakościowe?
Etap produkcji odnosi się do koncepcji technologicznej?
Którą z poniższych metod można zastosować do pomiaru skręcalności właściwej substancji organicznej?
Do 200 g wody wsypano 63,8 g azotanu(V) potasu, otrzymując w temperaturze 293 K roztwór nasycony tej soli. Ile gramów KNO3 co najmniej należy dosypać, aby po podgrzaniu do temperatury 313 K roztwór pozostał nasycony?
| Wzór chemiczny | Nazwa | Rozpuszczalność g/100 g H₂O | |||||
|---|---|---|---|---|---|---|---|
| 273 K | 293 K | 313 K | 333 K | 353 K | 373 K | ||
| KJ | Jodek potasu | 127,3 | 144 | 160,5 | 176,4 | 191,8 | 206,6 |
| KNO₃ | Azotan(V) potasu | 13,6 | 31,9 | 62,9 | 109,0 | 170,9 | 242,4 |
| K₂CO₃ | Węglan potasu | 185,5 | 167,3 | 181,4 | 202,7 | 230,9 | 268,6 |
| KOH | Wodorotlenek potasu | 401,1 | 691,9 | 325,3 | 368,8 | 455,6 | 581,6 |
Kluczowym działaniem w procesie uzyskiwania tlenu i azotu jest skraplanie powietrza, które realizuje się przy użyciu metody
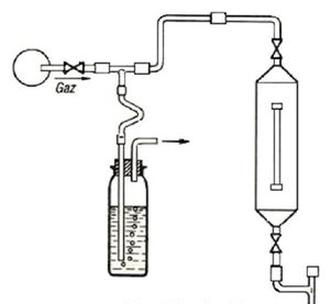
Na schemacie przedstawiono zestaw do
Podczas przeprowadzania analizy strąceniowej żelaza w próbce ważącej 0,3495 g uzyskano 0,2000 g osadu Fe2O3. Wyznacz procentowy udział jonów żelaza(III) w tej próbce, przyjmując, że współczynnik analityczny do przeliczenia masy Fe2O3 na Fe wynosi 0,6994.
Oznaczanie zawartości magnezu w nawozowych ekstraktach realizuje się, miareczkując roztwór za pomocą roztworu EDTA. Jakie to oznaczenie?
Aby przygotować 400 g roztworu KNO₃ o stężeniu 5%, ile substancji należy użyć?
Jakie parametry powinny być zapisywane przez obsługę wapiennego pieca szybowego w dokumentacji dotyczącej nadzorowanego procesu?
Gaz wykorzystywany do syntezy amoniaku musi zawierać substraty w stosunku molowym zbliżonym do wymaganego, a zawartość związków tlenu nie powinna wynosić więcej niż 5 ppm. Jaką metodę należy wykorzystać do oceny jakości gazu syntezowego?
Która z dostępnych suszarek pozwala na suszenie przy najniższej wartości temperatury?
Jakim sposobem można pobrać próbkę surowca fosforowego do analizy jakościowej, która ma być wykorzystana w produkcji superfosfatu prostego?
Jak należy przechowywać metanol?
Próbka, która jest w całości przeznaczona do jednego oznaczenia, to próbka
Każda próbka, która trafia do laboratorium i jest analizowana, powinna być zarejestrowana w dzienniku analiz. Jakie informacje muszą być tam uwzględnione?
Podczas określania stężenia roztworu sacharozy z wykorzystaniem metody refraktometrycznej przeprowadza się pomiar
Jak przeprowadza się oznaczenie pH próbki ścieków przemysłowych?
Możliwe jest zwiększenie produkcji benzyny z instalacji DRW podczas procesu
Ile mililitrów kwasu solnego o stężeniu 2 mol/dm3 jest wymagane do przygotowania 250 cm3 roztworu o stężeniu 0,15 mol/dm3? (MHCl =36,46 g/mol)
W systemie destylacji rurowo-wieżowej, w przypadku awarii pomp tłoczących ropę naftową, konieczne jest wyłączenie palników pieca oraz wypchnięcie zgromadzonego surowca z rur pieca za pomocą pary do kolumny destylacyjnej w celu
Aby zapobiec zestalaniu się stężonych roztworów saletry amonowej podczas wytwarzania nawozu azotowego, należy je utrzymywać w odpowiednio wysokiej temperaturze (od 137 °C do 377 °C), w zależności od stężenia roztworu. Jakie medium technologiczne będzie właściwe do ogrzewania rurociągów w sposób przeponowy, przez które przepływają te roztwory?
Aby przeprowadzić ilościowe oznaczanie kwasu siarkowego(VI) za pomocą metody klasycznego miareczkowania, należy przygotować
Która z wymienionych substancji najczęściej służy do określania miana roztworu HCl?
Kwas azotowy(V) w dużym stężeniu powinien być transportowany w cysternach lub pojemnikach wykonanych
Klasyfikację wybranych stali według ich składu chemicznego zestawiono w tabeli.
Analiza badanej próbki wykazała zawartość C = 0,21 %, Mn = 1,3 %, Si = 0,20 %, S = 0,035 %, P = 0,040 %.
Którą stal poddano badaniu?
| Symbol stali | Skład chemiczny % | ||||
|---|---|---|---|---|---|
| C | Mn | Si | Smax | Pmax | |
| St03 | max 0,25 | 1,3 | max 0,40 | 0,065 | 0,070 |
| St3S | max 0,22 | 1,1 | 0,1÷0,35 | 0,050 | 0,050 |
| St3W | max 0,17 | 1,3 | 0,1÷0,35 | 0,040 | 0,040 |
| St4W | max 0,20 | 1,3 | 0,1÷0,35 | 0,040 | 0,040 |
| MSt5 | 0,26÷0,37 | max 0,35 | 0,050 | 0,050 | 0,050 |
Jak według zasad bhp powinny być realizowane prace związane z konserwacją instalacji do chlorowania benzenu?
Każdy z urządzeń działających w technicznych pomieszczeniach wydziałów produkcji przemysłu chemicznego powinien mieć
Wolnorodnikowa polimeryzacja polietylenu odbywa się w temperaturach od 420 do 530 K oraz pod ciśnieniem w zakresie 150 do 200 MPa. Który z pomiarów warunków procesowych wskazuje na poprawny przebieg obserwowanego procesu?
Jakie informacje powinny być zawarte w dokumentacji dotyczącej procesu produkcji superfosfatu metodą okresową?
Oczyszczona ropa naftowa może zawierać maksymalnie 3 mg NaCl w 1 dm3 oraz mniej niż 0,2% mas. wody. Przeprowadzona analiza nowej partii ropy o gęstości 780 g/dm3 wykazała, że zawiera ona 0,01% mas. soli w stosunku do masy ropy oraz 1 g H2O w 1 dm3. Jak oceniasz jakość dostarczonego surowca?