Pytanie 1
Jaką substancję oznacza się metodą Kjeldahla?
Wynik: 15/40 punktów (37,5%)
Wymagane minimum: 20 punktów (50%)
Jaką substancję oznacza się metodą Kjeldahla?
Zjawisko opisane w ramce to
| Jeżeli w wodzie zostanie rozpuszczona α-D-glukopiranoza, to roztwór tuż po rozpuszczeniu wykazuje skręcalność właściwą [α]D= +112,2°, lecz w miarę upływu czasu skręcalność ta stopniowo spada do wartości charakterystycznej w stanie równowagi, mianowicie [α]D= +52,7° |
Wśród wskaźników stosowanych w analizach kompleksometrycznych znajdują się
Lepkość oleju napędowego w temperaturze 40°C wynosi 3 mm2/s. Jaką lepkość to określa?
Wzorzec glukozy o stężeniu 0,5 mg/cm3 wykazuje absorbancję 0,150. Jakie jest stężenie glukozy w badanej próbie, jeśli jej absorbancja wynosi 0,450 przy założeniu spełnienia prawa Lamberta-Beera w badanym zakresie stężeń i identycznych warunkach pomiaru?
stężenie glukozy [mg/cm3] = Ap / Aw · cw Ap - absorbancja próbki Aw - absorbancja wzorca cw - stężenie wzorca [mg/cm3] |
Jak należy przygotować próbkę wody do zamrożenia w naczyniu, które
W świadectwie jakości roztworu amoniaku cz. podana jest informacja: zawartość amoniaku 30÷32% m/m Uwzględniając informacje zawarte w tabeli, określ gęstość tego roztworu w temperaturze 20°C.
| Zależność gęstości roztworu amoniaku od stężenia w 20°C | |||||||
|---|---|---|---|---|---|---|---|
| % wagowy | 1 | 6 | 10 | 16 | 20 | 26 | 30 |
| gęstość [g/cm³] | 0,9939 | 0,9730 | 0,9575 | 0,9362 | 0,9229 | 0,9040 | 0,8920 |
Krzywa na rysunku obrazuje miareczkowanie

Który zestaw sprzętu jest niezbędny do wykonania oznaczenia kwasowości wody?
| Procedura oznaczania kwasowości wody metodą miareczkowania wobec wskaźników. |
|---|
| Do kolby stożkowej odmierzyć 100 cm3 badanej wody, dodać 3 krople oranżu metylowego i miareczkować roztworem NaOH o stężeniu 0,05 mol/dm3 do pierwszej zmiany barwy z różowej na słomkowożółtą. Następnie dodać 10 kropli fenoloftaleiny i miareczkować roztworem NaOH do wyraźnie różowego zabarwienia utrzymującego się przez 3 minuty. |
Na podstawie zamieszczonych w tabeli informacji wskaż związek chemiczny, którego należy użyć w celu oddzielenia kationu Pb2+ z mieszaniny kationów grupy pierwszej.
| Pb2+ | Hg22+ | Ag+ |
| + rozc. HCl | ||
| PbCl2↓ | Hg2Cl2↓ | AgCl↓ |
| Dodać kilka kropli H2O, ogrzać na łaźni, odsączyć na gorąco | ||
| Pb2+ | Hg2Cl2↓ | AgCl↓ |
| + K2CrO4 | + NH3 aq | +stęż. NH3 aq |
W równaniu dotyczącym iloczynu rozpuszczalności siarczanu(VI) baru: Kso = [Ba2+][SO42-], jonowe stężenia Ba2+ oraz SO42- są przedstawione jako
Oznaczona twardość ogólna wody wynosi 2 mval/dm3. Wartość ta przeliczona na stopnie niemieckie, zgodnie z zamieszczonym przelicznikiem jednostek, wynosi
| 1 mval/dm3 – 2,8°dH (stopni niemieckich) |
Czym jest eluent?
Wartość pH punktu równoważnikowego w miareczkowaniu mocnych kwasów przy użyciu mocnych zasad wynosi
W ramce zamieszczono opis wykonania oznaczenia metodą
| Oznaczenie aktywności amylaz opiera się na pomiarze ilości rozpuszczonej skrobi, co określa się na podstawie zmiany intensywności zabarwienia w mieszaninie reakcyjnej, w skład której wchodzi jod. |
Ze względu na zmieniającą się podczas miareczkowania objętość badanego roztworu, należy obliczyć poprawkę p w przypadku miareczkowania
| p = Vpróbki + Vwody + Vtitrantu Vpróbki + Vwody |
W trakcie badań mikrobiologicznych, pomimo stosowania pełnego i sterylnego stroju ochronnego oraz szczególnej staranności przy przeprowadzaniu pomiarów, dochodzi do zanieczyszczenia podłoża wzrostowego, co skutkuje wynikiem o kilka JTK/m3 wyższym od faktycznego stężenia zanieczyszczeń. Jakie to zjawisko?
Oblicz stężenie glukozy w surowicy krwi, jeżeli absorbancja tej próby wynosi 0,350, a wzorzec o stężeniu 0,2 mg/ml wykazuje absorbancję 0,120.
Użyj wzoru:$$ \text{stężenie glukozy [mg/ml]} = \frac{A_p}{A_w} \cdot c_w $$gdzie:
\( A_p \) - absorbancja próbki
\( A_w \) - absorbancja wzorca
\( c_w \) - stężenie wzorca [mg/ml]
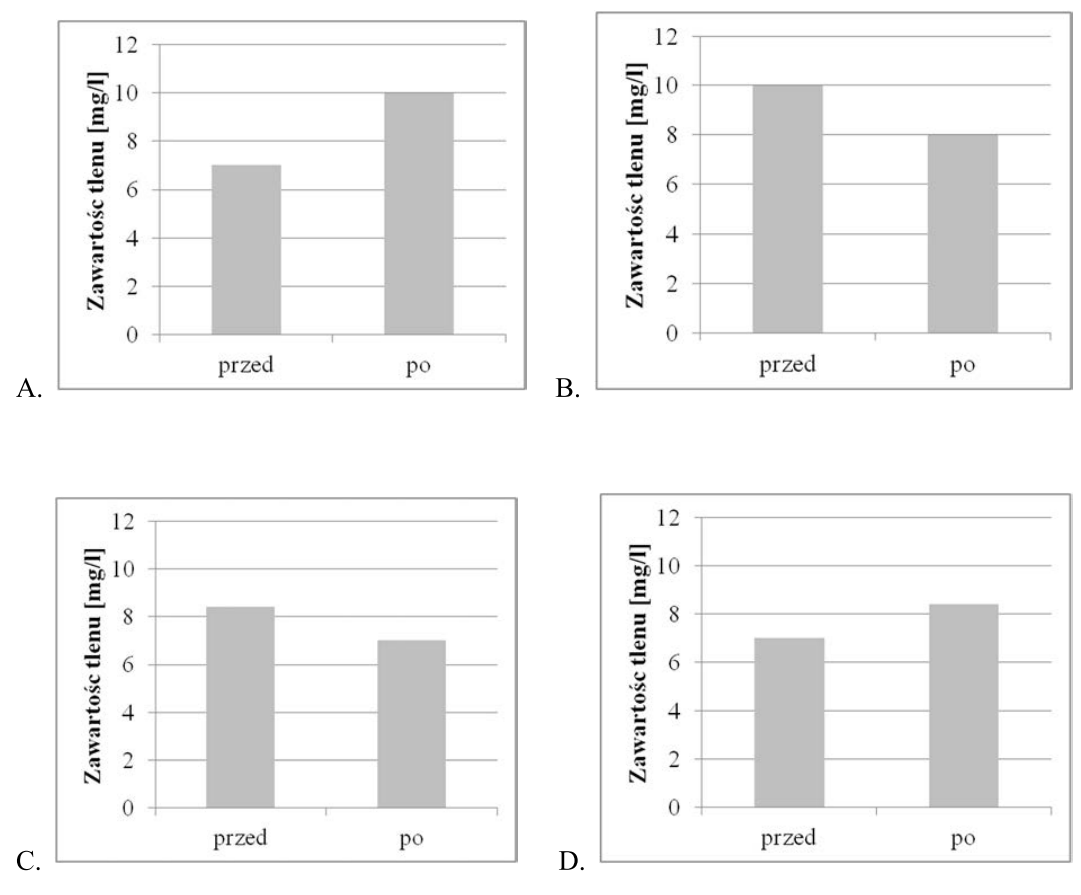
Badaniom poddano wodę z akwarium przed napowietrzaniem i po napowietrzaniu. Wiadomo, że zawartość tlenu w wodzie powinna wzrosnąć o 20%. Który z wykresów obrazuje wyniki tych badań?
Ilościowa analiza polegająca na dodawaniu równoważnej ilości roztworu odczynnika miareczkującego oraz precyzyjnym pomiarze jego objętości to analiza
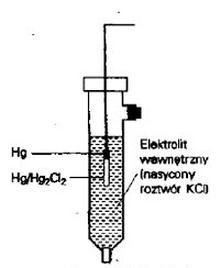
Który rodzaj elektrody odniesienia przedstawiono na rysunku?
Z analizy danych zawartych w tabeli wynika, że
| Tabela. Rodzaj paliwa stałego, zawartość węgla pierwiastkowego i wartość opałowa | ||||
|---|---|---|---|---|
| Rodzaj paliwa | Torf | Węgiel brunatny | Węgiel kamienny | Antracyt |
| Zawartość C, % | 55 – 63 | 63 – 76 | 80 – 90 | 93 – 98 |
| Wartość opałowa, MJ/kg | 21 – 24 | 26 – 32 | 30 – 35 | 36 |
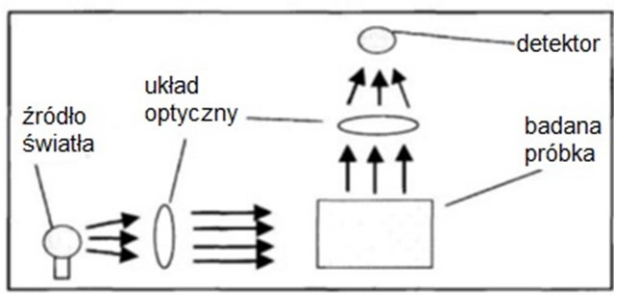
Na schemacie przedstawiono bieg promieni świetlnych
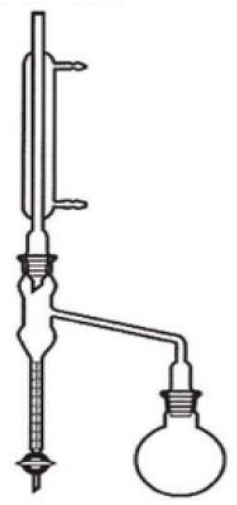
Zawartość wody w produktach spożywczych można oznaczyć za pomocą przedstawionego na rysunku aparatu Deana-Starka metodą
Analizując próbkę wody powierzchniowej stwierdzono, że zawartość azotanów wynosi 4,5 mg/dm3, siarczanów 120 mg/dm3, a stężenie jonów chlorkowych 180 mg/dm3. Na podstawie danych zawartych w tabeli wskaż klasę czystości wody, z której została pobrana próbka.
| Wartości graniczne wskaźników jakości wody w klasach jakości wód powierzchniowych | |||||
|---|---|---|---|---|---|
| Wskaźnik [mg/dm³] | I klasa czystości | II klasa czystości | III klasa czystości | IV klasa czystości | V klasa czystości | Wartości dopuszczalne |
| azotany | 5,0 | 15,0 | 25,0 | 50,0 | >50,0 |
| siarczany | 100 | 150 | 250 | 300 | > 300 |
| chlorki | 100 | 200 | 300 | 400 | > 400 |
Określenie miedzi w postaci czystego osadu pierwiastka przeprowadza się w trakcie analizy
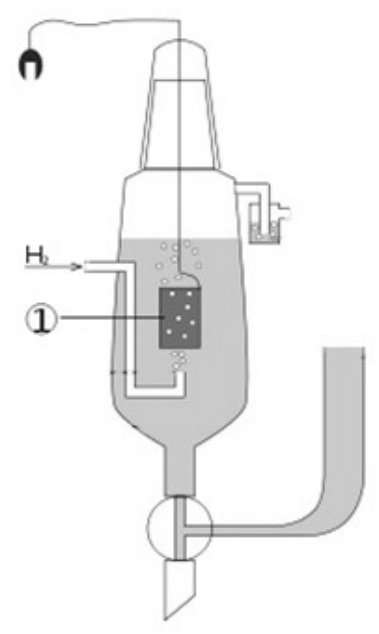
Na schemacie przedstawiającym elektrodę wodorową, cyfrą 1 oznaczono
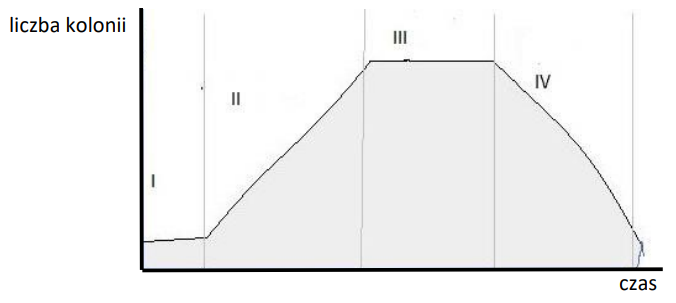
Na wykresie przedstawiającym krzywą wzrostu bakterii, cyfrą IV oznaczono fazę
Dokładność metody definiowana jest na podstawie ustalonej wartości
Ezy oraz igły stosowane w mikrobiologii należy wyjaławiać
W warunkach neutralnych manganian(VII) potasu ulega redukcji do
Reakcja ksantoproteinowa umożliwia identyfikację aminokwasu, który zawiera w swojej budowie
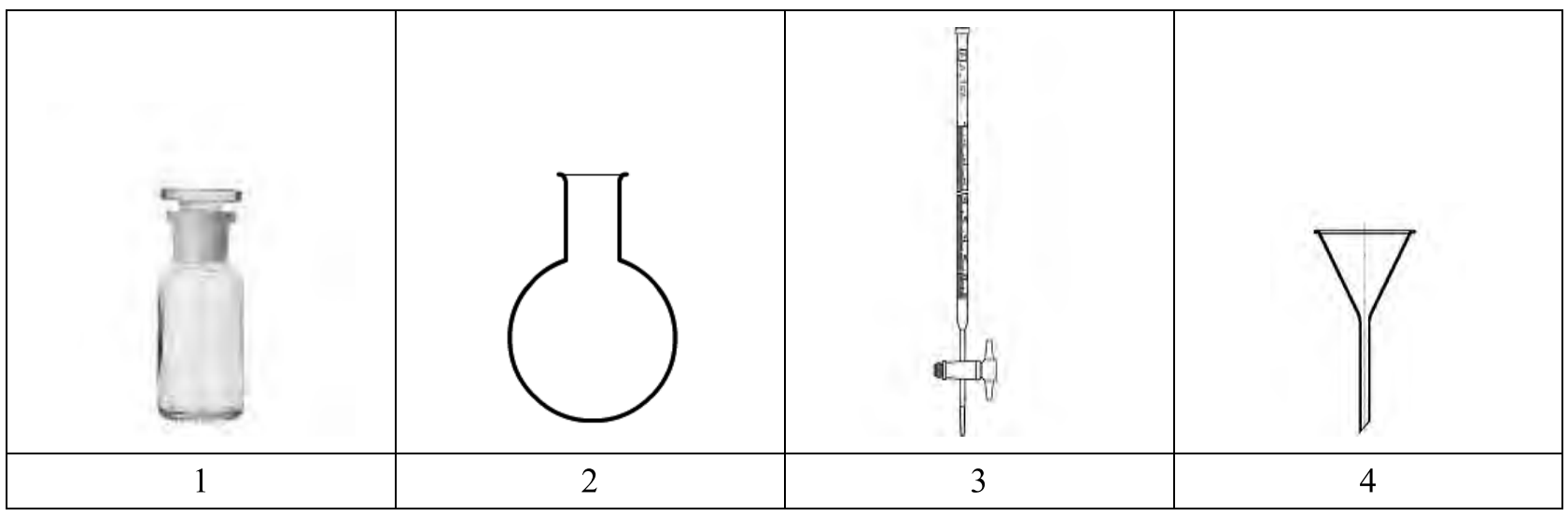
Korzystając z rysunków zamieszczonych w tabeli, wybierz zestaw sprzętu potrzebnego do oznaczania CO2 w wodach powierzchniowych metodą miareczkową.
Określ typ destylacji, który polega na przemianie składnika mieszaniny substancji organicznych w stan pary w temperaturze niższej od jego temperatury wrzenia.
Zjawisko polegające na przepuszczaniu rozpuszczalnika przez membranę półprzepuszczalną z roztworu o wyższym stężeniu do roztworu o niższym stężeniu substancji rozpuszczonej określa się mianem
Na rysunku przedstawiono wykonanie analizy metodą
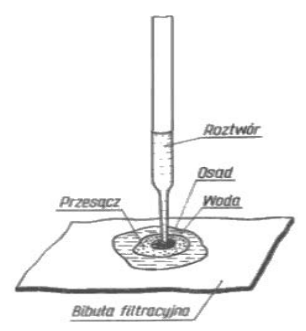
Do oceny kwasowości mleka wykorzystuje się metodę miareczkowania
Jakie aspekty nie są objęte badaniami organoleptycznymi olejów rafinowanych?
Jednym z kroków w procesie przygotowania preparatu mikrobiologicznego w stanie żywym jest
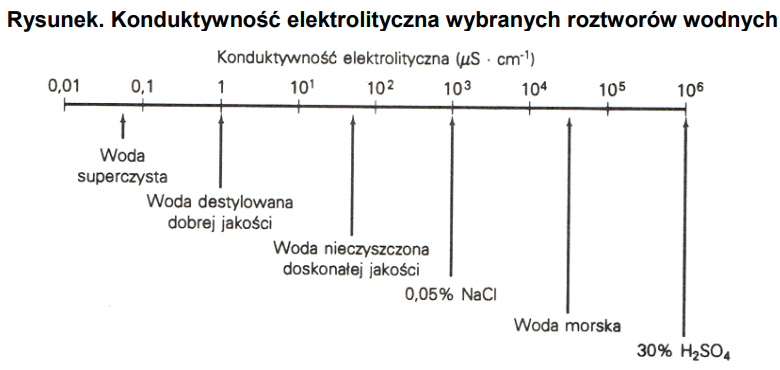
Konduktywność elektrolityczna wody destylowanej stosowanej w laboratorium chemicznym wynosi 0,001 mS cm-1. Z analizy danych przedstawionych na rysunku wynika, że woda ta jest