Pytanie 1
Sprzyja tworzeniu osadów grubokrystalicznych w czystszej formie oraz umożliwiających łatwiejsze sączenie
Wynik: 28/40 punktów (70,0%)
Wymagane minimum: 20 punktów (50%)
Sprzyja tworzeniu osadów grubokrystalicznych w czystszej formie oraz umożliwiających łatwiejsze sączenie
W jakich instrumentalnych metodach optycznych wykorzystuje się zjawiska absorpcji oraz rozpraszania promieniowania elektromagnetycznego?
Na ilustracji przedstawiono

Rysunek przedstawia poszczególne etapy wykonania preparatu mikroskopowego utrwalonego. Cyfrą 3 oznaczono
Analityczne mnożniki dla wagowego oznaczania wapnia (M = 40,08 g/mol) w formie CaC2O4 (M = 128,10 g/mol), CaCO3 (M = 100,09 g/mol) oraz CaO (M = 56,08 g/mol) wynoszą odpowiednio
Jakie substancje stosuje się do barwienia preparatów mikroskopowych według metody Grama?
Dla czterech różnych próbek gleb lekkich o odczynie kwaśnym oznaczono zawartość metali w mg/kg suchej masy. Wyniki zestawiono w tabeli:
Graniczne zawartości metali śladowych w powierzchniowej warstwie gleb bardzo lekkich | |||||
|---|---|---|---|---|---|
| Stopień zanieczyszczenia gleb | Zawartość metali w mg/kg suchej masy | ||||
| Pb | Cd | Zn | Cu | Ni | |
| 0 zawartość naturalna | 30 | 0,3 | 50 | 15 | 10 |
| 1 zawartość podwyższona | 70 | 1 | 100 | 30 | 30 |
| 2 słabe zanieczyszczenie | 100 | 2 | 300 | 50 | 50 |
| 3 średnie zanieczyszczenie | 500 | 3 | 700 | 150 | 100 |
| 4 silne zanieczyszczenie | 2500 | 5 | 3000 | 300 | 400 |
| 5 bardzo silne zanieczyszczenie | >2500 | >5 | >3000 | >300 | >400 |
| Metal | Próbka 1. | Próbka 2. | Próbka 3. | Próbka 4. |
|---|---|---|---|---|
| Pb | 180,0 | 15,0 | 25,0 | 29,0 |
| Cd | 1,6 | 0,3 | 0,2 | 0,6 |
| Zn | 40,0 | 55,5 | 48,0 | 37,0 |
| Cu | 328,0 | 25,0 | 8,0 | 56,0 |
| Ni | 135,0 | 8,0 | 8,0 | 19,0 |
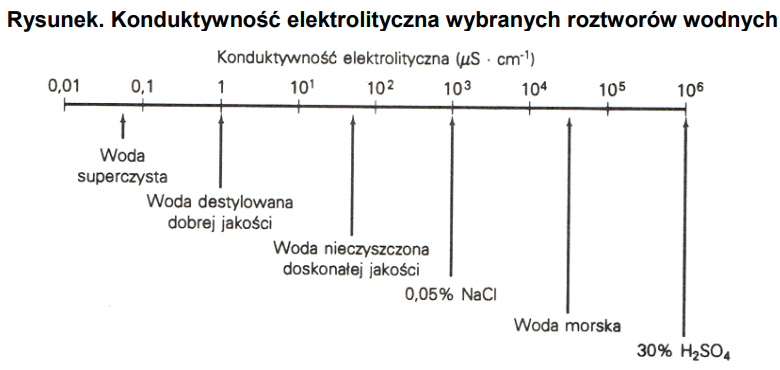
Konduktywność elektrolityczna wody destylowanej stosowanej w laboratorium chemicznym wynosi 0,001 mS cm-1. Z analizy danych przedstawionych na rysunku wynika, że woda ta jest
Przy separacji osadu z roztworu za pomocą wirówki laboratoryjnej istotne jest, aby rotor wirówki
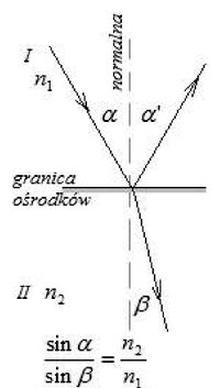
Na rysunku przedstawiono graficzną interpretację zależności wynikających z prawa
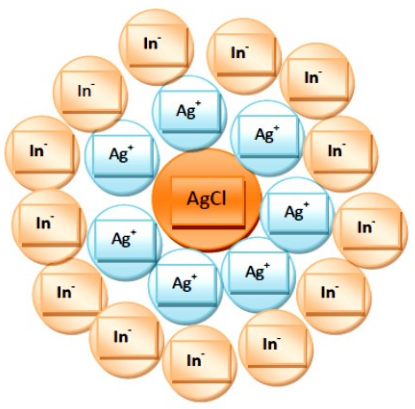
Reakcja jonu Ag+ z substancją pełniącą rolę odczynnika grupowego, 4g+ + Cl- —> AgCl ↓, jest typowa dla kationów z grupy
Wymaganie chemiczne na tlen ChZT określa ilość
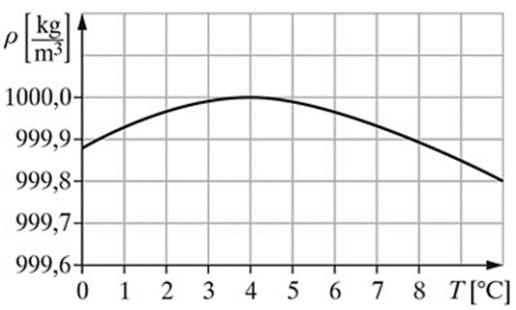
Na podstawie przedstawionego na rysunku wykresu zależności gęstości wody od temperatury, określ w jakiej temperaturze gęstość wody wynosi 1 g/cm3.
Proces stapiania substancji z perłą fosforanową lub boraksową realizuje się
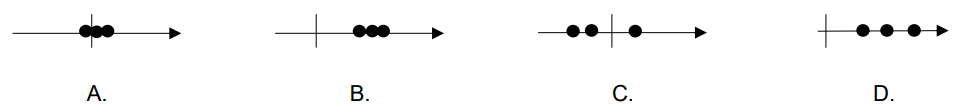
Na którym rysunku przedstawiono schemat metody dokładnej i nieprecyzyjnej?
Reakcja: MnO4- + 8H+ + 5e- → Mn2+ + 4H2O jest wykorzystywana w metodzie analizy jakościowej, określanej jako
W tabeli przedstawiono charakterystykę
| Charakterystyka wybranych metod optycznych stosowanych w analizie instrumentalnej | ||
|---|---|---|
| Metoda | Obserwowane zjawisko | Pomiar |
| 1 | załamanie światła | współczynnik załamania światła padającego na powierzchnię próbki |
| 2 | skręcanie płaszczyzny światła spolaryzowanego | kąt skręcenia płaszczyzny polaryzacji światła |
| 3 | rozproszenie promieniowania | natężenie wiązki światła rozproszonego wychodzącego z kuwety pomiarowej |
W badaniach dotyczących kinetyki hydrolizy sacharozy wykorzystuje się mierzenie aktywności optycznej cukrów, które określa się
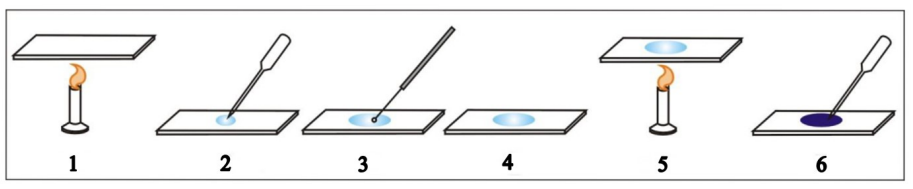
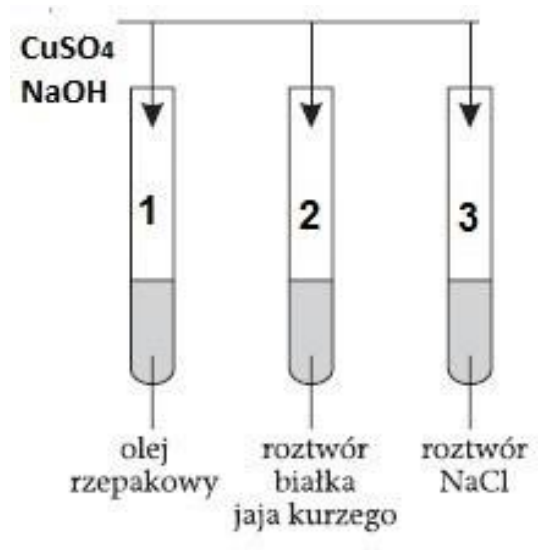
Na podstawie zamieszczonego schematu ilustrującego przeprowadzone badania wskaż, jaką barwę przyjmie roztwór w probówce oznaczonej numerem 2.
Właściwością jakościową produktów technologicznych jest
W badanym powietrzu zawartość mikroorganizmów wyniosła 33,33 w 10 dm3. Zgodnie z zamieszczonymi normami powietrze takie uważa się za
| Stopień zanieczyszczenia | Ogólna liczba bakterii w 1 m3 |
|---|---|
| Niezanieczyszczone | poniżej 1000 |
| Średnio zanieczyszczone | od 1000 do 3000 |
| Silnie zanieczyszczone | powyżej 3000 |
Na schemacie przedstawiono mechanizm działania wskaźników
Woda pobrana do analizy mikrobiologicznej została rozcieńczona w proporcji 1:1000. Z uzyskanej mieszanki pobrano 0,1 ml, który następnie umieszczono na szalce z pożywką. Po hodowli na szalce zaobserwowano 10 jtk. Jakie było stężenie bakterii w analizowanej wodzie?
Metoda analityczna opierająca się na pomiarze kąta rotacji płaszczyzny światła spolaryzowanego to
Wskaźników używanych w oznaczeniach kompleksometrycznych nie obejmuje
Jak nazywa się część białkowa enzymu?
W dwóch niezidentyfikowanych probówkach znajdują się roztwory: w jednej - glukozy, a w drugiej - sacharozy. Jakiego odczynnika należy użyć, aby rozpoznać glukozę?
Gdzie wykorzystuje się efekt Tyndalla?
Stosunek masy proszku luźno nasypanego do objętości, którą ten proszek zajmuje, definiuje gęstość
Aby zmierzyć kąt skręcenia płaszczyzny światła spolaryzowanego przechodzącego przez analizowaną substancję, należy zastosować metodę
Zjawisko opisane w zamieszczonej informacji to
| Jeżeli w wodzie zostanie rozpuszczona α-D-glukopiranoza, to roztwór tuż po rozpuszczeniu wykazuje skręcalność właściwą [α]D = +112,2°, lecz w miarę upływu czasu skręcalność ta stopniowo spada do wartości charakterystycznej w stanie równowagi, mianowicie [α]D = +52,7° |
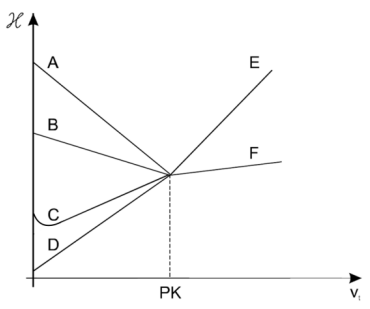
Zawartość kwasu octowego oznaczano alkacymetrycznie, mierząc zmiany przewodnictwa właściwego mieszaniny reakcyjnej w wyniku dodawania roztworu NaOH. Przebieg miareczkowania przedstawiają linie
Oznaczono LZ i LJ dla czterech różnych próbek tłuszczów. Wyniki zestawiono w tabeli:
Na podstawie zamieszczonych danych o liczbach właściwych wybranych tłuszczów wskaż próbkę, którą stanowi olej rzepakowy.
| Liczby właściwe wybranych tłuszczów | ||
|---|---|---|
| Rodzaj tłuszczu | Liczba zmydlania (LZ) mg KOH / g tłuszczu | Liczba jodowa (LJ) g I₂ / 100 g tłuszczu |
| Olej lniany | 187 – 197 | 169 – 192 |
| Olej sojowy | 188 – 195 | 114 – 138 |
| Olej rzepakowy | 167 – 179 | 94 – 106 |
| Tran wielorybi | 170 – 202 | 102 – 144 |
| Masło krowie | 218 – 245 | 25 – 38 |
| Smalec wieprzowy | 193 – 200 | 46 – 66 |
| Próbka | Liczba zmydlania (LZ) | Liczba jodowa (LJ) |
|---|---|---|
| 1 | 190 | 140 |
| 2 | 171 | 99 |
| 3 | 194 | 105 |
| 4 | 195 | 60 |
W trakcie mikrobiologicznych analiz żywności przed posiewem konieczne jest dokonanie rozcieńczenia próbki. W tym celu po dokładnym wymieszaniu badanego płynu pobiera się 10 cm3 za pomocą jałowej pipety, umieszcza w kolbie z 90 cm3 płynu rozcieńczającego i starannie miesza. Następnie z pierwszego rozcieńczenia przenosi się 1 cm3 do probówki, wzbogaconej o 9 cm3 płynu rozcieńczającego. W ten sposób uzyskuje się rozcieńczenie
Gęstość granulatów tworzyw sztucznych można określić przy użyciu
Aby rozpuścić próbkę mosiądzu, należy zastosować kwas
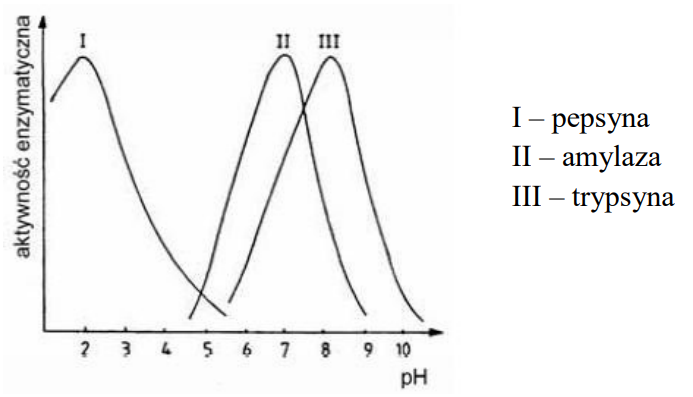
Na wykresie przedstawiono zależność aktywności enzymów od pH. Optimum aktywności amylazy występuje przy pH
W dwóch nieoznakowanych kolbach znajdują się roztwory HCl o różnych stężeniach: 0,1 mol/dm3 oraz 0,01 mol/dm3. Aby odróżnić te roztwory, nie można zastosować
Na podstawie informacji zamieszczonych w tabeli wskaż wzór związku, który wytrąci się w postaci osadu.
| Badany kation | Odczynnik grupowy | NaOH | Barwienie płomienia |
|---|---|---|---|
| Mg2+ | brak | biały osad | |
| K+ | brak | fiołkowy | |
| Na+ | brak | żółty |
Jakim wskaźnikiem posługujemy się w argentometrycznym oznaczaniu chlorków w roztworze soli fizjologicznej?