Pytanie 1
Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest
Wynik: 28/40 punktów (70,0%)
Wymagane minimum: 20 punktów (50%)
Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest
Jaka jest moc dawki pochłoniętej w brachyterapii HDR?
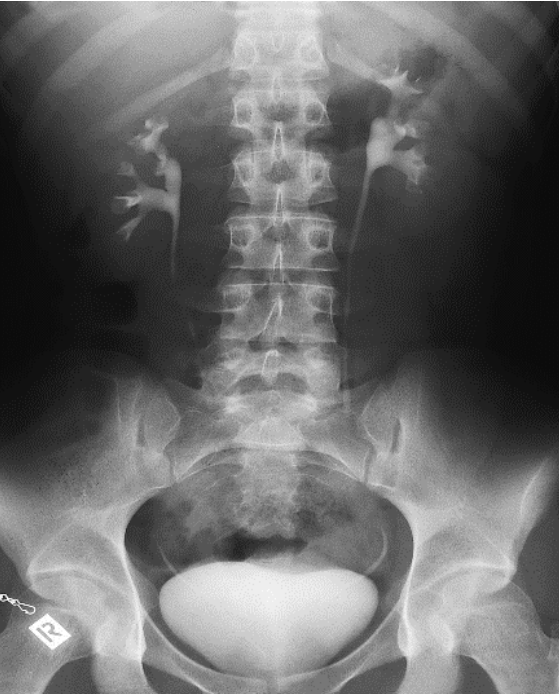
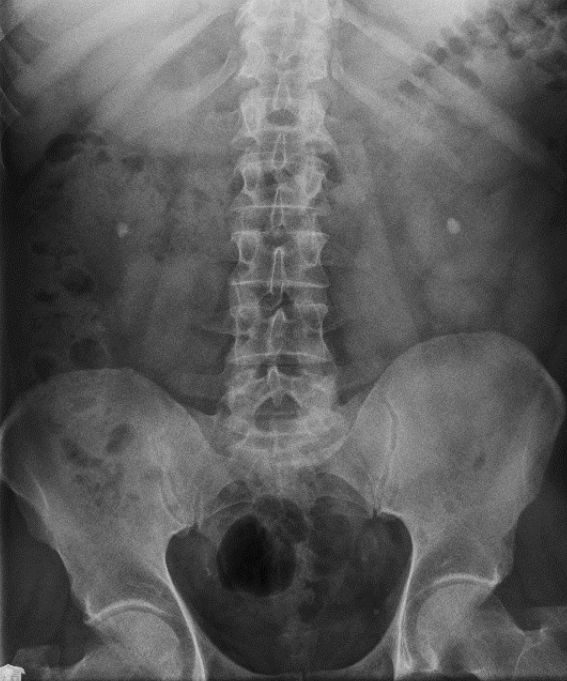
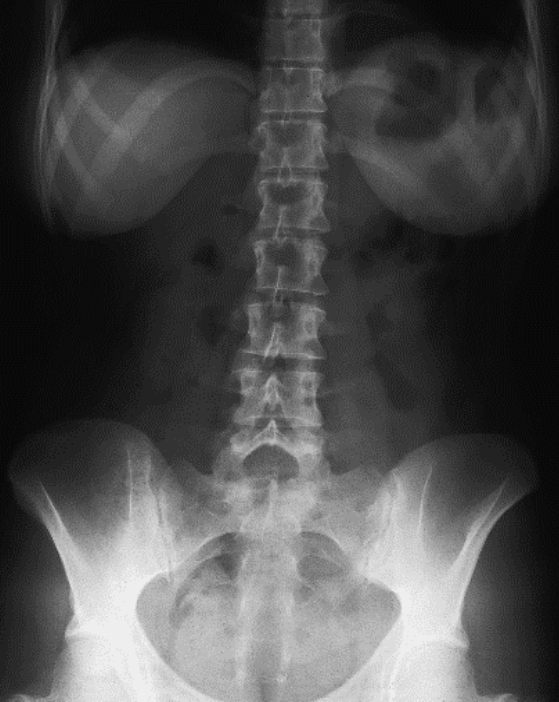
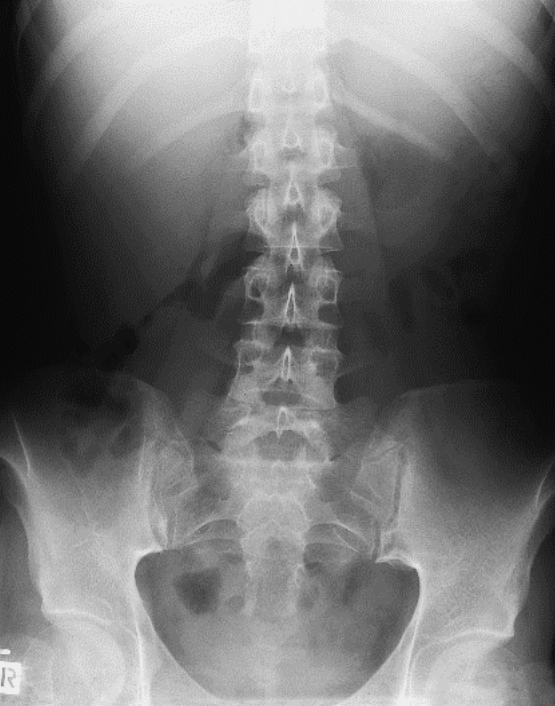
Na którym radiogramie uwidoczniona jest kamica nerkowa?
Droga przewodnictwa powietrznego fali akustycznej przebiega przez
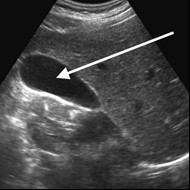
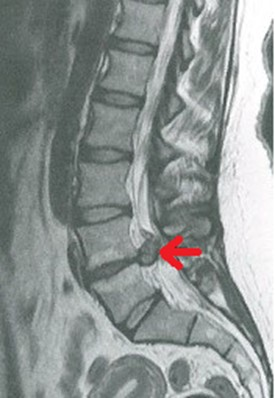
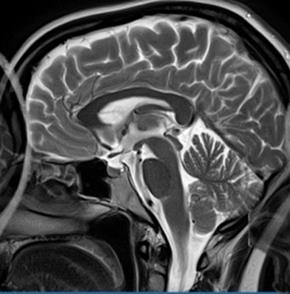
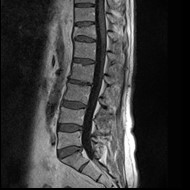
Na obrazie MR kręgosłupa lędźwiowego strzałką wskazano
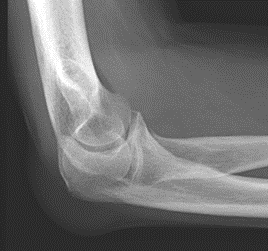
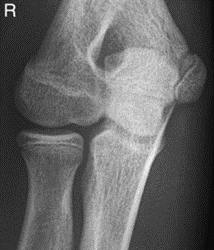
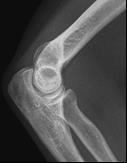
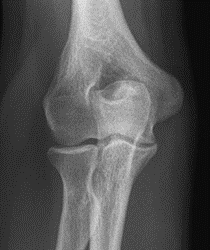
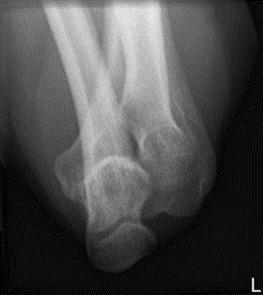
Które zdjęcie RTG stawu łokciowego zostało wykonane w projekcji skośnej w rotacji zewnętrznej?
W brachyterapii MDR stosowane są dawki promieniowania
W ultrasonografii występuje zależność:
Do zadań technika elektroradiologa w pracowni hemodynamicznej należy
Promieniowanie jonizujące pośrednio to
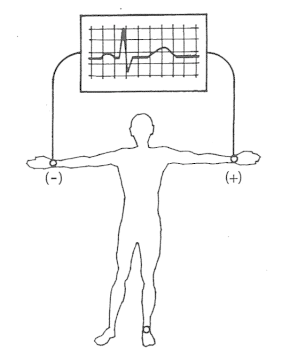
Które odprowadzenie elektrokardiograficzne przedstawiono na ilustracji?
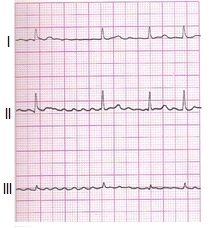
Zamieszczone badanie elektrokardiograficzne wykazało u pacjenta
Standardowe badanie urografii polega na podaniu pacjentowi środka kontrastującego
Który środek ochrony radiologicznej pacjenta należy zastosować podczas wykonywania zdjęcia bocznego kręgosłupa szyjnego?
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
Zgodnie z procedurą wzorcową w badaniu MR należy ułożyć pacjenta na brzuchu do diagnostyki
Obszary napromieniania w technice IMRT w trakcie wykonywania zabiegu radioterapeutycznego wyznacza
W radioterapii hadronowej leczenie odbywa się przy użyciu
Ligand stosuje się
Który radioizotop jest stosowany w scyntygrafii perfuzyjnej mózgu?
W ułożeniu do rentgenografii AP stawu kolanowego promień główny pada
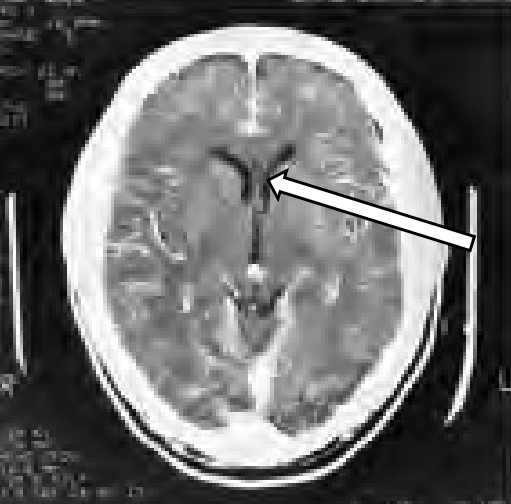
Którą strukturę anatomiczną oznaczono na skanie TK głowy?
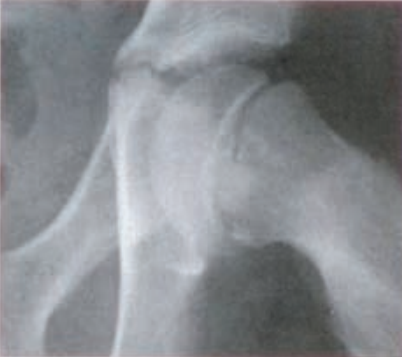
Na rentgenogramie przedstawione jest złamanie Saltera-Harrisa typu
Podczas wykonywania zdjęć wewnątrzustnych zębów górnych linia Campera powinna przebiegać w stosunku do płaszczyzny podłogi
Odprowadzenie EKG mierzące różnicę potencjałów między lewym podudziem a prawym przedramieniem oznacza się jako
W lampie rentgenowskiej promieniowanie X powstaje w wyniku hamowania
Diagnozowanie metodą PET oparte jest na zjawisku
Celem radioterapii paliatywnej nie jest
HRCT (high-resolution computed tomography) jest metodą obrazowania TK
Wskaż przyczynę powstania artefaktu widocznego na obrazie MR.
Skrótem HRCT (High Resolution Computed Tomography) określa się tomografię komputerową
Którą ochronę radiologiczną należy zastosować podczas wykonywania zdjęcia rentgenowskiego przeglądowego klatki piersiowej u pacjentki w okresie rozrodczym?
W badaniu EKG elektrodę przedsercową V4 należy umocować
Którą strukturę anatomiczną i w jakiej projekcji uwidoczniono na radiogramie?
Podczas wykonywania zdjęcia rentgenowskiego klatki piersiowej w celu ochrony radiologicznej pacjenta należy zastosować
Na obrazie uwidoczniono złamanie kompresyjne kręgu
Teleterapia polega na napromienowaniu
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
W badaniu audiometrycznym rezerwa ślimakowa to odległość między krzywą
Na obrazie ultrasonograficznym jamy brzusznej strzałką wskazano