Pytanie 1
W brachyterapii MDR stosowane są dawki promieniowania
Wynik: 17/40 punktów (42,5%)
Wymagane minimum: 20 punktów (50%)
W brachyterapii MDR stosowane są dawki promieniowania
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Gadolin jako dożylny środek kontrastowy stosowany w MR powoduje
Obszary napromieniania w technice IMRT w trakcie wykonywania zabiegu radioterapeutycznego wyznacza
Obrazy DDR są tworzone w trakcie
Jaki jest cel stosowania bolusa w radioterapii?
W brachyterapii MDR stosowane są dawki promieniowania
Brachyterapia polega na napromieniowaniu pacjenta promieniowaniem
W technice napromieniania SSD mierzona jest odległość źródła promieniowania od
W scyntygrafii wykorzystywane są głównie radioizotopy emitujące promieniowanie
Który detektor w radiografii wymaga laserowego czytnika obrazu?
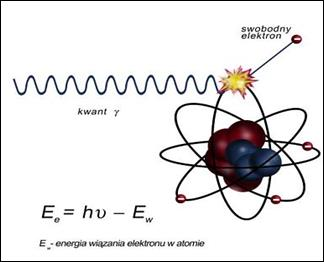
Na ilustracji przedstawiono zjawisko
Jakie wymagania techniczne muszą spełniać aparaty terapeutyczne stosowane w zakładach brachyterapii, służące bezpośrednio do napromieniania pacjenta metodą zdalnego wprowadzania źródeł promieniotwórczych?
W pozytonowej tomografii emisyjnej PET zostaje zarejestrowane promieniowanie powstające podczas
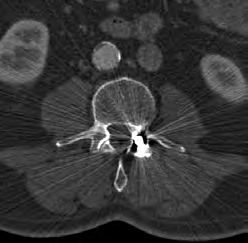
Który artefakt jest widoczny na skanie tomografii komputerowej?
W sekwencji echa spinowego obraz T2-zależny uzyskuje się przy czasie repetycji TR
W ultrasonografii występuje zależność:
Jakie źródła promieniowania stosowane są w brachyterapii?
W celu maksymalnego ograniczenia dawki promieniowania badanie rentgenowskie u dzieci należy wykonać
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
SPECT to
W leczeniu izotopowym tarczycy należy podać
Który parametr ekspozycji ma decydujący wpływ na kontrast obrazu rentgenowskiego?
W diagnostyce metodą rezonansu magnetycznego biorą udział
Radioizotopowa terapia medycyny nuklearnej polega na wprowadzeniu do tkanek lub narządów radiofarmaceutyku
W której technice brachyterapii stosuje się źródła promieniowania o mocy dawki 2-12 Gy/h?
Który radioizotop jest emiterem promieniowania alfa?
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
W obrazowaniu MR wykorzystuje się moment magnetyczny
Planowany obszar napromieniania PTV obejmuje
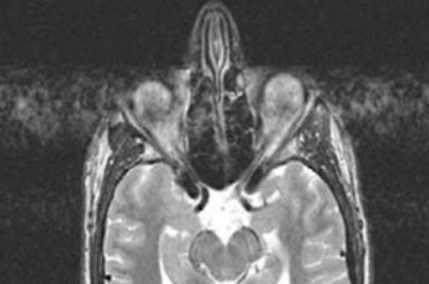
Co jest przyczyną artefaktu widocznego na obrazie MR?
Fala głosowa rozchodzi się
Która sekwencja obrazowania MR wykorzystuje impulsy RF o częstotliwości rezonansowej tłuszczu do tłumienia sygnału pochodzącego z tkanki tłuszczowej?
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz
Do czego służy do symulator rentgenowski wykorzystywany w procesie radioterapii?
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
Hiperfrakcjonowanie dawki w radioterapii oznacza napromieniowywanie pacjenta
Czas repetycji w obrazowaniu metodą rezonansu magnetycznego to
Hiperfrakcjonowanie dawki w teleradioterapii polega na napromienianiu 2 do 3 razy dziennie dawką frakcyjną