Pytanie 1
W makroanalizie wykorzystuje się próbki o ciężarze
Wynik: 20/40 punktów (50,0%)
Wymagane minimum: 20 punktów (50%)
W makroanalizie wykorzystuje się próbki o ciężarze
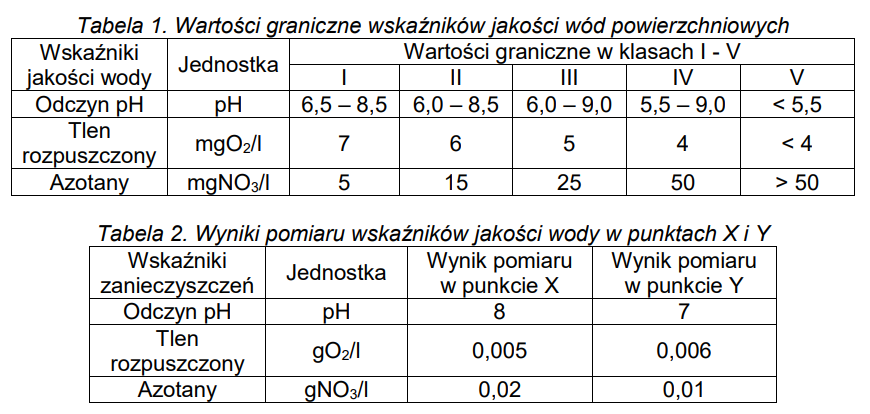
Na podstawie danych w tabelach 1-2 zawierających wartości graniczne wskaźników jakości wody i uzyskane wyniki pomiarowe oceń jakość wody w punktach pomiarowych X i Y, określając jej klasę.
W Polsce ustalono normy dla pyłów PM10 na trzech poziomach (dobowych):
- poziom dopuszczalny 50 ug/m3 - oznacza, że jakość powietrza jest niezadowalająca, jednak nie powoduje poważnych skutków dla zdrowia ludzkiego.
- poziom informowania 200 ug/m3 - wskazuje, że jakość powietrza jest zła i konieczne jest ograniczenie aktywności na świeżym powietrzu, ponieważ norma została przekroczona czterokrotnie.
- poziom alarmowy 300 ug/m3 - wskazuje, że jakość powietrza jest bardzo zła, norma została przekroczona sześciokrotnie i należy zdecydowanie ograniczyć przebywanie na zewnątrz, a najlepiej pozostać w domu, zwłaszcza osoby z chorobami.
Na stacji Monitoringu Środowiska dokonano pomiarów zanieczyszczenia powietrza pyłem PM10, uzyskując średnią dobową 0,25 mg/m3. Z przeprowadzonej analizy wynika, że
W ramce scharakteryzowano odczynniki
| Łączą się z danym jonem ubocznym, wiążąc go w trwałe zespoły i tym samym wyłączają go z udziału w roztworze lub obniżają znacznie jego stężenie. |
Jaką objętość roztworu EDTA zużyto do odmiareczkowania jonów magnezu podczas analizy przeprowadzonej zgodnie z zamieszczoną procedurą?
| Procedura Współoznaczanie wapnia i magnezu w wodach naturalnych polega na przeprowadzeniu dwóch miareczkowań mianowanym 0,0100 mol/dm3 roztworem EDTA. Pierwsze miareczkowanie przeprowadza się w środowisku buforu amoniakalnego pH = 10 wobec czerni eriochromowej T, jako wskaźnika. Objętość zużytego titranta odpowiada sumie zawartości jonów wapnia i magnezu. Drugie miareczkowanie przeprowadza się w środowisku silnie zasadowym pH=12-13 wobec mureksydu. Objętość użytego titranta zależy od ilości jonów wapnia. Podczas wykonywania oznaczenia zużyto na pierwsze miareczkowanie wobec czerni eriochromowej średnio V1= 20,3 cm3 roztworu EDTA, na drugie oznaczenie wobec mureksydu zużyto średnio V2= 5,4 cm3 tego samego roztworu EDTA. |
Na jakich materiałach wykonuje się podłoża mikrobiologiczne?
W wyniku oznaczenia wagowego otrzymano 0,2451 g tlenku żelaza(III). Ile gramów żelaza zawierała analizowana próbka?
| MFe = 55,845 g/mol, MO = 15,999 g/mol |
Do czego używa się polarymetru?
Do zmiareczkowania próbki roztworu NaOH wykorzystano 10 cm3 roztworu HCl o stężeniu 0,1 mol/dm3. Ile NaOH (M = 40 g/mol) znajdowało się w próbce?
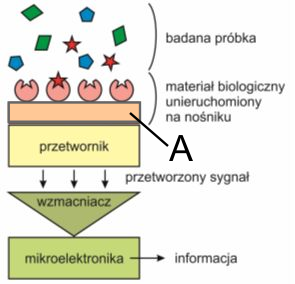
Na zamieszczonym schemacie biosensora literą A oznaczono
Podczas miareczkowania roztworu amoniaku o stężeniu 0,1 mol/dm3 za pomocą roztworu kwasu solnego o stężeniu 0,1 mol/dm3, skok krzywej leży w granicach pH 6,3–4,3. W tym miareczkowaniu jako wskaźnik należy zastosować
| Wskaźnik | Przedział pH |
| Błękit tymolowy | 1,2–2,8 |
| 8,0–9,6 | |
| Oranż metylowy | 3,1–4,4 |
| Czerwień metylowa | 4,2–6,2 |
| Błękit bromotymolowy | 6,7–7,6 |
| Fenoloftaleina | 8,0–9,8 |
| Tymoloftaleina | 9,3–10,5 |
Do kationów trzeciej grupy analitycznej, wytrącanych w formie siarczków roztworem AKT w środowisku amoniakalnym, należą:
| A. | Ni2+, Co2+, Fe2+, Fe3+, Mn2+, Zn2+ |
| B. | Mn2+, Cu2+, Cd2+, Cr3+, Ag+, Zn2+ |
| C. | Fe2+, Mg2+, Pb2+, Al3+, Ca2+ |
| D. | Ba2+, Ca2+, Sr2+ |
Ilość flawonoidów, które wykazują działanie antyoksydacyjne, powinna wynosić dziennie 1000 mg. Oblicz, jak wiele gramów czarnej porzeczki należy zjeść, aby zaspokoić potrzebę na antyoksydanty, wiedząc, że 100 g czarnej porzeczki zawiera 640 mg flawonoidów.
W eksperymencie mającym na celu wykazanie nienasyconego charakteru oleju rzepakowego stosuje się reakcję
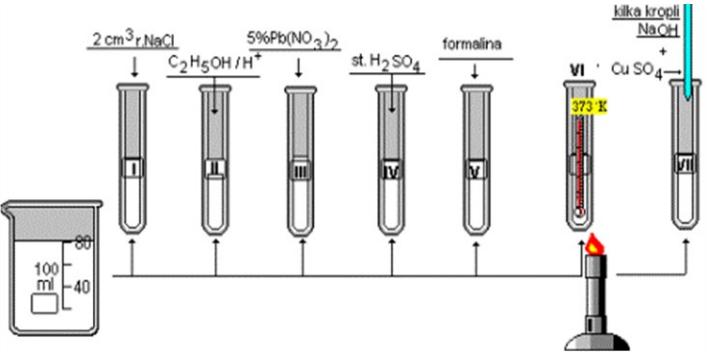
Na rysunku przedstawiono schemat doświadczenia pozwalającego na zbadanie właściwości
Dokładność metody definiowana jest na podstawie ustalonej wartości
Na podstawie informacji zamieszczonych w tabeli wskaż nazwę badanego związku.
| Dodany odczynnik | Obserwacje |
|---|---|
| Cu(OH)₂ | Zawiesina Cu(OH)₂ rozpuściła się, a roztwór przyjął szafirową barwę |
| Cu(OH)₂ | Po ogrzaniu probówki pojawił się ceglastoczerwony osad |
| [Ag(NH₃)₂]⁺ | Na ściankach probówki pojawiło się srebro metaliczne |
Zamieszczony w ramce opis określa liczbę
| Liczba gramów fluorowca, przeliczona na gramy jodu, który w określonych warunkach ulega reakcji addycji do atomów węgla związanych wiązaniem wielokrotnym, zawartych w 100 g badanego tłuszczu. Jest ona proporcjonalna do liczby wiązań wielokrotnych w tłuszczach. |
Formy przetrwalnikowe bakterii nie obejmują
W temperaturze 20°C wyznaczono gęstość i współczynnik załamania światła kwasu butanowego. Wyniki zestawiono w tabeli. Refrakcja molowa kwasu butanowego wynosi
| Gęstość | Współczynnik załamania światła |
|---|---|
| 0,960 g/cm³ | 1,398 |
| RM = n2 - 1 n2 + 2 M d |
| RM – refrakcja molowa, cm3/mol n – współczynnik załamania światła d – gęstość, g/cm3 M – masa molowa, 88 g/mol |
Jaka była zawartość jonów żelaza (II) w oznaczanym roztworze, jeżeli na jego zmiareczkowanie zużyto \( 10 \, \text{cm}^3 \) roztworu \( \text{KMnO}_4 \) o stężeniu \( 0{,}02 \, \text{mol/dm}^3 \)?
Wzór do obliczeń:
$$ m_{Fe} = 5 \cdot c_{mol} \cdot V \cdot M_{Fe} $$
gdzie: \( V \) – objętość roztworu \( \text{KMnO}_4 \) zużyta w czasie miareczkowania [\( \text{dm}^3 \)], \( M_{Fe} = 56 \, \text{g/mol} \), \( c_{mol} \) – stężenie molowe roztworu \( \text{KMnO}_4 \) [\( \text{mol/dm}^3 \)]
Część opisu skutków analizy
(...) generuje kation jednowartościowy, a sole powstałe z tym kationem to w przeważającej mierze substancje trudnorozpuszczalne. Większość jego soli jest bezbarwna. Ten bezbarwny jon ma zdolność do tworzenia jonów kompleksowych, na przykład z tiosiarczanem sodowym. Związki tego kationu są wrażliwe na światło (ciemnieją pod jego działaniem), dlatego powinny być przechowywane w pojemnikach z ciemnego szkła (...) Z opisu wynika, że w analizowanym surowcu jakościowo oznaczano kation
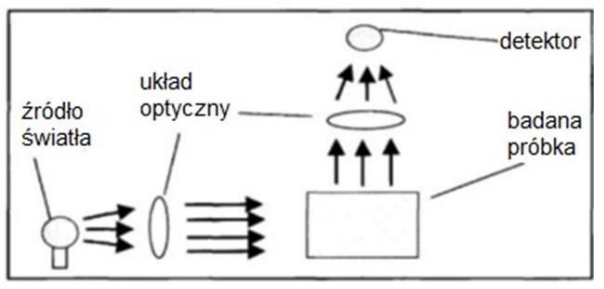
Na ilustracji przedstawiono bieg promieni świetlnych
Na wykresie przedstawiono krzywą miareczkowania
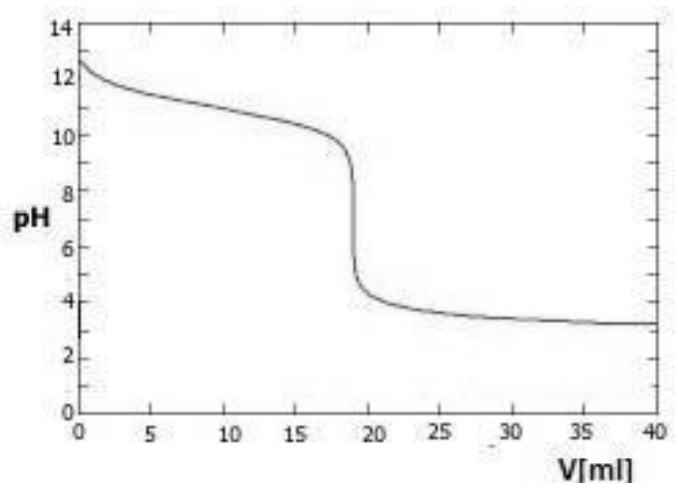
W procedurze analitycznej zapisano. Ile wynosi zawartość procentowa Na2B4O7 • H2O w badanej próbce boraksu, jeżeli na zmiareczkowanie 0,3 g próbki zużyto 15,4 cm3 roztworu NaOH?
| 1 cm3 roztworu NaOH o stężeniu 0,1 mol/dm3 odpowiada 19,07 mg tetraboranu sodu Na2B4O7·H2O |
Podstawą klasyfikacji kationów w analizie jakościowej jest wydzielanie trudno rozpuszczalnych osadów?
Aby wykonać roztwór mosiądzu (stop miedzi), jaki kwas należy zastosować?
Jakim czynnikiem dokonuje się sterylizacji w autoklawie?
Posługując się wagą techniczną o dokładności 0,1 g, odważono trzy próbki stopu żelaza. Masy stopów żelaza wynosiły odpowiednio:
Próbka 1 — masa 100 g Próbka 2 — masa 10 g Próbka 3 — masa 1 g Obliczone błędy względne oznaczenia wynoszą:
| Próbka 1 | Próbka 2 | Próbka 3 | |
|---|---|---|---|
| A. | 0,1% | 1% | 10% |
| B. | 10% | 1% | 0,1% |
| C. | 1% | 1% | 1% |
| D. | 0,1% | 0,1% | 0,1% |
Który nawóz, spośród wymienionych w tabeli, zawiera najwięcej azotu azotanowego?
| Tabela. Zawartość składnika czynnego w nawozach azotowych | |
|---|---|
| Nawóz | Zawartość składników, % |
| Saletra potasowa | N – 13,5% |
| Saletra magnezowa | N – 10,8% |
| Saletra amonowa | N – 34% (NH4+ – 17%, NO3- – 17%) |
| Saletra wapniowa | N – 14,5% |
| Siarczan amonu | N – 21% |
| Mocznik | N – 46% |
Jaka jest wartość stałej Michaelisa, przy której enzym ma największe powinowactwo do substratu?
Aby zniwelować oddziaływanie wody obecnej w próbce materiału sypkiego na rezultat analizy składu, próbkę należy poddać
Na jakość paliwa nie ma wpływu
Badanie organoleptyczne wody przeznaczonej do ludzkiego spożycia obejmuje określenie
Które urządzenie przedstawiono na rysunku?

Badanie obecności pałeczek Salmonella w produktach spożywczych klasyfikuje się jako analiza
Na rysunku przedstawiono schemat blokowy
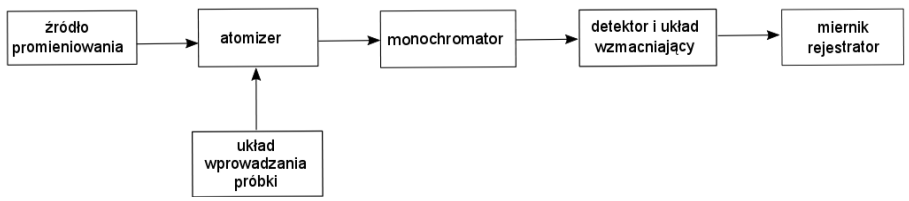
Jakie właściwości mierzą wiskozymetry?
Jakie jednostki stosuje się do określenia tzw. indeksu nadmanganianowego, który symbolicznie reprezentuje ilość związków organicznych w wodzie pitnej?
Wartość pH punktu równoważnikowego w miareczkowaniu mocnych kwasów przy użyciu mocnych zasad wynosi