Pytanie 1
Piktogram nie jest konieczny dla
Wynik: 27/40 punktów (67,5%)
Wymagane minimum: 20 punktów (50%)
Piktogram nie jest konieczny dla
Przy transporcie próbek wody zaleca się, aby próbki były
Wskaż, do jakiego typu należą zamieszczone równania reakcji.
| I. 2 Mg + O2 → 2 MgO |
| II. 2 KMnO4 → K2MnO4 + MnO2 + O2 |
| III. BaCl2 + H2SO4→ BaSO4 + 2 HCl |
Podstawowa substancja w analizie miareczkowej charakteryzuje się następującymi właściwościami:
Roztwór, który jest dodawany z biurety w formie kropli do roztworu substancji, którą analizujemy, określamy mianem
Na podstawie danych w tabeli próbkę, w której będzie oznaczany BZT, należy przechowywać
| Oznaczany parametr | Rodzaj naczynia do przechowywania | Sposób utrwalania | Dopuszczalny czas przechowywania |
|---|---|---|---|
| barwa | szklane lub polietylenowe | - schłodzenie do temperatury 2-5°C | 24 h |
| fosforany ogólne | szklane lub polietylenowe | - zakwaszenie kwasem siarkowym(VI) - schłodzenie do temperatury 2-5°C | 4 h 48 h |
| BZT | szklane | - schłodzenie do temperatury 2-5°C - przechowywanie w ciemności | 24 h |
| azot azotanowy(V) | szklane lub polietylenowe | - schłodzenie do temperatury 2-5°C - dodanie 2 cm3 chloroformu do 1 dm3 próbki | 24 h 48 h |
W laboratorium chemicznym systemy wodne zazwyczaj oznacza się kolorem zielonym
Jakie roztwory chemiczne powinny być stanowczo pobierane przy włączonym dygestorium?
Etykieta roztworu kwasu azotowego(V) o koncentracji 6 mol/dm3 powinna zawierać nazwę substancji oraz
Jakim kolorem oznacza się instalację gazową w laboratorium analitycznym?
Woda, która została poddana dwukrotnej destylacji, to woda
Do wykonania preparatu według zamieszczonej procedury należy przygotować wagę, łyżeczkę, palnik gazowy, trójnóg, bagietkę, szczypce metalowe oraz
| Procedura otrzymywania tlenku magnezu przez prażenie węglanu magnezu. Odważoną ilość węglanu magnezu ubić dokładnie w tyglu (wcześniej zważonym) i przykryć pokrywką. Początkowo ogrzewać niewielkim kopcącym płomieniem, a następnie gdy tygiel ogrzeje się, ogrzewać silniej w temperaturze czerwonego żaru przez około 20 minut. Po zakończeniu prażenia tygiel odstawić do ostudzenia chroniąc przed wilgocią. Zważyć tygiel z preparatem i obliczyć wydajność. |
Po połączeniu 50 cm3 wody z 50 cm3 alkoholu etylowego, objętość otrzymanej mieszanki jest poniżej 100 cm3. Zjawisko to jest spowodowane
Na etykiecie odważki analitycznej znajduje się napis: Z odważki tej można przygotować
Odważka analityczna azotan(V) srebra(I) AgNO3 0,1 mol/dm3 |
Na podstawie informacji zawartej na pipecie, została ona skalibrowana na
Komora przeszklona w formie dużej szafy, wyposażona w wentylator, która zapobiega wydostawaniu się szkodliwych substancji do atmosfery laboratorium oraz chroni przed pożarami i eksplozjami, to
Laboratoryjny stół powinien być zaopatrzony w instalację gazową oraz
Odlanie cieczy z nad osadu to
Do 200 g roztworu NaOH (M = 40 g/mol) o stężeniu 10 % dodano wodę destylowaną w kolbie miarowej o pojemności 500 cm3 do znaku. Jakie jest stężenie molowe powstałego roztworu?
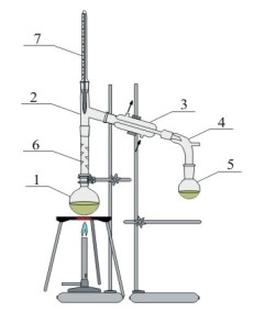
Na rysunku numerem 3 oznaczono
Jakie środki należy zastosować do gaszenia pożaru metali, takich jak magnez, sód czy potas?
Rysunek przedstawia

Które z wymienionych reakcji chemicznych stanowi reakcję redoks?
Roztwór amoniaku o stężeniu 25% nie powinien być trzymany
Aby uzyskać roztwór AgNO3 (masa molowa AgNO3 to 169,8 g/mol) o stężeniu 0,1 mol/dm3, należy rozpuścić w wodzie destylowanej i dopełnić kolbę wodą destylowaną do zaznaczonej kreski.
Metoda przygotowania próbki do badania, która nie jest
Jakie urządzenie wykorzystuje się do określania lepkości płynów?
W standardowym układzie destylacyjnym, który ma ukośną chłodnicę, wykorzystuje się chłodnicę
Między wodorotlenkiem baru a chlorkiem amonu dochodzi do spontanicznej reakcji, która powoduje silne schłodzenie mieszaniny oraz wydobycie się charakterystycznego zapachu amoniaku.
Ba(OH)2(s) + 2 NH4Cl(s) → BaCl2(aq) + 2 H2O(c) + 2 NH3(g) Wskaź, które sformułowanie właściwie wyjaśnia to zjawisko.
nieodwracalnie jej równowagę.
Aby uzyskać sole sodowe fenoli, należy stopić dany fenol z sodą (M = 106 g/mol), stosując 10% nadmiar w porównaniu do ilości stechiometrycznej, według równania:
2 ArOH + Na2CO3 → 2 ArONa + H2O + CO2 Ile sody jest wymagane do reakcji z 7,2 g 2-naftolu (M = 144 g/mol)?
Aby przygotować 500 cm3 roztworu KMnO4 (M = 158 g/mol) o stężeniu 0,02 mol/dm3, ile należy zważyć?
Przedstawiony na rysunku sprzęt służy do

Gdzie należy przechowywać cyjanek potasu KCN?
Odpady, które w przeważającej mierze składają się z osadów siarczków metali ciężkich, nazywa się
Naważkę NaOH o masie 0,0400 g rozpuścić w małej ilości wody, a następnie przelać ten roztwór do kolby miarowej o pojemności 500 cm3 i uzupełnić kolbę miarową wodą do tzw. kreski. Masa molowa NaOH wynosi 40,0 g/mol. Jakie jest stężenie molowe przygotowanego roztworu?
Z etykiety wynika, że dany związek mógł być

W celu rozdrabniania niewielkich ilości bardzo twardego materiału wykorzystuje się moździerze
Próbka laboratoryjna posiadająca cechy higroskopijne powinna być pakowana
Jakie substancje wykorzystuje się do wykrywania obecności jonów chlorkowych w wodzie mineralnej?
Ustalanie miana roztworu polega na