Pytanie 1
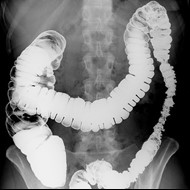
Przedstawiony obraz radiologiczny został zarejestrowany podczas badania jelita
Wynik: 31/40 punktów (77,5%)
Wymagane minimum: 20 punktów (50%)
Przedstawiony obraz radiologiczny został zarejestrowany podczas badania jelita

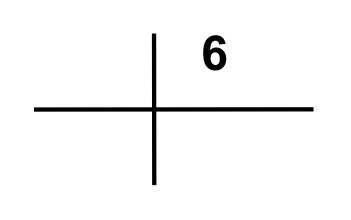
W badaniu EEG w systemie „10-20” elektrody w okolicy skroniowej oznaczone są literą
Pielografia zstępująca umożliwia diagnostykę
Po zakończeniu badania angiograficznego należy zapisać w dokumentacji medycznej pacjenta:
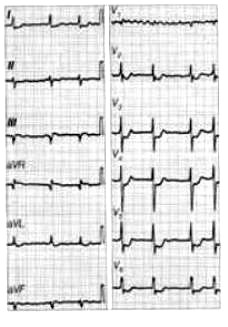
Na elektrokardiogramie uwidoczniono
Kolonoskopia to badanie, które ma na celu ocenę błony śluzowej
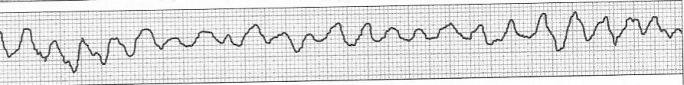
Zamieszczony elektrokardiogram przedstawia
Który radiofarmaceutyk może zostać podany pacjentowi w scyntygrafii perfuzyjnej mózgu?
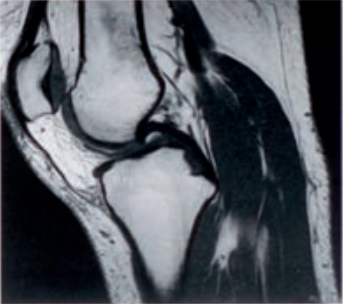
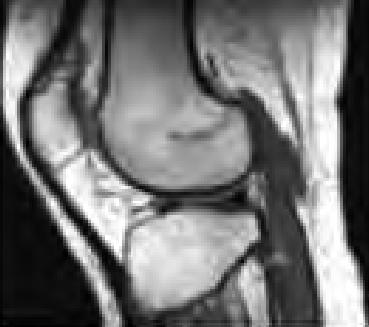
Którą metodę badania zastosowano w obrazowaniu stawu kolanowego?
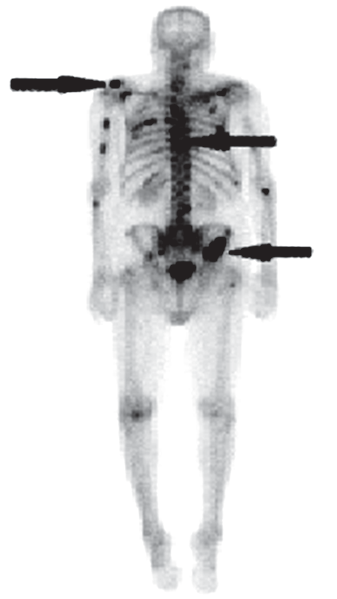
Na scyntygramie kości strzałkami oznaczono ogniska
Jaka jest odległość pomiędzy źródłem promieniowania a powierzchnią ciała pacjenta w technice izocentrycznej radioterapii?
W radioterapii hadronowej leczenie odbywa się przy użyciu
„Ognisko zimne” w obrazie scyntygraficznym określa się jako
Standardowo do wykonania których zdjęć należy zastosować kratkę przeciwrozproszeniową?
Do zdjęcia lewobocznego kręgosłupa lędźwiowo-krzyżowego pacjenta należy ułożyć na boku
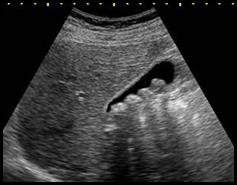
Którą strukturę anatomiczną uwidoczniono na zamieszczonym obrazie USG?
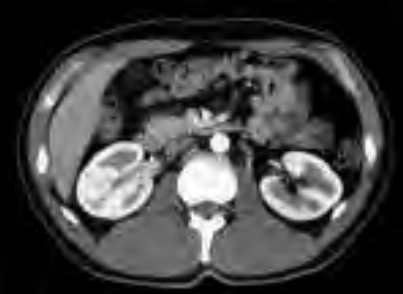
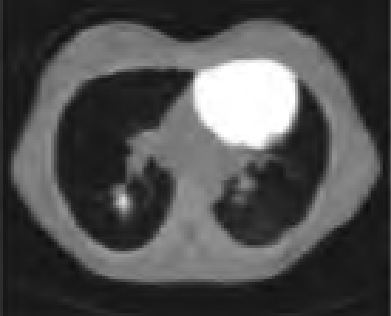
Na którym obrazie zarejestrowano badanie scyntygraficzne?
W badaniu EKG różnice potencjałów pomiędzy lewym podudziem a lewym przedramieniem rejestruje odprowadzenie
Bezwzględnym przeciwwskazaniem do badania spirometrycznego jest
Jak oznacza się w radioterapii obszar tkanek zawierający GTV i mikrorozsiewy w fazie niewykrywalnej klinicznie?
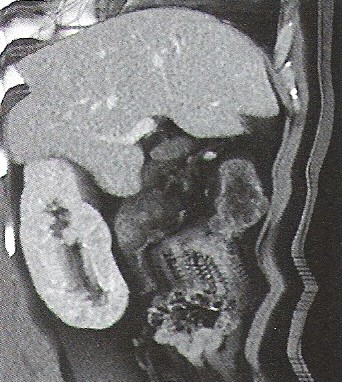
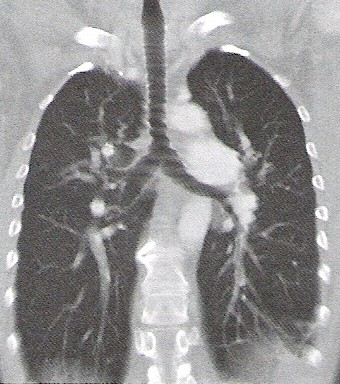
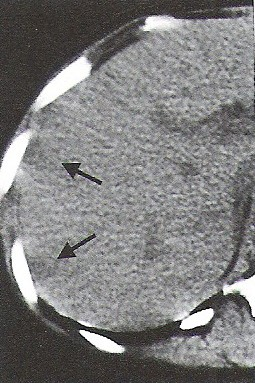
Na którym obrazie TK uwidoczniony jest artefakt spowodowany ruchami oddechowymi pacjenta?

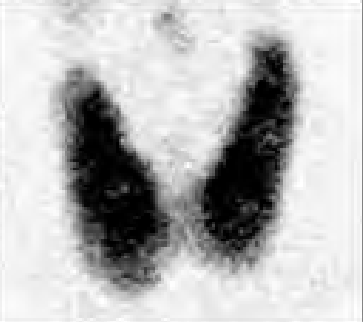
Zdjęcie którego zęba górnego zlecił na skierowaniu lekarz stomatolog?
Osłony na gonady dla osób dorosłych powinny posiadać równoważnik osłabienia promieniowania nie mniejszy niż
W leczeniu izotopowym tarczycy podaje się
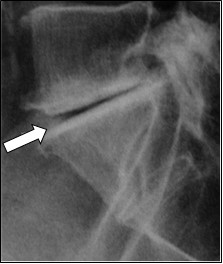
Na rentgenogramie strzałką zaznaczono
W audiometrii badanie polegające na maskowaniu (zagłuszaniu) tonów szumem białym to próba
W której pozycji wykonuje się zdjęcie jamy brzusznej u pacjenta z podejrzeniem perforacji żołądka?
Promieniowanie rentgenowskie jest
Jaki jest cel stosowania bolusa w radioterapii?
Celem radioterapii paliatywnej nie jest
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
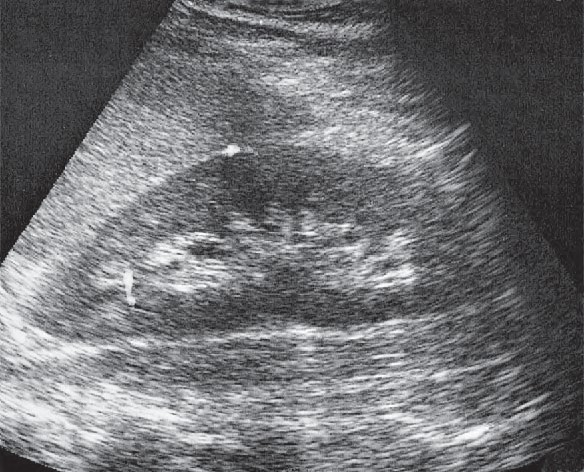
Który narząd widoczny jest na wydruku badania ultrasonograficznego?
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
Znak umieszczony w pracowni rezonansu magnetycznego zakazuje wstępu osobom

Scyntygrafia kości „whole body” jest wskazana podczas diagnostyki
Który obraz MR mózgu został wykonany w sekwencji DWI?
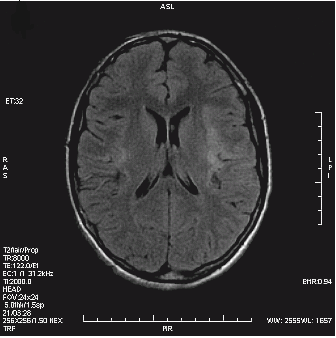
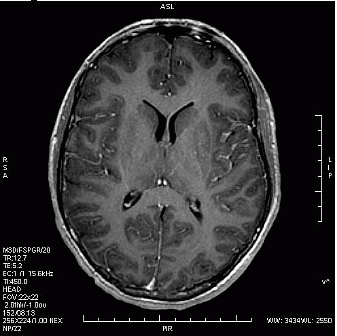
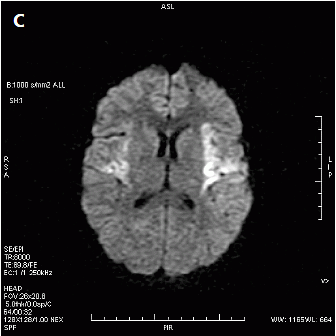
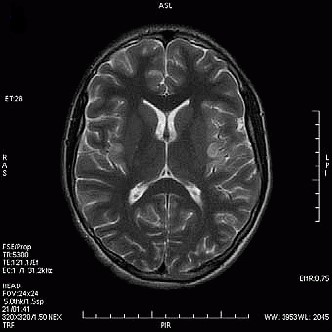
Zamieszczony obraz został wykonany metodą
Kolimator wielolistkowy w akceleratorze liniowym jest stosowany do
Jakie symbole mają odprowadzenia kończynowe dwubiegunowe w badaniu EKG?
Która sekwencja obrazowania MR wykorzystuje impulsy RF o częstotliwości rezonansowej tłuszczu do tłumienia sygnału pochodzącego z tkanki tłuszczowej?