Pytanie 1
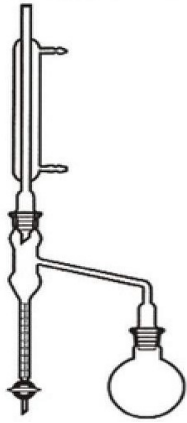
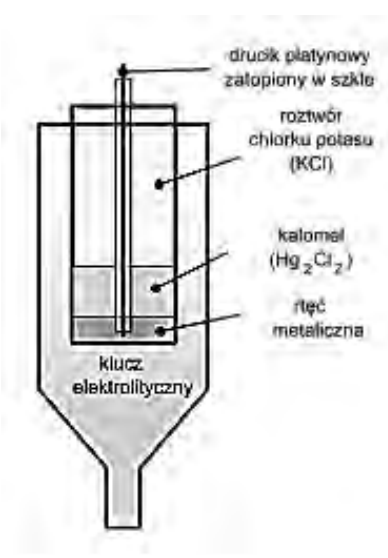
Na rysunku przedstawiono aparat, za pomocą którego można oznaczyć
Wynik: 33/40 punktów (82,5%)
Wymagane minimum: 20 punktów (50%)
Na rysunku przedstawiono aparat, za pomocą którego można oznaczyć

Podstawowe kryteria oceny jakości nafty to:
Zgodnie z klasyfikacją Bunsena, aniony przypisywane są do jednej z 7 grup analitycznych na podstawie różnic w ich zachowaniu względem jonów
W literaturze chromatografię określa się skrótem GC
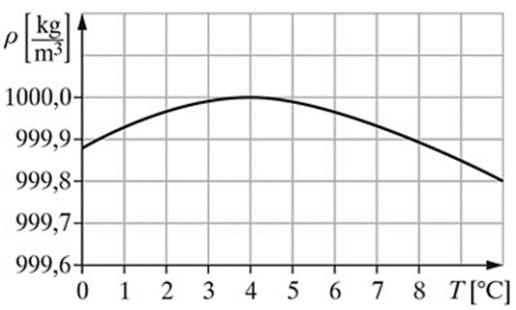
Na podstawie przedstawionego na rysunku wykresu zależności gęstości wody od temperatury, określ w jakiej temperaturze gęstość wody wynosi 1 g/cm3.
Czym jest eluent?
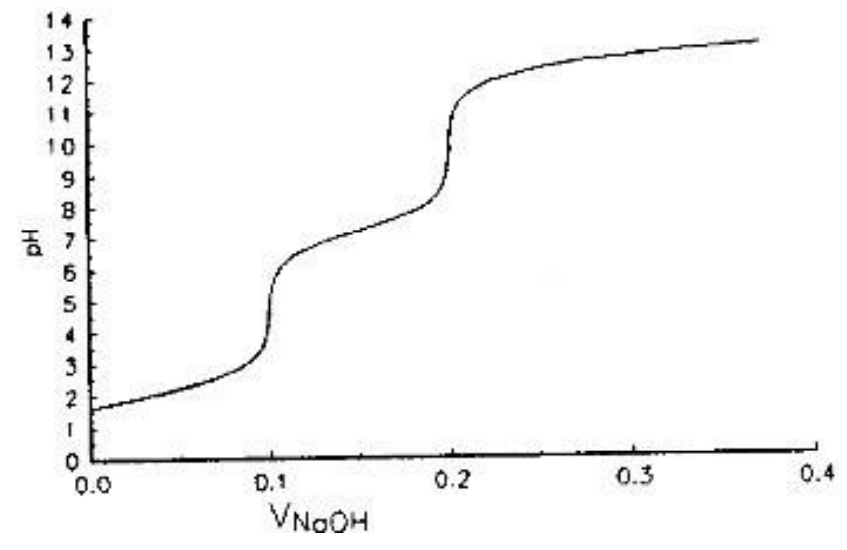
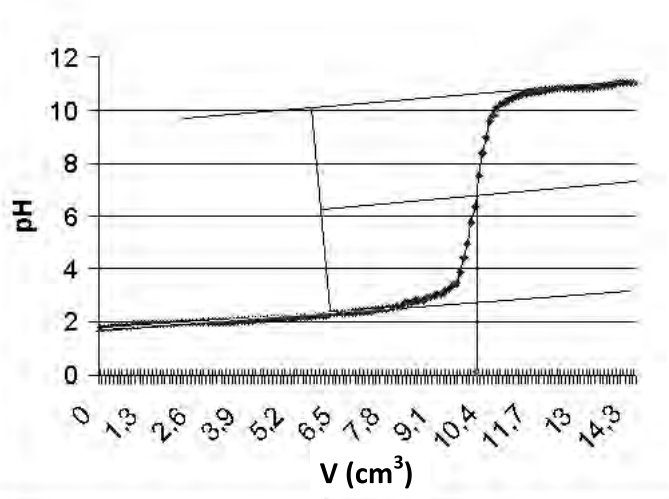
Przedstawioną na rysunku krzywą wyznaczono przy pomocy
Proces strącania osadu, który polega na wiązaniu na nim jonów lub cząsteczek, które w roztworze nie wytrąciłyby się samodzielnie, określa się mianem
Jakim urządzeniem określa się temperaturę zapłonu oleju opałowego?
W laboratorium mikrobiologicznym do przeprowadzania jałowienia na zimno wykorzystuje się
W analizie najczęściej oznacza się parametry CHZT i BZT
Na zmiareczkowanie odważki KOH zużyto 30,0 cm3 roztworu HCl o stężeniu 0,1 mol/dm3. Ile gramów KOH zawierała odważka?
| MKOH = 56 g/mol |
Na którym rysunku przedstawiono sprzęt stosowany do pomiaru mętności wody?
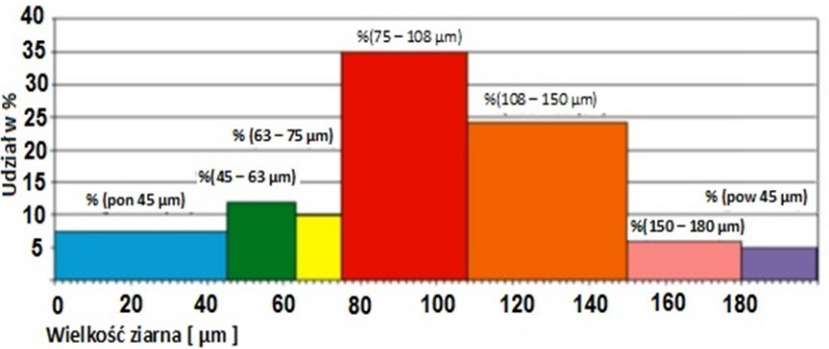
Na diagramie słupkowym przedstawiono wyniki analizy sitowej surowca w formie proszkowej. W jakiej kolejności zamontowano sita w wytrząsarce, licząc je od naczynia zbierającego?
W trakcie analizy przeprowadzonej metodą fotometrii płomieniowej próbkę nawozu o wadze 0,1000 g rozpuszczono w 250 cm3 wody destylowanej. Po wykonaniu badań uzyskano zawartość potasu równą 0,0830 mg/cm3. Jaką wartość procentową K2O ma badany nawóz i czy mieści się ona w normie, jeśli współczynnik przeliczeniowy K na K2O wynosi 1,205, a zawartość procentowa K2O w nawozie powinna być w zakresie 40-50%?
Który zbiór zawiera jedynie odczynniki grupowe używane w analizie jakościowej jonów?
Które urządzenie przedstawiono na rysunku?

Zakończenie miareczkowania ustala się na podstawie pomiaru zmiany przewodnictwa roztworu poddanego miareczkowaniu w metodzie
Błąd pomiarowy, który stanowi różnicę pomiędzy średnim wynikiem pomiaru a wartością rzeczywistą, określa się mianem
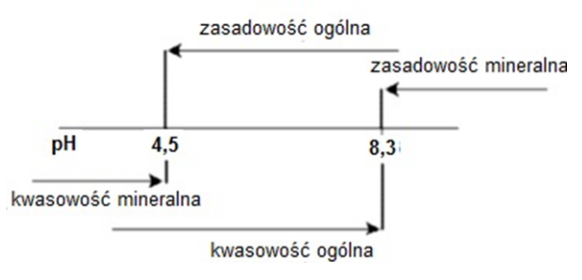
Na schemacie przedstawiono zakres występowania kwasowości i zasadowości w wodach naturalnych w zależności od pH. Dla wody o pH = 4,1 należy wykonać badanie
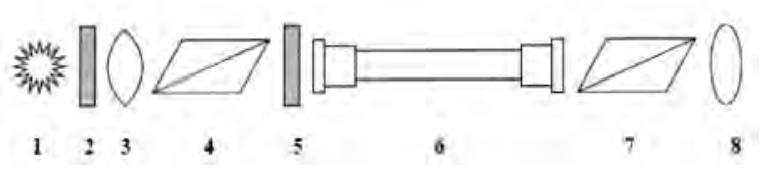
Na rysunku przedstawiającym schemat polarymetru, cyfrą 6 oznaczono
Na rysunku przedstawiono schemat elektrody
Związki lotne, które występują w wielu roślinach i mogą być wydobywane, np. poprzez destylację z parą wodną lub dzięki ciągłej ekstrakcji w aparacie Soxhleta, to
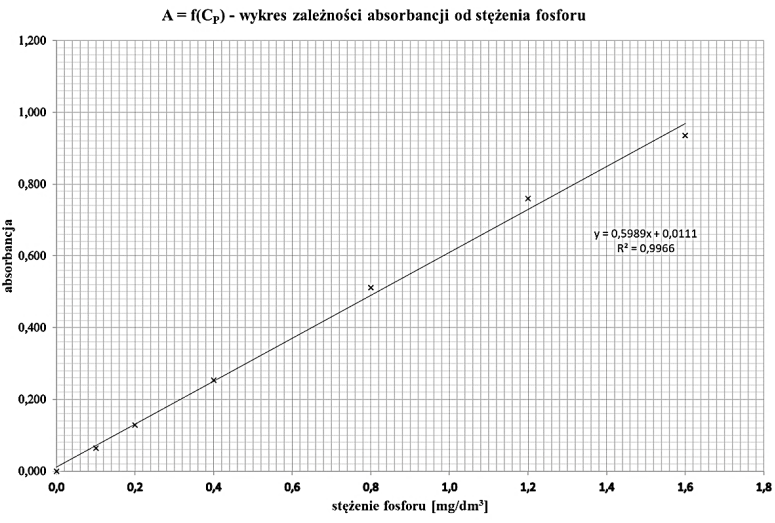
Na rysunku przedstawiono wykres zależności absorbancji od stężenia fosforu. Ile wynosi stężenie fosforu w próbce, jeśli absorbancja dla badanej próbki wynosi A = 0,628?
Wielkość określająca zmienność wyników przy wielokrotnym pomiarze tego samego składnika tą samą metodą nosi nazwę
Obecność jasnofioletowego zabarwienia płomienia palnika podczas analiz chemicznych wskazuje na obecność w roztworze jonów
Wskaź urządzenie, które wykorzystuje się do pomiaru zasolenia wody?
Zjawisko, w którym obce jony są mechanicznie zatrzymywane przez szybko rosnący kryształ, określane jest mianem
Zamieszczony opis dotyczy barwienia bakterii metodą
| − fiolet krystaliczny, 2-3 minuty, |
| − płyn Lugola, 1-2 minuty, |
| − alkohol aż do odbarwienia, ok. 30 sekund, |
| − woda – spłukanie, |
| − fuksyna w roztworze fenolowym (rozcieńczenie1:10), 20 sekund, |
| − woda – spłukanie |
Jaką metodę wykorzystuje się do identyfikacji cukrów redukujących?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
W dwóch nieoznaczonych probówkach znajdują się roztwory: w jednej – glukozy, a w drugiej - sacharozy. Jakiego odczynnika trzeba użyć, aby rozpoznać glukozę?
Oznaczona twardość ogólna wody wynosi 2 mval/dm3. Wartość ta przeliczona na stopnie niemieckie, zgodnie z zamieszczonym przelicznikiem jednostek, wynosi
| 1 mval/dm3 – 2,8°dH (stopni niemieckich) |
Jaką metodę analityczną stosuje się do pomiaru przewodnictwa cieczy umieszczonej między dwiema elektrodami, do których dostarczany jest prąd zmienny?
W trakcie badań mikrobiologicznych, pomimo stosowania pełnego i sterylnego stroju ochronnego oraz szczególnej staranności przy przeprowadzaniu pomiarów, dochodzi do zanieczyszczenia podłoża wzrostowego, co skutkuje wynikiem o kilka JTK/m3 wyższym od faktycznego stężenia zanieczyszczeń. Jakie to zjawisko?
Jaką metodą dokonuje się oceny intensywności koloru karmelu?
Określ typ destylacji, który polega na przemianie składnika mieszaniny substancji organicznych w stan pary w temperaturze niższej od jego temperatury wrzenia.
Z jaką precyzją należy zważyć próbkę o masie 20 mg, aby błąd względny nie wynosił więcej niż 0,05%?
Który spośród tłuszczów wymienionych w przedstawionej tabeli wykazuje najbardziej nienasycony charakter?
| Liczby właściwe wybranych tłuszczów | ||
|---|---|---|
| Rodzaj tłuszczu | Liczba zmydlania (LZ) mg KOH / g tłuszczu | Liczba jodowa (LJ) g I₂ / 100 g tłuszczu |
| Olej lniany | 187 – 197 | 169 – 192 |
| Olej sojowy | 188 – 195 | 114 – 138 |
| Olej rzepakowy | 167 – 179 | 94 – 106 |
| Tran wielorybi | 170 – 202 | 102 – 144 |
| Masło krowie | 218 – 245 | 25 – 38 |
| Smalec wieprzowy | 193 – 200 | 46 – 66 |
Przedstawiona na rysunku krzywa miareczkowania jest charakterystyczna dla