Pytanie 1
Na radiogramie uwidoczniono złamanie
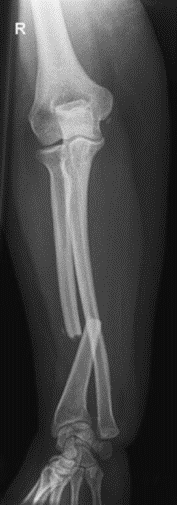
Wynik: 33/40 punktów (82,5%)
Wymagane minimum: 20 punktów (50%)
Na radiogramie uwidoczniono złamanie

Na obrazie uwidoczniono
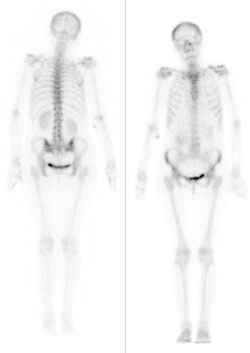
Które znaczniki są wykorzystywane w scyntygrafii tarczycy?
Na obrazie rezonansu magnetycznego strzałką wskazano patologiczny kręg
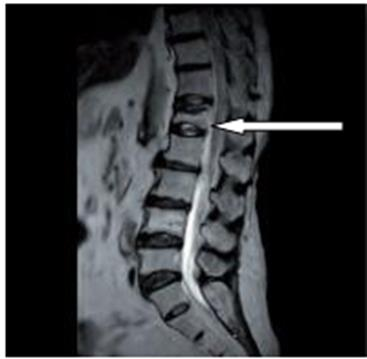
Która struktura może być oknem akustycznym w badaniu ultrasonograficznym?
Jednostką indukcji magnetycznej jest
W radiografii mianem SID określa się
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
Do zadań technika elektroradiologa w pracowni hemodynamicznej należy
Na obrazie MR jamy brzusznej strzałką wskazano
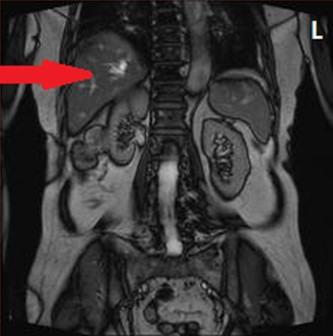
Zgodnie z procedurą wzorcową w badaniu MR należy ułożyć pacjenta na brzuchu do diagnostyki
Przyczyną zaniku kostnego jest
Do zadań technika elektroradiologa w pracowni hemodynamicznej należy
Teleterapia polega na napromienowaniu
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
Jaka jest odległość pomiędzy źródłem promieniowania a powierzchnią ciała pacjenta w technice izocentrycznej radioterapii?
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
Chorobą układu oddechowego typu obturacyjnego jest
Które odprowadzenie w badaniu EKG rejestruje różnice potencjałów pomiędzy lewym a prawym przedramieniem?
Kto jest odpowiedzialny za wykonywanie testów podstawowych kontroli jakości gammakamery w Zakładzie Medycyny Nuklearnej?
Na zamieszczonym przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano

W celu oceny wieku kostnego u dziecka praworęcznego, wykonuje się pojedyncze zdjęcie w projekcji
Promieniowanie rentgenowskie jest
Które zdjęcie RTG stawu łokciowego zostało wykonane w projekcji skośnej w rotacji zewnętrznej?
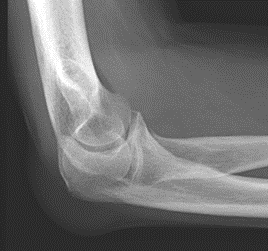
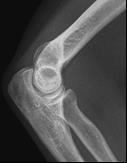
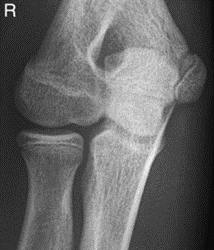
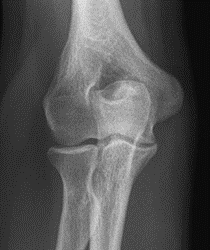
Na ilustracji przedstawiono zjawisko
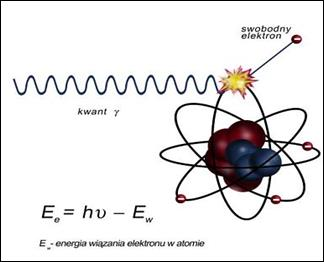
Nieostrość geometryczna obrazu rentgenowskiego zależy od
Technikę bramkowania oddechowego stosuje się w badaniu MR
W leczeniu izotopowym tarczycy podaje się
Który środek kontrastujący stosuje się w badaniu metodą rezonansu magnetycznego?
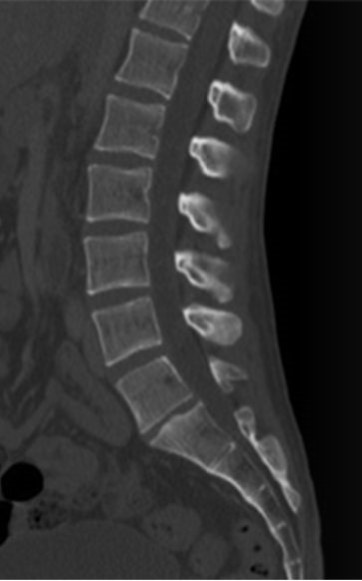
Którą metodą zostało wykonane badanie kręgosłupa zobrazowane na zdjęciu?
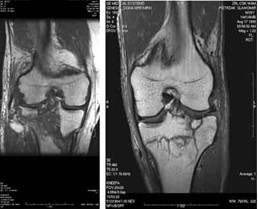
Którą metodą i w której płaszczyźnie zostało wykonane badanie stawu kolanowego zobrazowane na zdjęciach?
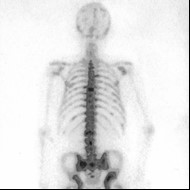
Przedstawiony obraz został zarejestrowany podczas wykonywania
Brachyterapia wewnątrzprzewodowa jest stosowana w leczeniu
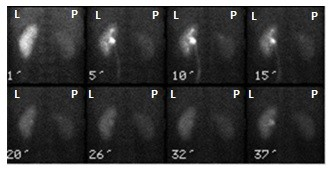
Na zarejestrowanych obrazach badania renoscyntygraficznego widać, że prawa nerka pacjenta
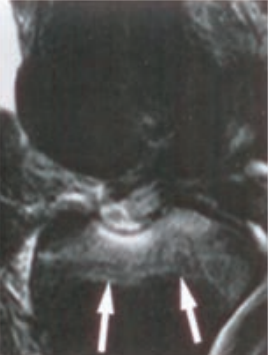
Obraz stawu kolanowego otrzymano metodą
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
Na radiogramie uwidoczniono złamanie
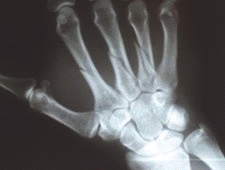
Które zdjęcia należy wykonać pacjentom z chorobą reumatoidalną stawów kolanowych?
„Ognisko zimne” w obrazie scyntygraficznym określa się jako
Objawem późnego odczynu popromiennego po teleradioterapii jest