Pytanie 1
Jaka jest moc dawki pochłoniętej w brachyterapii HDR?
Wynik: 36/40 punktów (90,0%)
Wymagane minimum: 20 punktów (50%)
Jaka jest moc dawki pochłoniętej w brachyterapii HDR?
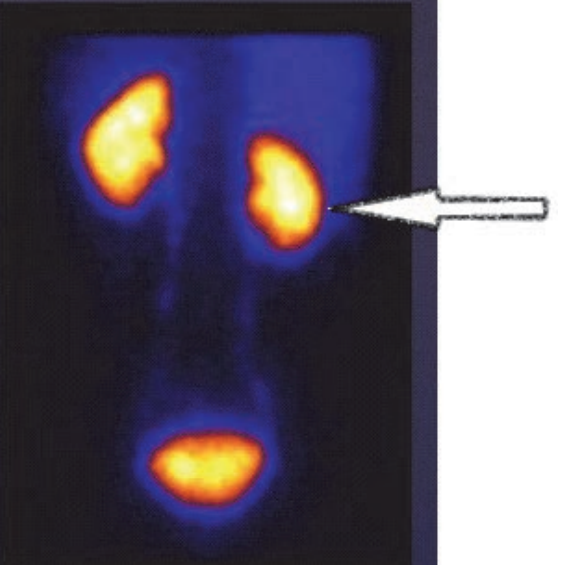
Który narząd został uwidoczniony na przedstawionym obrazie scyntygraficznym?
Jaki rozmiar kasety należy zastosować, wykonując standardowe zdjęcie stawu kolanowego w projekcji bocznej?
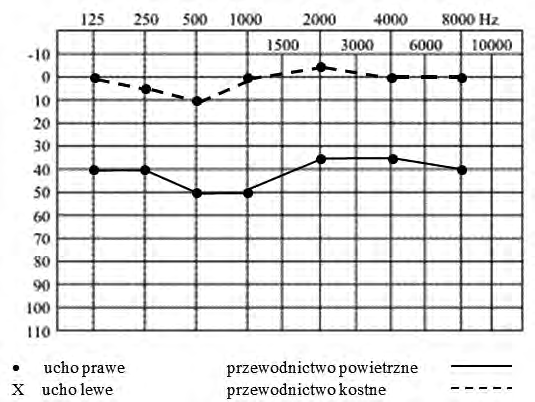
Na podstawie zapisu badania audiometrycznego rozpoznano u pacjenta uszkodzenie słuchu
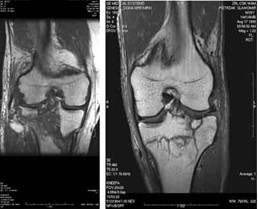
Którą metodą i w której płaszczyźnie zostało wykonane badanie stawu kolanowego zobrazowane na zdjęciach?
Badanie cewki moczowej polegające na wstecznym wprowadzeniu środka kontrastowego to
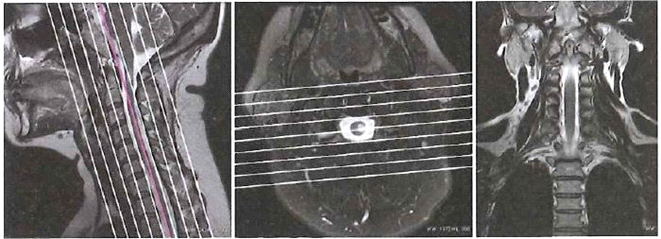
Obrazy MR kręgosłupa szyjnego przedstawiają etap planowania badania warstw
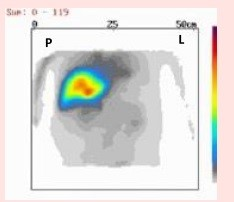
Podczas badania gammakamerą źródłem promieniowania jest
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
Dobierz dla standardowego pacjenta projekcję, pozycję i sposób ułożenia kasety o wymiarach 30 cm × 40 cm do zdjęcia przeglądowego układu moczowego.
| Projekcja | Pozycja | Ułożenie kasety | |||
|---|---|---|---|---|---|
| 1. | AP | 3. | stojąca | 5. | poprzeczne |
| 2. | PA | 4. | leżąca | 6. | podłużne |
Źródłem promieniowania protonowego stosowanego w radioterapii jest
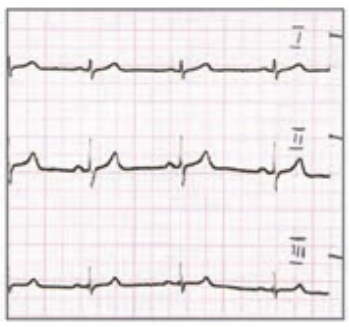
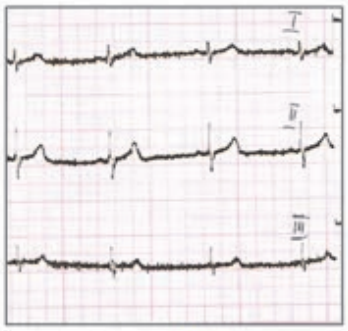
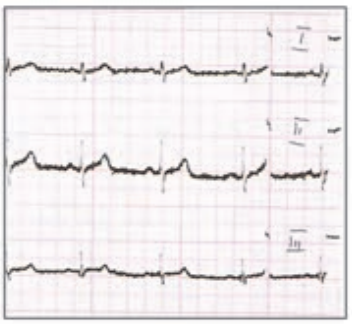
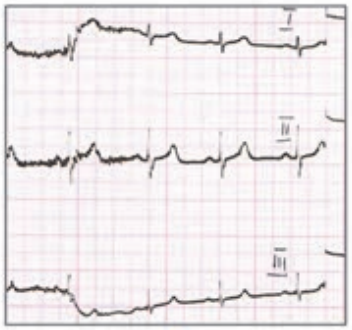
Który elektrokardiogram jest poprawny technicznie?
Podczas wykonywania zdjęcia rentgenowskiego klatki piersiowej w celu ochrony radiologicznej pacjenta należy zastosować
W scyntygrafii serca metoda bramkowanej akwizycji SPECT umożliwia między innymi ocenę frakcji wyrzutowej
Który zestaw zdjęć narządów klatki piersiowej należy wykonać u pacjenta z podejrzeniem lewostronnego zapalenia płuc?
Który radiofarmaceutyk należy podać pacjentowi w scyntygrafii perfuzyjnej mózgu?
W badaniu MR czas repetycji TR jest parametrem określającym odstęp czasu między
Radiogram przedstawia
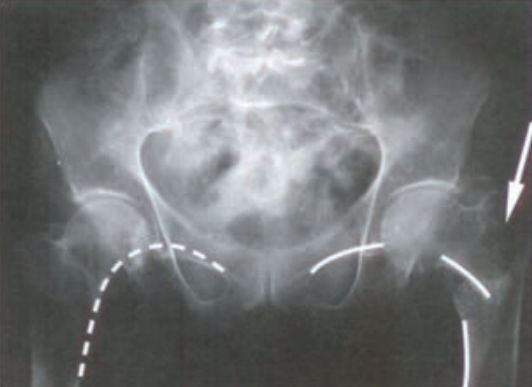
Który artefakt wskazano strzałkami na obrazie USG nerki?
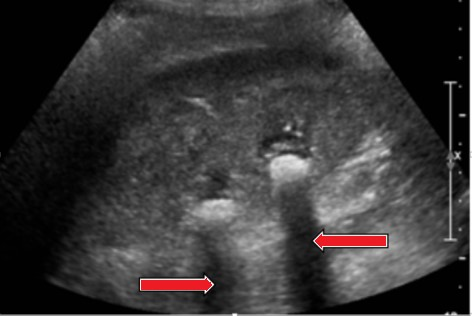
Zamieszczone obrazy związane są z badaniem
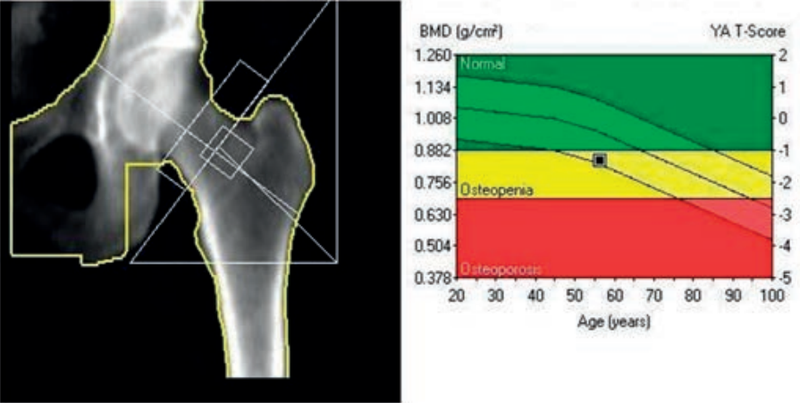
Przy ułożeniu do zdjęcia AP czaszki płaszczyzna
Na schemacie oznaczono
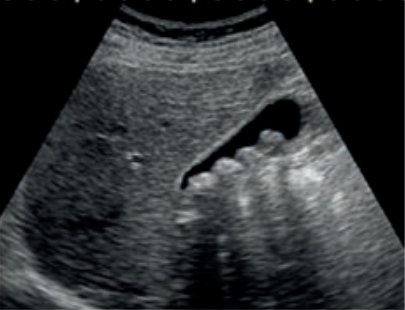
Jakie struktury anatomiczne uwidoczniono na obrazie USG?
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
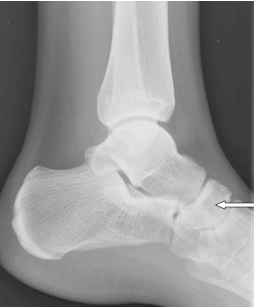
Na radiogramie strzałką oznaczono
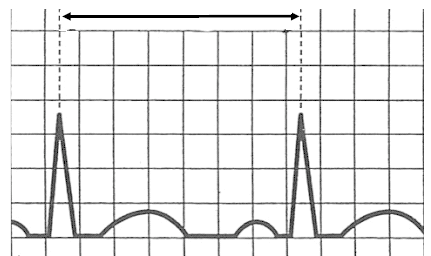
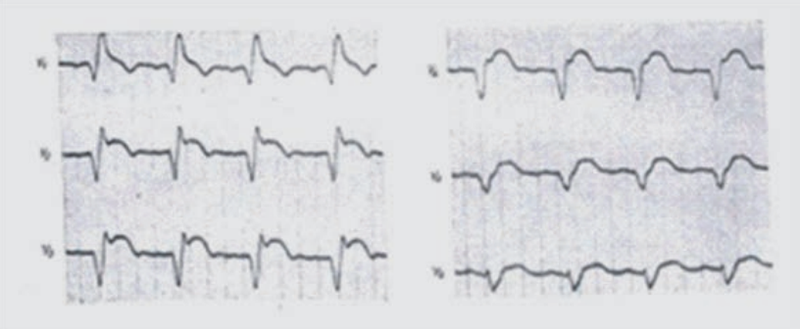
Na elektrokardiogramie zarejestrowano
Którym skrótem oznacza się tomografię komputerową wysokiej rozdzielczości?
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
Zadaniem technika elektroradiologii w pracowni badań naczyniowych jest
Obrazy DDR są tworzone w trakcie
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
Parametr SNR w obrazowaniu MR oznacza
Obrazowanie w sekwencjach STIR, FLAIR, SE wykonywane jest w badaniu
Kryterium rozpoznawczym dla fali δ (delta) w badaniu EKG jest
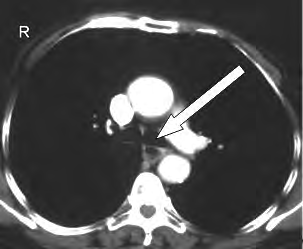
Na obrazie TK klatki piersiowej w przekroju poprzecznym strzałką oznaczono
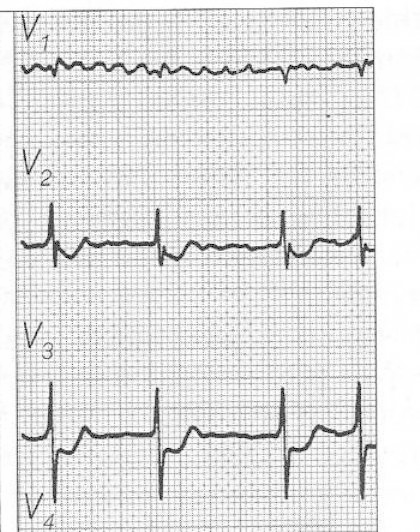
Zamieszczony elektrokardiogram przedstawia
Cholangiografia to badanie radiologiczne
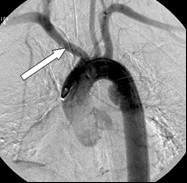
Na obrazie cyfrowej angiografii subtrakcyjnej strzałką zaznaczono
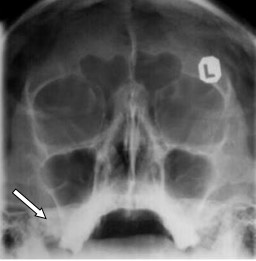
Na radiogramie czaszki strzałką zaznaczono
Na scyntygramie strzałką oznaczono