Pytanie 1
Jaką metodą nie można rozdzielać mieszanin?
Wynik: 28/40 punktów (70,0%)
Wymagane minimum: 20 punktów (50%)
Jaką metodą nie można rozdzielać mieszanin?
Aby przygotować 250 cm3 roztworu wodorotlenku potasu o stężeniu 0,25 mola, potrzebne będzie
Odważka analityczna wodorotlenku sodu, przygotowana fabrycznie, zawiera 0,1 mola NaOH. Jaką objętość wody destylowanej należy dodać w kolbie miarowej, aby uzyskać roztwór wodorotlenku sodu o stężeniu 0,0500 mol/dm3?
Które z poniższych równań ilustruje reakcję, w której powstają produkty gazowe?
Podstawowa substancja w analizie miareczkowej charakteryzuje się następującymi właściwościami:
Proces oddzielania składników jednorodnej mieszaniny, polegający na eliminacji jednego lub większej ilości składników z roztworu lub substancji stałej przy użyciu odpowiednio wybranego rozpuszczalnika, to
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
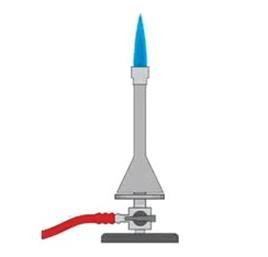
Na rysunku przedstawiono palnik
W przypadku rozlania żrącego odczynnika chemicznego na skórę pierwszym poprawnym działaniem jest:
Jak nazywa się proces, w którym następuje wytrącenie ciała stałego z przesyconego roztworu w wyniku spadku temperatury?
W trakcie określania miana roztworu NaOH, do zmiareczkowania 25,0 cm3 tego roztworu, użyto 30,0 cm3 roztworu HCl o stężeniu 0,1000 mol/dm3. Jakie miało miano zasady?
Jaką objętość powinna mieć kolba miarowa, aby przygotować mianowany roztwór NaOH o stężeniu 0,050 M z analitycznej odważki, która zawiera 0,1 mola NaOH?
Nie należy podgrzewać cieczy w szczelnie zamkniętych pojemnikach, ponieważ
Substancje chemiczne, które zazwyczaj wykorzystuje się w eksperymentach preparatywnych oraz w jakościowych analizach, charakteryzujące się czystością w przedziale 99-99,9%, nazywa się
Aby poprawić efektywność reakcji opisanej równaniem: HCOOH + C2H5OH ⇄ HCOOC2H5 + H2O, należy
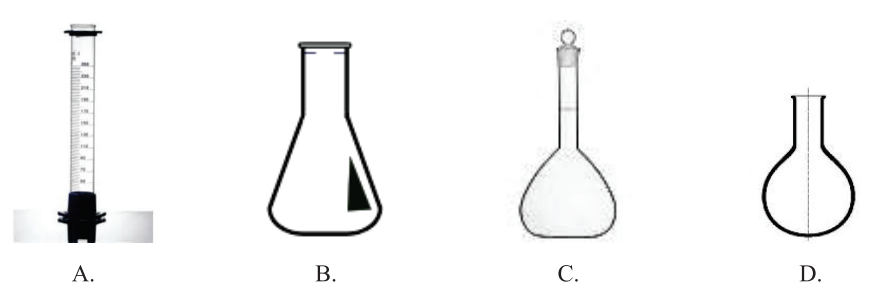
W celu przygotowania roztworu mianowanego należy użyć sprzętu przedstawionego na rysunku
Aby otrzymać 200 g roztworu siarczanu(VI) sodu o stężeniu 12%, należy wykorzystać
(Na – 23 g/mol; S – 32 g/mol; H – 1 g/mol; O – 16 g/mol)
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Najskuteczniejszą techniką separacji ketonu oraz kwasu karboksylowego obecnych w roztworze benzenowym jest
Aby przygotować 500 cm3 roztworu KMnO4 (M = 158 g/mol) o stężeniu 0,02 mol/dm3, ile należy zważyć?
W jakiej standardowej temperaturze są kalibrowane szklane naczynia pomiarowe?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Czułość bezwzględna wagi definiuje się jako
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Który z poniższych sposobów homogenizacji próbki jest najbardziej odpowiedni do przygotowania próbki gleby do analizy chemicznej?
Podczas rozkładu chloranu(V) potasu powstają chlorek potasu oraz tlen. Ile gramów tlenu zostanie wydzielonych w trakcie rozkładu 24,5 g chloranu(V) potasu, jeśli jednocześnie uzyskano 14,9 g chlorku potasu? Masy molowe pierwiastków: K = 39 g/mol, Cl = 35,5 g/mol, O=16 g/mol?
Sączenie na gorąco powinno być użyte, aby
Podaj kolejność odczynników chemicznych według rosnącego stopnia czystości?
Technika oddzielania płynnych mieszanin, w której wykorzystuje się różnice w prędkości migracji składników przez odpowiednią bibułę, nazywa się
Jakie metody można zastosować do rozdzielania i koncentracji składników próbki?
Proces oddzielania cieczy od osadu nazywa się
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Próbka pobrana z próbki ogólnej, która odzwierciedla cechy partii produktu, określa się jako próbka
Zgodnie z danymi zawartymi w tabeli wskaźników roztwór obojętny będzie miał barwę
| Wskaźnik | Zakres zmiany barwy (w jednostkach pH) | Barwa w środowisku | |
|---|---|---|---|
| kwaśnym | zasadowym | ||
| błękit tymolowy | 1,2 – 2,8 | czerwona | żółta |
| oranż metylowy | 3,1 – 4,4 | czerwona | żółta |
| czerwień metylowa | 4,8 – 6,0 | czerwona | żółta |
| czerwień chlorofenolowa | 5,2 – 6,8 | żółta | czerwona |
| błękit bromotymolowy | 6,0 – 7,6 | żółta | niebieska |
| czerwień fenolowa | 6,6 – 8,0 | żółta | czerwona |
| błękit tymolowy | 8,0 – 9,6 | żółta | niebieska |
| fenoloftaleina | 8,2 – 10,0 | bezbarwna | czerwona |
| żółcień alizarynowa | 10,1 – 12,0 | żółta | zielona |
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Sprzęt laboratoryjny przedstawiony na ilustracji stanowi element zestawu do

Jaką metodę poboru próbek przedstawiono na rysunku?

To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
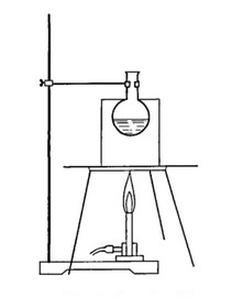
Na rysunku przedstawiono ogrzewanie kolby z cieczą w łaźni