Pytanie 1
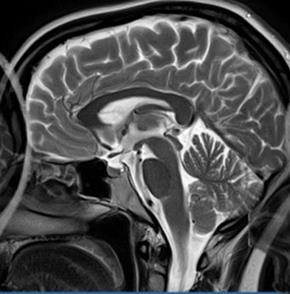
Która przyczyna spowodowała powstanie artefaktu widocznego na zamieszczonym obrazie MR?
Wynik: 14/40 punktów (35,0%)
Wymagane minimum: 20 punktów (50%)
Która przyczyna spowodowała powstanie artefaktu widocznego na zamieszczonym obrazie MR?

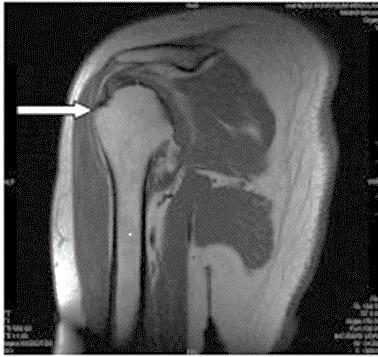
Którą strukturę anatomiczną oznaczono na zamieszczonym obrazie rezonansu magnetycznego?
Chorobą układu oddechowego typu obturacyjnego jest
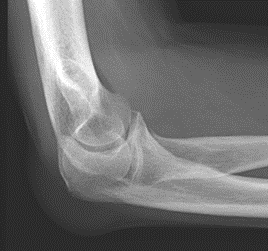
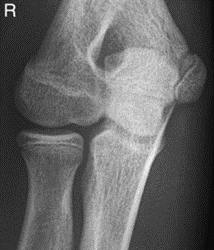
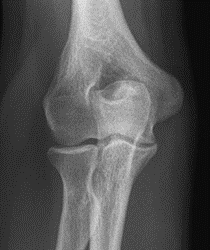
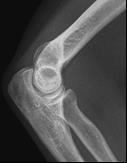
Które zdjęcie RTG stawu łokciowego zostało wykonane w projekcji skośnej w rotacji zewnętrznej?
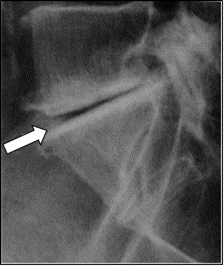
Na zamieszczonym rentgenogramie strzałką zaznaczono
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
W badaniu EKG odprowadzenie I rejestruje różnicę potencjałów między
Który obszar napromieniania w radioterapii oznacza się skrótem PTV?
Nieostrość geometryczna obrazu rentgenowskiego zależy od
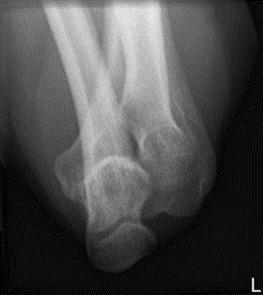
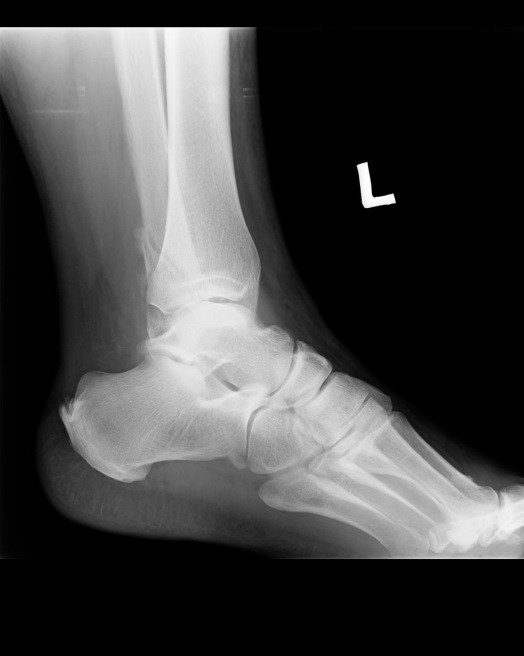
Którą strukturę anatomiczną i w jakiej projekcji uwidoczniono na radiogramie?
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Jak przebiega promień centralny w projekcji AP czaszki?
Na obrazie radiologicznym uwidoczniono złamanie kości
Gdzie znajduje się węzeł zatokowo-przedsionkowy wywołujący rytmiczne skurcze mięśnia serca?
W badaniu cystografii wstępującej środek kontrastowy należy podać
Brak odpowiedzi na to pytanie.
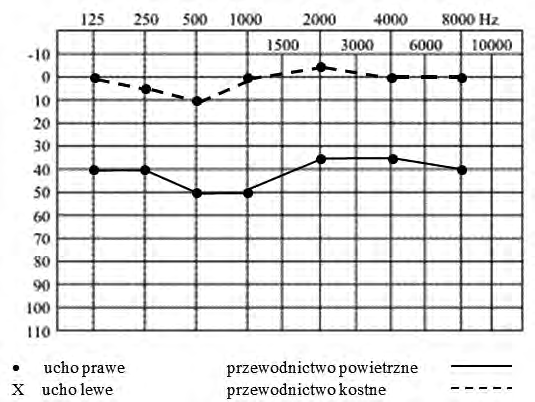
Na podstawie zapisu badania audiometrycznego rozpoznano u pacjenta uszkodzenie słuchu
Brak odpowiedzi na to pytanie.
Proces chemicznego wywoływania radiogramów polega na
Brak odpowiedzi na to pytanie.
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
Brak odpowiedzi na to pytanie.
Jakie symbole mają odprowadzenia kończynowe dwubiegunowe w badaniu EKG?
Brak odpowiedzi na to pytanie.
W badaniu MR nadgarstka w ułożeniu na supermana pacjent leży na
Brak odpowiedzi na to pytanie.
Który środek kontrastujący stosuje się w badaniu metodą rezonansu magnetycznego?
Brak odpowiedzi na to pytanie.
W leczeniu izotopowym tarczycy należy podać
Brak odpowiedzi na to pytanie.
Hiperfrakcjonowanie dawki w radioterapii oznacza napromienienie pacjenta
Brak odpowiedzi na to pytanie.
Który obszar napromieniania wskazano na ilustracji strzałką?
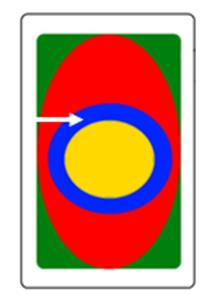
Brak odpowiedzi na to pytanie.
Który środek ochrony radiologicznej należy zastosować podczas badania czaszki 53-letniego pacjenta za pomocą tomografii komputerowej?
Brak odpowiedzi na to pytanie.
W pozytonowej tomografii emisyjnej PET zostaje zarejestrowane promieniowanie powstające podczas
Brak odpowiedzi na to pytanie.
Na wykresie EKG zaznaczono
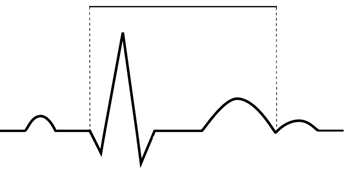
Brak odpowiedzi na to pytanie.
Na obrazie ultrasonograficznym jamy brzusznej strzałką wskazano
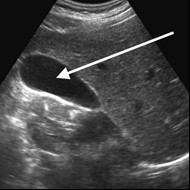
Brak odpowiedzi na to pytanie.
Zamieszczone na ilustracji obrazy dotyczą badania
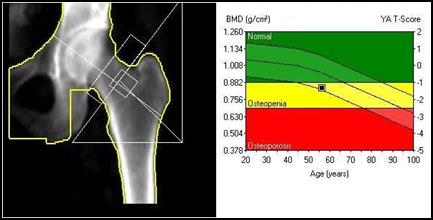
Brak odpowiedzi na to pytanie.
Na obrazie TK nadgarstka uwidocznione jest złamanie kości
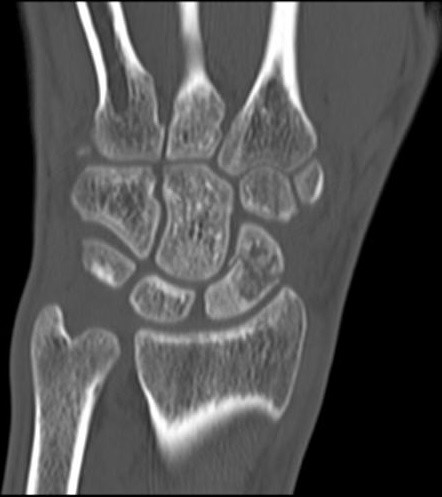
Brak odpowiedzi na to pytanie.
Obiektywną metodą badania słuchu jest audiometria
Brak odpowiedzi na to pytanie.
Cholangiografia to badanie radiologiczne
Brak odpowiedzi na to pytanie.
Które ciało obce w obszarze badania nie stanowi przeciwwskazania do wykonania MR?
Brak odpowiedzi na to pytanie.
Który materiał światłoczuły należy zastosować w rentgenodiagnostyce analogowej, by zminimalizować dawkę promieniowania jonizującego otrzymaną przez pacjenta?
Brak odpowiedzi na to pytanie.
Do środków kontrastujących negatywnych należą
Brak odpowiedzi na to pytanie.
Kolimator wielolistkowy w akceleratorze liniowym jest stosowany do
Brak odpowiedzi na to pytanie.
Na obrazie rezonansu magnetycznego strzałką wskazano patologiczny kręg
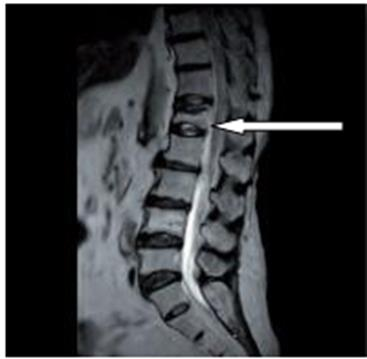
Brak odpowiedzi na to pytanie.
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Brak odpowiedzi na to pytanie.
Którą ochronę radiologiczną należy zastosować podczas wykonywania zdjęcia rentgenowskiego przeglądowego klatki piersiowej u pacjentki w okresie rozrodczym?
Brak odpowiedzi na to pytanie.
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz
Brak odpowiedzi na to pytanie.