Pytanie 1
Roztwór, który jest dodawany z biurety w formie kropli do roztworu substancji, którą analizujemy, określamy mianem
Wynik: 27/40 punktów (67,5%)
Wymagane minimum: 20 punktów (50%)
Roztwór, który jest dodawany z biurety w formie kropli do roztworu substancji, którą analizujemy, określamy mianem
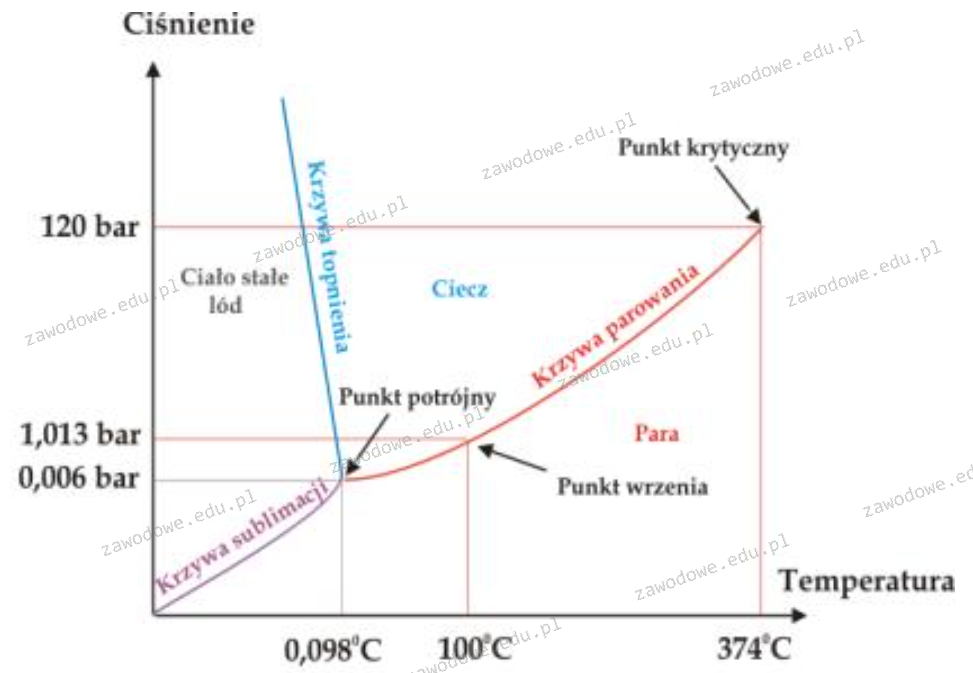
Korzystając z wykresu wskaż, w jakiej postaci występuje woda w temperaturze 10°C i pod ciśnieniem 100 barów.
Jakim rozpuszczalnikiem o niskiej temperaturze wrzenia wykorzystuje się do suszenia szkła laboratoryjnego?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Którego odczynnika należy użyć do przygotowania roztworu wzorcowego, zawierającego jony \( \text{Fe}^{3+} \)?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Zaleca się schładzanie próbek wody transportowanych do laboratorium do temperatury
Nie należy używać do czyszczenia szklanych naczyń laboratoryjnych
W celu uzyskania 500 g mieszaniny oziębiającej o temperaturze -18oC należy zmieszać
| Tabela. Mieszaniny oziębiające | ||
|---|---|---|
| Temperatura mieszaniny [°C] | Skład mieszaniny | Stosunek masowy |
| -2 | Woda + chlorek amonu | 10 : 3 |
| -15 | Woda + rodanek amonu | 10 : 13 |
| -18 | Lód + chlorek amonu | 10 : 3 |
| -21 | Lód + chlorek sodu | 3 : 1 |
| -22 | Lód + chlorek amonu + azotan(V) amonu | 25 : 5 : 11 |
| -25 | Lód + azotan(V) amonu | 1 : 1 |
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Przedstawiony sposób dotyczy pobierania próbki wody do przeprowadzenia badań
| Sposób pobierania próbki wody do przeprowadzenia badań: - próbki pobrać do sterylnych butelek; - przed przystąpieniem do pobierania wody zdjąć z kurka wszelkie urządzenia, zeskrobać zanieczyszczenia, następnie całkowicie otwierając i zamykając zawór, wielokrotnie płukać; - metalowy kurek wysterylizować płomieniem, a kurek z tworzywa sztucznego alkoholem etylowym; - kurek otworzyć do połowy przepływu i spuszczać wodę przez około 2-3 minuty do osiągnięcia stałej temperatury; - pobrać próbkę wody napełniając butelkę do około ¾ objętości i natychmiast zamknąć korkiem. |
Na etykiecie próbki środowiskowej należy umieścić datę jej pobrania, lokalizację poboru oraz
W celu przygotowania 100 cm3 roztworu mianowanego, jaką kolbę należy zastosować?
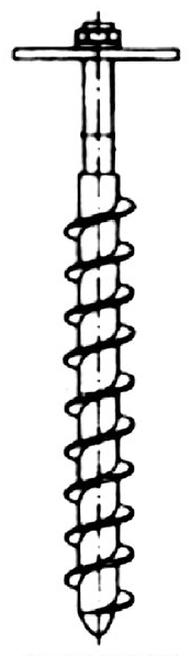
Na rysunku pokazano przyrząd do poboru próbek
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Laboratoryjny stół powinien być zaopatrzony w instalację gazową oraz
Wszystkie pojemniki z odpadami, zarówno stałymi, jak i ciekłymi, które są przekazywane do służby zajmującej się utylizacją, powinny być opatrzone informacjami
Mianowanie roztworu o stężeniu przybliżonym można wykonać poprzez
Eliminacja substancji organicznych z próbki poprzez jej spalenie nazywa się
Próbkę uzyskaną z próbki ogólnej poprzez jej zmniejszenie nazywa się
Na diagramie przedstawiającym proces pobierania prób środowiskowych do analizy literą Y oznaczono próbkę
Czysty odczynnik (skrót: cz.) charakteryzuje się poziomem czystości wynoszącym
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Przebieg: Po zważeniu dwóch suchych zlewek, odważ kolejno: do jednej 3,63 g Co(NO3)2·6H2O, a do drugiej 3,75 g Na2CO3·10H2O. Następnie do obu zlewek wlej 25 cm3 gorącej wody i mieszając za pomocą bagietki doprowadź do całkowitego rozpuszczenia soli. Do roztworu Co(NO3)2 dodaj gorący roztwór Na2CO3 podczas mieszania. Otrzymany roztwór schłodź w łaźni wodnej z 3 kostkami lodu do temperatury pokojowej. Schłodzony roztwór przefiltruj przy użyciu zestawu do sączenia pod próżnią. Osad na lejku przepłucz wodą destylowaną, aż osiągnie obojętny odczyn przesączu. Przesączony osad osusz z sączkiem międzyposiadającym złożone arkusze bibuły w temperaturze pokojowej. Po wyschnięciu osad zważ i oblicz wydajność. Określ, jaki czynnik wpływa na skład jakościowy uzyskanego węglanu kobaltu(II)?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Jakie urządzenie wykorzystuje się do określania lepkości płynów?
W standardowym układzie destylacyjnym, który ma ukośną chłodnicę, wykorzystuje się chłodnicę
Ile masy kwasu mrówkowego jest wymagane do uzyskania 11,2 dm3 tlenku węgla(II) (w warunkach normalnych) w procesie odwodnienia kwasu mrówkowego (M = 46 g/mol) za pomocą kwasu siarkowego(VI), zakładając efektywność procesu na poziomie 70%?
Jakie urządzenie laboratoryjne jest używane do realizacji procesu ekstrakcji?
W trakcie destylacji cieczy wykorzystuje się tzw. kamienie wrzenne, ponieważ
Temperatura topnienia mocznika wynosi 133 °C. W celu określenia czystości preparatów tej substancji, przeprowadzono badania temperatury ich topnienia, uzyskując wyniki przedstawione w tabeli. Wskaż preparat o najmniejszym stopniu czystości.
| Preparat | A | B | C | D |
|---|---|---|---|---|
| Zakres temperatury topnienia [°C] | 132-133 | 130-133 | 125-133 | 128-133 |
Z partii materiału należy pobrać ogólną próbkę w ilości odpowiadającej promilowi całej partii. Na podstawie podanej informacji określ, ile pierwotnych próbek, każda ważąca 10 g, trzeba pobrać z partii cukru o masie 0,5 t, aby uzyskać reprezentatywną próbkę ogólną?
Ogrzewanie organicznych substancji w atmosferze powietrza w otwartym naczyniu, mające na celu przemianę tych substancji w związki nieorganiczne, określa się jako mineralizacja?
W karcie charakterystyki chemikaliów znajduje się informacja o przechowywaniu dichromianu(VI) potasu: .. powinien być przechowywany w odpowiednio oznakowanych, szczelnie zamkniętych pojemnikach, w chłodnym, suchym i dobrze wentylowanym magazynie, który posiada instalację elektryczną i wentylacyjną. Z tego opisu wynika, że ten chemikal może być przechowywany
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Aby otrzymać roztwór AgNO3 (masa molowa AgNO3 to 169,8 g/mol) o stężeniu 0,1 mol/dm3, należy
Roztwory o ściśle określonym stężeniu, używane w analizach miareczkowych, nazywamy
Aby oddzielić mieszankę etanolu i wody, konieczne jest przeprowadzenie procesu
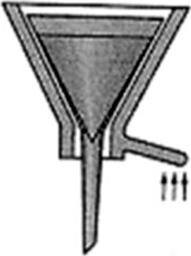
Na ilustracji przedstawiono sprzęt stosowany do sączenia osadu