Pytanie 1
Na obrazie RM uwidoczniono odcinek kręgosłupa
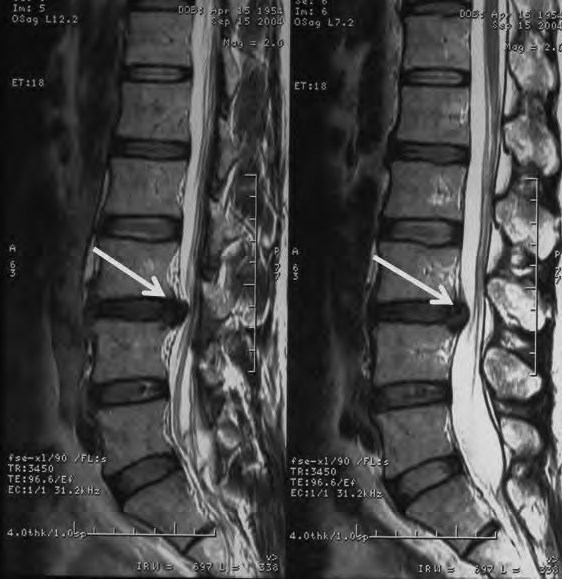
Wynik: 30/40 punktów (75,0%)
Wymagane minimum: 20 punktów (50%)
Na obrazie RM uwidoczniono odcinek kręgosłupa

Standardowe badanie urografii polega na podaniu pacjentowi środka kontrastującego
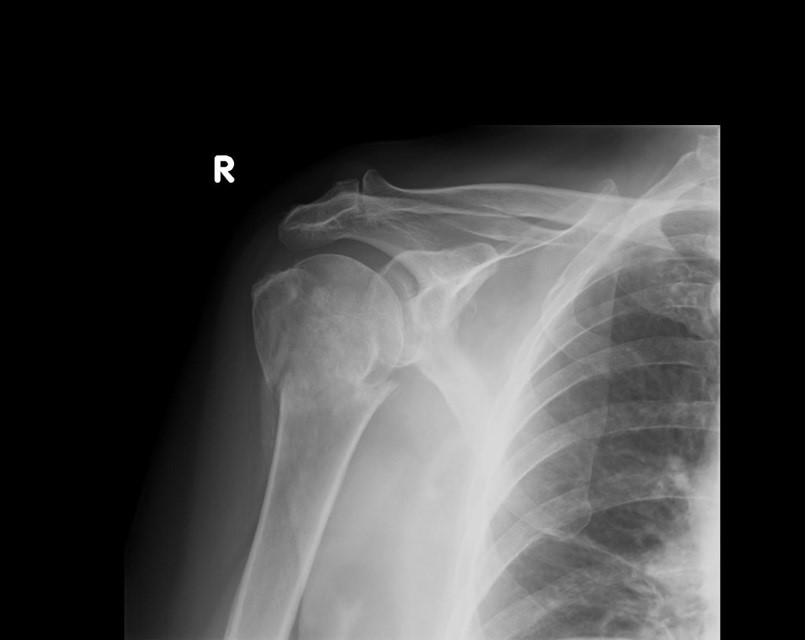
Na radiogramie uwidoczniono złamanie
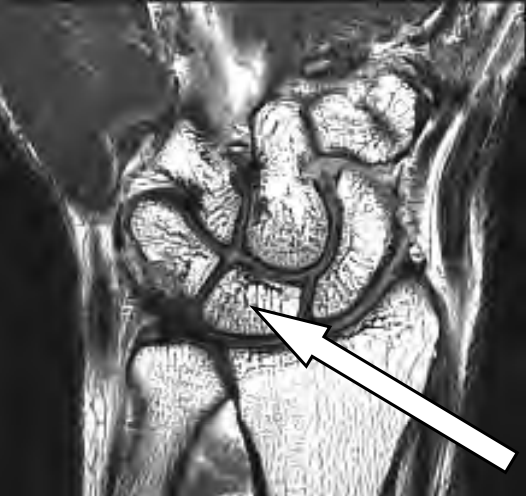
Na obrazie RM nadgarstka lewego strzałką oznaczono kość
Jakie wiązki promieniowania emituje medyczny akcelerator liniowy?
Diagnozowanie metodą PET oparte jest na zjawisku
W badaniu EEG w systemie „10-20” elektrody w okolicy skroniowej oznaczone są literą
W systemie międzynarodowym ząb pierwszy przedtrzonowy po stronie lewej oznacza się symbolem
Na zamieszczonym przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano

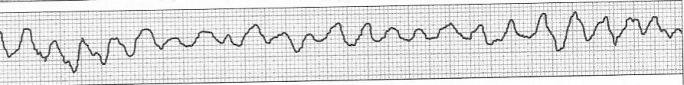
Zamieszczony elektrokardiogram przedstawia
Na obrazie rezonansu magnetycznego strzałką oznaczono wyrostek kolczysty kręgu
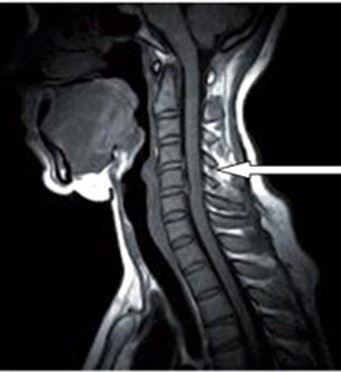
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
W której próbie stroikowej przystawia się stroik do czoła (u podstawy nosa) lub na szczycie głowy i porównuje się przewodnictwo kostne ucha prawego i lewego?
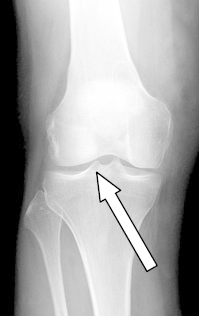
Którą strukturę anatomiczną oznaczono strzałką na radiogramie stawu kolanowego?
W metodzie RM (rezonansu magnetycznego) po umieszczeniu pacjenta w silnym, stałym polu magnetycznym dochodzi do oddziaływania
W badaniu PET stosuje się tylko radioizotopy emitujące
W badaniu audiometrycznym do oceny przewodnictwa kostnego wybranego ucha słuchawkę kostną należy przyłożyć do
W badaniu EKG punktem przyłożenia odprowadzenia przedsercowego C2 jest
Jednym z kryteriów poprawnie wykonanego badania spirometrycznego jest czas trwania natężonego wydechu, który powinien wynosić u osób powyżej 10 roku życia co najmniej
Jakie wymagania techniczne muszą spełniać aparaty terapeutyczne stosowane w zakładach brachyterapii, służące bezpośrednio do napromieniania pacjenta metodą zdalnego wprowadzania źródeł promieniotwórczych?
W leczeniu izotopowym tarczycy podaje się
Warstwa półchłonna (WP) służy do obliczania
Jaki kolor ma warstwa korowa kości w badaniu MR na obrazie T1- zależnym?
Do podstawowych projekcji stosowanych w diagnostyce mammograficznej należą
Na rentgenogramie stopy uwidocznione jest złamanie
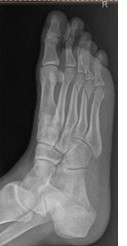
Na obrazie uwidoczniono złamanie kompresyjne kręgu
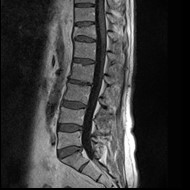
Z kratką przeciwrozproszeniową należy wykonać zdjęcie
Scyntygrafia kości „whole body” jest wskazana podczas diagnostyki
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Parametrem krwi, który powinien zostać oznaczony u pacjenta przed wykonaniem badania MR z kontrastem jest
Po podaniu kontrastu obraz zmian nowotworowych w badaniu MR najlepiej uwidacznia się w sekwencji
Badanie cewki moczowej polegające na wstecznym wprowadzeniu środka kontrastowego to
Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest
Jakie źródła promieniowania stosowane są w brachyterapii?
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
Kryterium rozpoznawczym dla fali δ (delta) w badaniu EKG jest
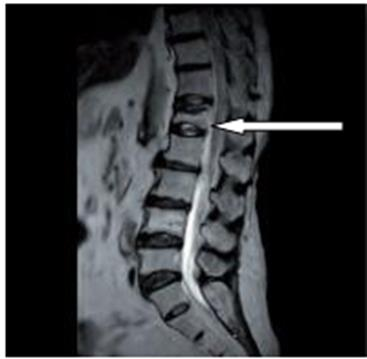
Na obrazie rezonansu magnetycznego strzałką wskazano patologiczny kręg
Które ciało obce w obszarze badania nie stanowi przeciwwskazania do wykonania MR?
Więzka promieniowania X to