Pytanie 1
Którego związku chemicznego, z uwagi na jego silne właściwości higroskopijne, nie powinno się używać w analizie miareczkowej jako substancji podstawowej?
Wynik: 34/40 punktów (85,0%)
Wymagane minimum: 20 punktów (50%)
Którego związku chemicznego, z uwagi na jego silne właściwości higroskopijne, nie powinno się używać w analizie miareczkowej jako substancji podstawowej?
Reagenty o najwyższej czystości to reagenty
Na skutek krystalizacji 18 g kwasu benzoesowego uzyskano 8 g czystego produktu. Jaką wydajność miała ta krystalizacja?
Które spośród substancji wymienionych w tabeli pozwolą pochłonąć wydzielający się tlenek węgla(IV)?
| I | II | III | IV | V |
|---|---|---|---|---|
| Ca(OH)2(aq) | NaOH(s) | HNO3(stęż) | CuO(s) | CaO(s) |
Proces nitrowania najczęściej realizuje się, stosując organiczny substrat
Przedstawiony schemat ideowy ilustruje proces wytwarzania N2 → NO → NO2 → HNO3
W standardowym układzie destylacyjnym, który ma ukośną chłodnicę, wykorzystuje się chłodnicę
Pobieranie próbek wody z zbiornika wodnego, który zasila system wodociągowy, powinno odbywać się
Woda, która została poddana dwukrotnej destylacji, to woda
Eliminacja substancji organicznych z próbki poprzez jej spalenie nazywa się
Aby przygotować miano kwasu solnego, konieczne jest odważenie węglanu sodu o masie wynoszącej około 400 mg. Jaką precyzję powinna mieć waga używana do odważenia węglanu sodu?
Po rozpuszczeniu substancji w kolbie miarowej, należy odczekać przed dopełnieniem jej wodą "do kreski" miarowej. Taki sposób postępowania jest uzasadniony
Który z poniższych czynników nie mógł przyczynić się do błędnego określenia całkowitej liczby drobnoustrojów w surowym mleku?
Jakie oznaczenie znajduje się na naczyniach szklanych kalibrowanych do wlewu?
Oblicz, jaką ilość węglanu sodu w gramach należy przygotować, aby uzyskać 500 cm3 roztworu tej soli o stężeniu 0,1000 mol/dm3.
MNa = 23 g/mol, MC = 12 g/mol, MO = 16 g/mol
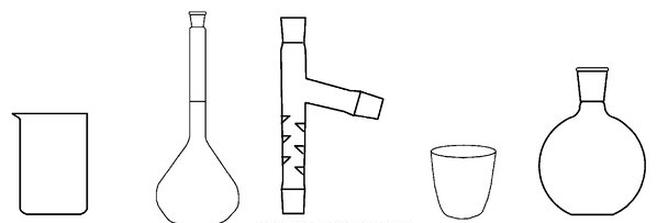
Wybierz zestaw, w którym znajdują się wyłącznie nazwy sprzętu laboratoryjnego pokazanego na rysunkach.
Aby uzyskać sole sodowe fenoli, należy stopić dany fenol z sodą (M = 106 g/mol), stosując 10% nadmiar w porównaniu do ilości stechiometrycznej, według równania:
2 ArOH + Na2CO3 → 2 ArONa + H2O + CO2 Ile sody jest wymagane do reakcji z 7,2 g 2-naftolu (M = 144 g/mol)?
Jakie narzędzie w laboratorium jest wykorzystywane do rozdrabniania małych ilości substancji stałych?
Błąd związany z odczytem poziomu cieczy w kolbie miarowej, spowodowany niewłaściwą pozycją oka w stosunku do skali, nazywany jest błędem
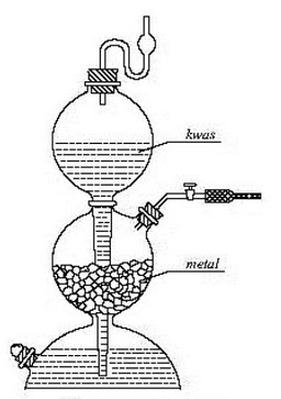
Na rysunku przedstawiono aparat
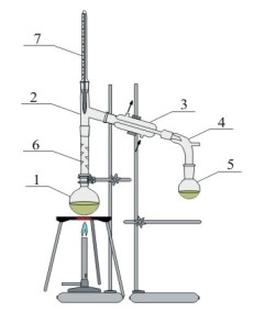
Na rysunku numerem 3 oznaczono
Sposoby utrwalania i przechowywania próbek wody przeznaczonych do badań fizykochemicznych.
Próbkę wody przeznaczoną do oznaczenia zawartości metali poddaje się utrwalaniu za pomocą
| Oznaczenie | Sposób utrwalania i przechowywania |
|---|---|
| Barwa | Przechowywać w ciemności |
| Mętność | Przechowywać w ciemności |
| Twardość | pH = 3 z użyciem HNO3 |
| OWO | 0,7 ml HCl/30 ml próbki |
| ChZT | pH 1- 2 z użyciem H2SO4 |
| Fosfor | Przechowywać w temperaturze 1-5°C |
| Glin | pH 1-2 z użyciem HNO3 |
| Żelazo | pH 1-2 z użyciem HNO3 |
| Utlenialność | pH1-2 z użyciem H2SO4, Przechowywać w ciemności |
W urządzeniu Soxhleta wykonuje się
Rozpuszczalnik stosowany w procesie krystalizacji powinien
Zgłębniki o konstrukcji przypominającej świder są wykorzystywane do pobierania próbek różnych materiałów
Wskaż definicję fiksanali?
Jak przebiega procedura unieszkodliwiania rozlanego kwasu siarkowego(VI)?
Sód powinien być przechowywany
Roztwór zawierający 16,00 g siarczanu(VI) miedzi(II) nasycono siarkowodorem. Masa wytrąconego siarczku miedzi(II), po odsączeniu i wysuszeniu, wynosiła 8,64 g. Oblicz procentową wydajność tej reakcji.
Równanie reakcji:
\( \text{CuSO}_4 + \text{H}_2\text{S} \rightarrow \text{CuS} + \text{H}_2\text{SO}_4 \)
\( \text{M CuSO}_4 = 160 \, \text{g/mol} \)
\( \text{M CuS} = 96 \, \text{g/mol} \)
W wyniku reakcji 100 g azotanu(V) ołowiu(II) z jodkiem potasu otrzymano 120 g jodku ołowiu(II). Wydajność reakcji wyniosła
| Pb(NO3)2 + 2KI → PbI2 + 2KNO3 | |
| (MPb(NO3)2 = 331 g/mol, MKI = 166 g/mol, MPbI2 = 461 g/mol, MKNO3 = 101 g/mol) |
Zestaw do filtracji pod obniżonym ciśnieniem powinien obejmować między innymi
Sączenie na gorąco powinno być użyte, aby
W probówce połączono roztwory CuSO4 oraz NaOH. Powstał niebieski osad, który po podgrzaniu zmienił kolor na czarny. Czarnym osadem jest
Jakim kolorem oznacza się instalację gazową w laboratorium analitycznym?
Chemikalia, dla których upłynął okres przydatności,
Jakie czynniki wpływają na zmiany jakościowe w składzie próbki?
Przykładem piany stałej jest
| faza rozproszona | faza rozpraszająca | ||
|---|---|---|---|
| gaz | ciecz | ciało stałe | |
| gaz | - | piana | piana stała |
| ciecz | aerozol ciekły | emulsja | emulsja stała |
| ciało stałe | aerozol stały | zol | zol stały |
Proces chemiczny, który polega na przejściu substancji w stanie stałym do roztworu, związany z reakcją tej substancji z rozpuszczalnikiem, to
Jaką masę chlorku sodu można znaleźć w 150 g roztworu soli o stężeniu 5% (m/m)?
W nieopisanej butelce prawdopodobnie znajduje się roztwór zasadowy. Wskaż odczynnik, który pozwoli to zweryfikować?