Pytanie 1
Które ciało obce w obszarze badania nie stanowi przeciwwskazania do wykonania MR?
Wynik: 3/40 punktów (7,5%)
Wymagane minimum: 20 punktów (50%)
Które ciało obce w obszarze badania nie stanowi przeciwwskazania do wykonania MR?
Rak drobnokomórkowy i rak niedrobnokomórkowy to postacie organiczne nowotworów złośliwych
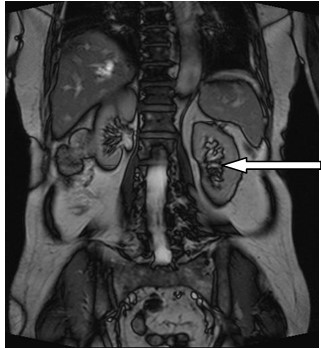
Który narząd został oznaczony strzałką na obrazie rezonansu magnetycznego?
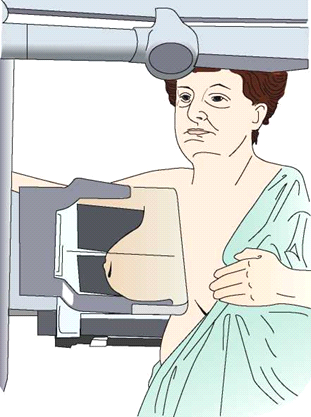
Ilustracja przedstawia pozycjonowanie pacjentki do badania mammograficznego w projekcji
Hałas podczas badania tomografii rezonansu magnetycznego jest efektem ubocznym pracy
Który artefakt jest widoczny na skanie tomografii komputerowej?
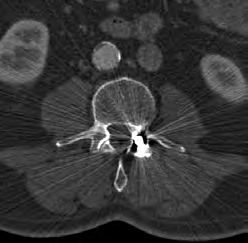
Skrótem CTV w radioterapii oznacza się
Jak zgodnie ze standardem należy ustawić pacjenta do badania rentgenowskiego w skosie tylnym prawym?
Dawka graniczna wyrażona jako dawka skuteczna (efektywna), dla osób zawodowo narażonych na działanie promieniowania jonizującego wynosi w ciągu roku kalendarzowego
Brak odpowiedzi na to pytanie.
W sekwencji echa spinowego obraz T2-zależny uzyskuje się przy czasie repetycji TR
Brak odpowiedzi na to pytanie.
W badaniu cystografii wstępującej środek kontrastowy należy podać
Brak odpowiedzi na to pytanie.
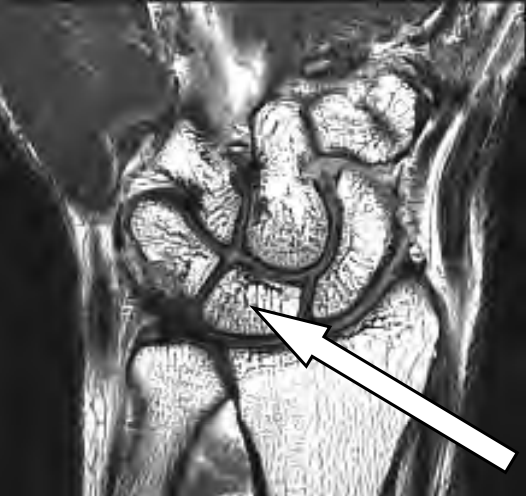
Na obrazie RM nadgarstka lewego strzałką oznaczono kość
Brak odpowiedzi na to pytanie.
Którą metodą zostało wykonane badanie kręgosłupa zobrazowane na zdjęciu?
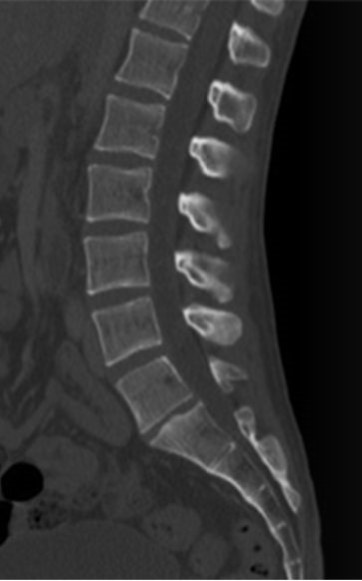
Brak odpowiedzi na to pytanie.
W radiologii stomatologicznej ząb o numerze 23 to kieł
Brak odpowiedzi na to pytanie.
Jakie symbole mają odprowadzenia kończynowe dwubiegunowe w badaniu EKG?
Brak odpowiedzi na to pytanie.
Na elektrokardiogramie zarejestrowano
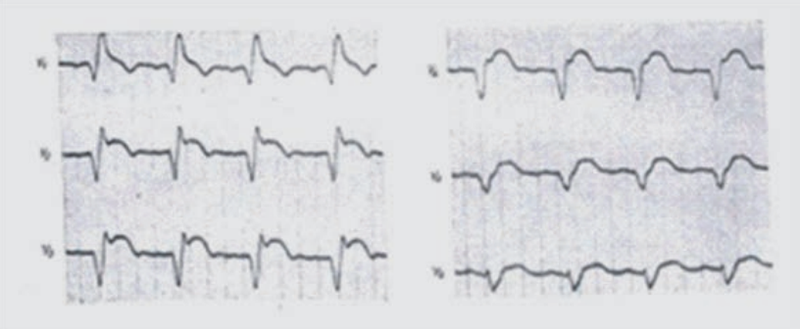
Brak odpowiedzi na to pytanie.
Zamieszczony obraz został wykonany metodą
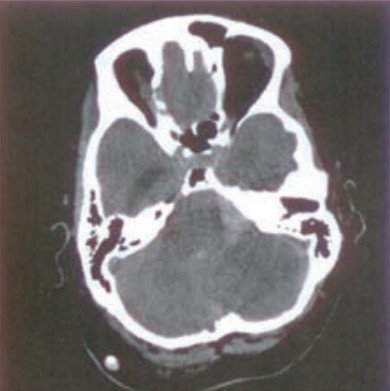
Brak odpowiedzi na to pytanie.
Który obszar napromieniania wskazano na ilustracji strzałką?
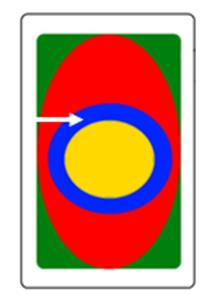
Brak odpowiedzi na to pytanie.
Celem radioterapii paliatywnej nie jest
Brak odpowiedzi na to pytanie.
Bezwzględnym przeciwwskazaniem do wykonania badania rezonansem magnetycznym jest
Brak odpowiedzi na to pytanie.
Urografia polega na
Brak odpowiedzi na to pytanie.
Na radiogramie stopy uwidocznione jest złamanie trzonu
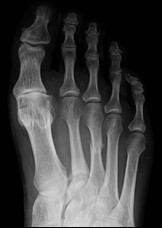
Brak odpowiedzi na to pytanie.
Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest
Brak odpowiedzi na to pytanie.
Do zadań technika elektroradiologa w pracowni hemodynamicznej należy
Brak odpowiedzi na to pytanie.
Który środek kontrastujący stosuje się w badaniu metodą rezonansu magnetycznego?
Brak odpowiedzi na to pytanie.
Na elektrokardiogramie uwidoczniono
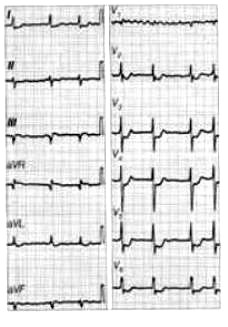
Brak odpowiedzi na to pytanie.
Na radiogramie czaszki strzałką zaznaczono
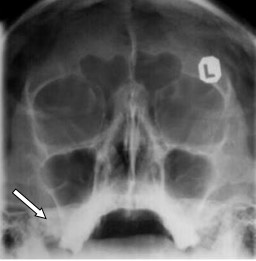
Brak odpowiedzi na to pytanie.
Jak oznacza się w systemie międzynarodowym czwarty górny ząb mleczny po stronie prawej?
Brak odpowiedzi na to pytanie.
Po zakończeniu badania angiograficznego należy zapisać w dokumentacji medycznej pacjenta:
Brak odpowiedzi na to pytanie.
Do zdjęcia rentgenowskiego żeber w projekcji skośnej tylnej pacjenta należy ustawić
Brak odpowiedzi na to pytanie.
W radiografii mianem SID określa się
Brak odpowiedzi na to pytanie.
Którą strukturę anatomiczną i w jakiej projekcji uwidoczniono na radiogramie?
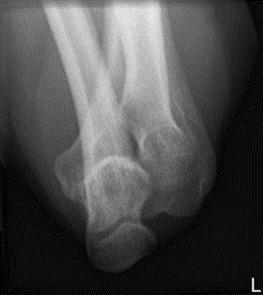
Brak odpowiedzi na to pytanie.
Którą kość zaznaczono strzałką na radiogramie stopy?
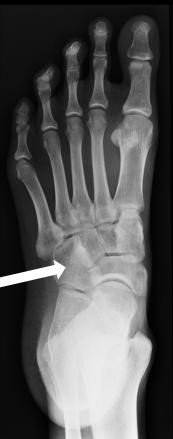
Brak odpowiedzi na to pytanie.
Na którym obrazie TK uwidoczniony jest artefakt spowodowany ruchami oddechowymi pacjenta?
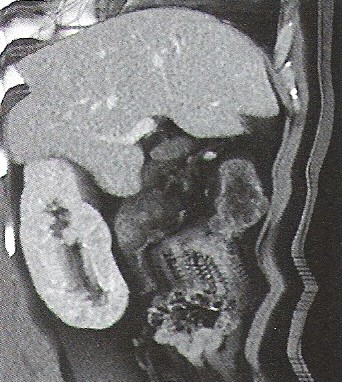
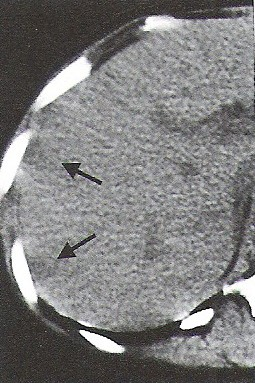

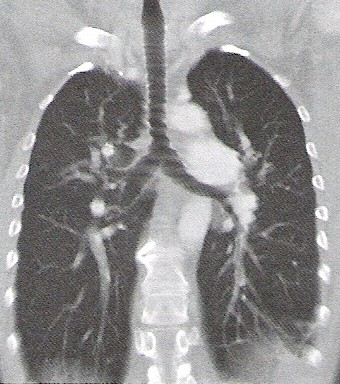
Brak odpowiedzi na to pytanie.
Na radiogramie TK głowy strzałką wskazano
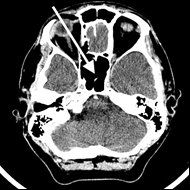
Brak odpowiedzi na to pytanie.
Wyniosłość międzykłykciowa znajduje się na nasadzie
Brak odpowiedzi na to pytanie.
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
Brak odpowiedzi na to pytanie.
Chorobą układu oddechowego typu obturacyjnego jest
Brak odpowiedzi na to pytanie.
Na radiogramie uwidoczniono złamanie
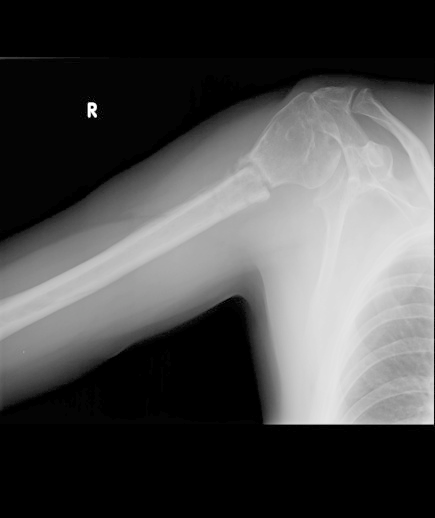
Brak odpowiedzi na to pytanie.
W celu unieruchomienia okolicy badanej podczas wykonywania zdjęcia nadgarstka u osoby dorosłej należy zastosować
Brak odpowiedzi na to pytanie.