Pytanie 1
Na radiogramie strzałką oznaczono
Wynik: 30/40 punktów (75,0%)
Wymagane minimum: 20 punktów (50%)
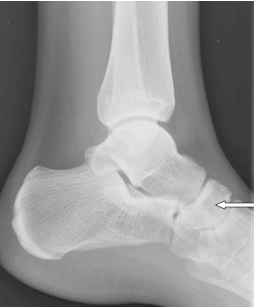
Na radiogramie strzałką oznaczono

W diagnostyce mammograficznej punktowy ucisk sutka stosuje się w projekcji
Cholangiografia to badanie radiologiczne
Brachyterapia wewnątrzjamowa jest wykorzystywana podczas leczenia nowotworu
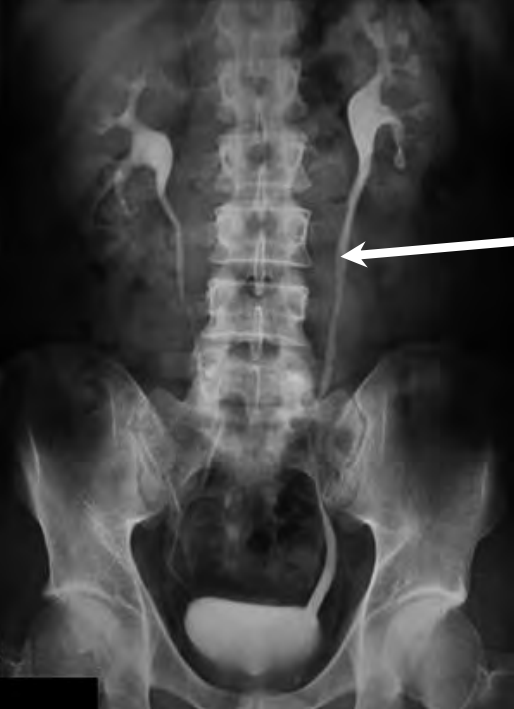
Na prawidłowo przedstawionym radiogramie badania kontrastowego strzałką zaznaczono
W której technice obrazowania zostają zarejestrowane jednocześnie dwa przeciwbieżne kwanty promieniowania gamma o równej energii 511 keV?
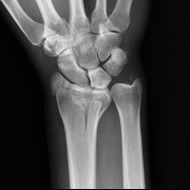
Na obrazie radiologicznym nadgarstka uwidoczniono złamanie nasady
W których projekcjach podstawowych wykonuje się standardowe badanie mammograficzne?
Które urządzenia pomocnicze służą do unieruchomienia pacjenta do zabiegu radioterapii?
Którą strukturę anatomiczną oznaczono na zamieszczonym obrazie rezonansu magnetycznego?
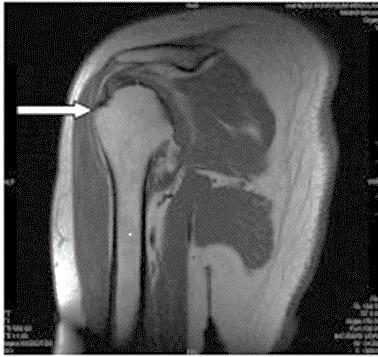
Do badania MR nadgarstka pacjenta należy ułożyć
W badaniu MR nadgarstka w ułożeniu na supermana pacjent leży na
Zgodnie z obowiązującymi przepisami powierzchnia gabinetu rentgenowskiego, w którym jest zainstalowany zestaw rentgenowski do badań naczyniowych, powinna wynosić
Wiązka elektronów najczęściej stosowana jest do leczenia zmian nowotworowych w obrębie
Zamieszczony elektrokardiogram przedstawia
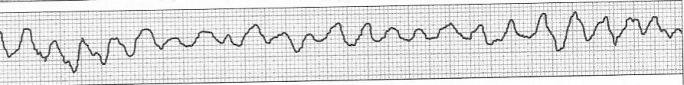
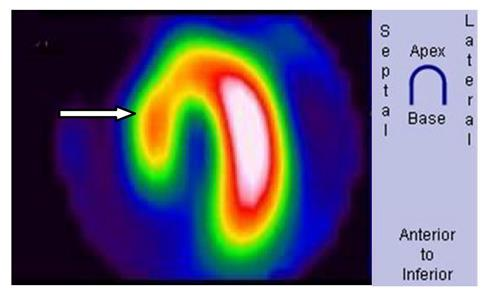
„Ognisko zimne” w obrazie scyntygraficznym określa się jako
Obszary napromieniania w technice IMRT w trakcie wykonywania zabiegu radioterapeutycznego wyznacza
Zestaw rentgenogramów przedstawia
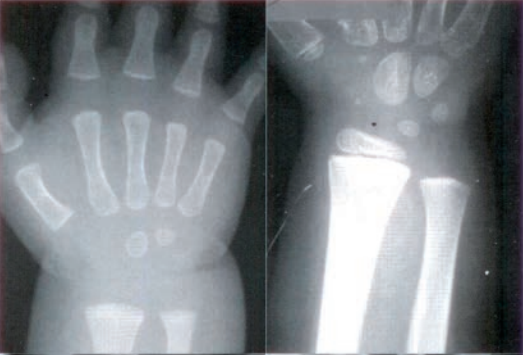
Jaki jest cel stosowania bolusa w radioterapii?
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz
Zarejestrowany na obrazie TK artefakt jest spowodowany
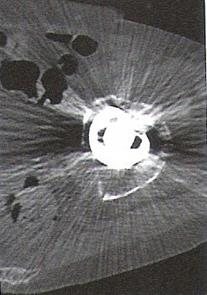
Przy ułożeniu do zdjęcia kręgów szyjnych CIII-CVII w projekcji przednio-tylnej lampa może być odchylona o kąt
Wskaż osłonę radiologiczną, która jest stosowana w pracowniach radiodiagnostyki stomatologicznej.




W sekwencji echa spinowego obraz T2-zależny uzyskuje się przy czasie repetycji TR
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
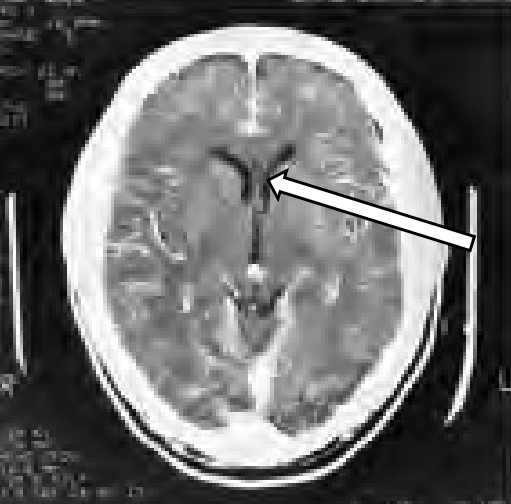
Którą strukturę anatomiczną oznaczono na skanie TK głowy?
Fala głosowa rozchodzi się
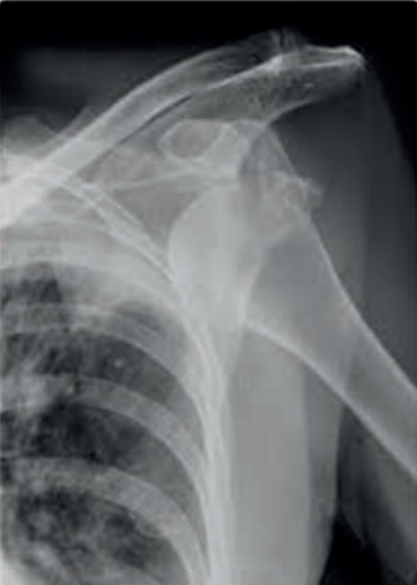
Którą patologię uwidoczniono na zamieszczonym rentgenogramie?
Który załamek odzwierciedla szybką repolaryzację komór w zapisie EKG?
W medycynie nuklearnej wykorzystuje się:
Który środek ochrony radiologicznej należy zastosować podczas badania czaszki 53-letniego pacjenta za pomocą tomografii komputerowej?
W badaniu audiometrycznym rezerwa ślimakowa to odległość między krzywą
W standardowym badaniu EEG elektrody P3, P4 i Pz umieszcza się na skórze głowy pacjenta nad płatami
Do zdjęcia lewobocznego kręgosłupa lędźwiowo-krzyżowego pacjenta należy ułożyć na boku
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
Do środków kontrastujących negatywnych należą
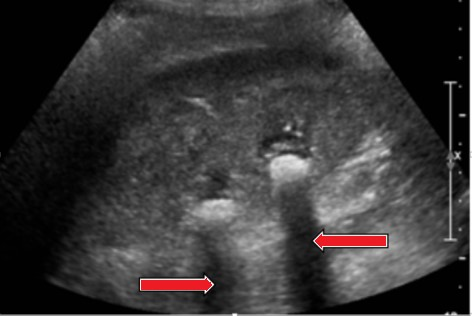
Który artefakt wskazano strzałkami na obrazie USG nerki?
W scyntygrafii wykorzystywane są głównie radioizotopy emitujące promieniowanie
Kolimator wielolistkowy w akceleratorze liniowym jest stosowany do
Na obrazie scyntygrafii perfuzyjnej serca strzałką wskazano ścianę