Pytanie 1
W kulturze bakterii i grzybów nie należy używać jako pożywki
Wynik: 16/40 punktów (40,0%)
Wymagane minimum: 20 punktów (50%)
W kulturze bakterii i grzybów nie należy używać jako pożywki
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Jakim wskaźnikiem posługujemy się w argentometrycznym oznaczaniu chlorków w roztworze soli fizjologicznej?
Możliwość stwierdzenia obecności jonów żelaza (III) w próbce można uzyskać poprzez dodanie roztworu
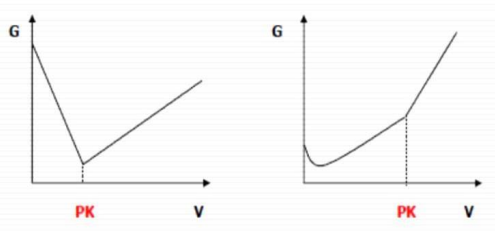
Wykresy przedstawiają przebieg krzywych miareczkowania
Zestaw zawierający palnik gazowy, statyw, łącznik, pierścień, trójkąt ceramiczny oraz tygiel porcelanowy z pokrywką jest stosowany w trakcie oznaczeń
Dokładność metody definiowana jest na podstawie ustalonej wartości
Ezy oraz igły stosowane w mikrobiologii należy wyjaławiać
Wskaźnik zanieczyszczenia wody bakterią jelitową - miano coli równe 10 - oznacza, że
Obecność jasnofioletowego zabarwienia płomienia palnika podczas analiz chemicznych wskazuje na obecność w roztworze jonów
Dla czterech różnych próbek gleb lekkich o odczynie kwaśnym oznaczono zawartość metali w mg/kg suchej masy. Wyniki zestawiono w tabeli:
Graniczne zawartości metali śladowych w powierzchniowej warstwie gleb bardzo lekkich | |||||
|---|---|---|---|---|---|
| Stopień zanieczyszczenia gleb | Zawartość metali w mg/kg suchej masy | ||||
| Pb | Cd | Zn | Cu | Ni | |
| 0 zawartość naturalna | 30 | 0,3 | 50 | 15 | 10 |
| 1 zawartość podwyższona | 70 | 1 | 100 | 30 | 30 |
| 2 słabe zanieczyszczenie | 100 | 2 | 300 | 50 | 50 |
| 3 średnie zanieczyszczenie | 500 | 3 | 700 | 150 | 100 |
| 4 silne zanieczyszczenie | 2500 | 5 | 3000 | 300 | 400 |
| 5 bardzo silne zanieczyszczenie | >2500 | >5 | >3000 | >300 | >400 |
| Metal | Próbka 1. | Próbka 2. | Próbka 3. | Próbka 4. |
|---|---|---|---|---|
| Pb | 180,0 | 15,0 | 25,0 | 29,0 |
| Cd | 1,6 | 0,3 | 0,2 | 0,6 |
| Zn | 40,0 | 55,5 | 48,0 | 37,0 |
| Cu | 328,0 | 25,0 | 8,0 | 56,0 |
| Ni | 135,0 | 8,0 | 8,0 | 19,0 |
Jakie sole nie podlegają procesowi hydrolizy?
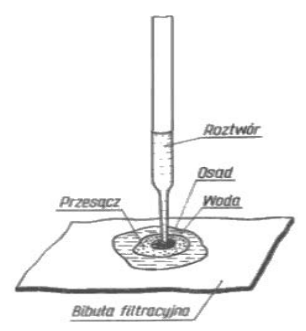
Na rysunku przedstawiono wykonanie analizy metodą
Urządzenie Abla-Pensky'ego jest używane do pomiaru temperatury
Ogólna twardość próbki wody stosowanej w technologiach wynosi 16,5°n, a twardość węglanowa osiąga 7,2°n. Jaką wartość ma twardość stała?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Jakie właściwości cieczy określa areometr?
W próbce wody, w której stwierdzono obecność 60,0 mg żelaza, dokonano oznaczenia jego zawartości za pomocą spektrofotometrii, uzyskując wynik 59,1 mg. Jaki jest błąd względny tego oznaczenia?
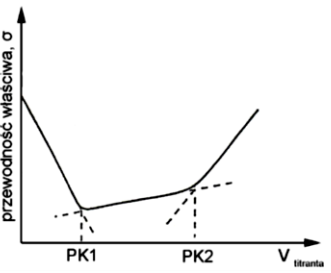
Rysunek przedstawia krzywą miareczkowania
Dawka substancji, która powoduje pierwsze widoczne zmiany w organizmie, nazywana jest
Rozpuszczono próbkę technicznego chlorku sodu w wodzie, a jony chlorkowe strącono przy pomocy AgNO3, w postaci AgCl, którego masa po wysuszeniu wyniosła 1,5000 g. Oblicz ilość chloru w analizowanej próbce. Mnożnik analityczny dla chloru w AgCl to 0,2474.
Określenie miedzi w postaci czystego osadu pierwiastka przeprowadza się w trakcie analizy
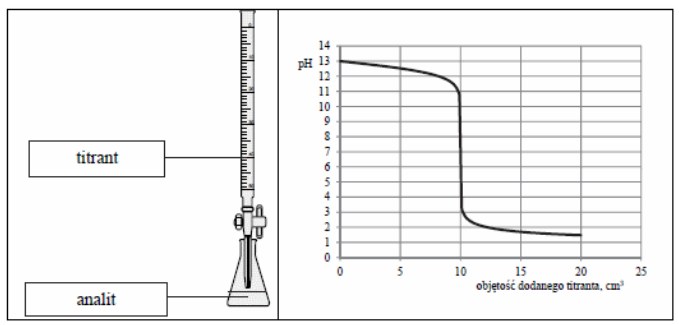
Na podstawie rysunku analitem może być roztwór
Jaką metodę wykorzystuje się do identyfikacji cukrów redukujących?
Które z przedstawionych reakcji zachodzą na elektrodach platynowych podczas elektrolizy azotanu(V) miedzi(II)?
| A. | K(–) Cu2+ + 2e → Cu | A(+) 2H+ + 2e → H2 |
| B. | K(–) 2H2O → O2 + 4H+ + 4e | A(+) Cu2+ + 2e → Cu |
| C. | K(–) Cu2+ + 2e → Cu | A(+) 2H2O → O2 + 4H+ + 4e |
| D. | K(–) Cu2+ + 2e → Cu | A(+) 4OH– → O2 + 2H2O + 4e |
| Zawartość chlorowodoru w próbce można obliczyć wg wzoru: mB = CA · VA⁄1000 · pB⁄pA · MB w którym: mB – masa analizowanej substancji [g] CA – stężenie titranta [mol/dm3] VA – objętość titranta [cm3] pA i pB – współczynniki stechiometryczne reakcji, odpowiednio titranta i substancji oznaczanej MB – masa molowa substancji oznaczanej; 36,46 g/mol Do oznaczenia zużyto średnio 20,0 cm3 titranta, którego stężenie wynosiło 0,1000 mol/dm3. Obliczono masę próbki, która wyniosła 0,07292 g. |
| A. | HCl + NaOH → NaCl + H2O |
| B. | 3HCl + Al(OH)3 → AlCl3 + 3H2O |
| C. | 2HCl + Na2CO3 → 2NaCl + H2O + CO2 |
| D. | 2HCl + Na2B4O7 + 5H2O → 4H3BO3 + 2NaCl |
Który z poniższych związków chemicznych stanowi kluczowe źródło azotu organicznego w podłożach hodowlanych?
Wyznacz refrakcję molową (Rm) dla kwasu octowego korzystając z danych zawartych w tabeli.
Rm = ∑a ∙ Ra gdzie: a – liczba atomów jednego rodzaju, Ra – refrakcja atomowa

W procedurze analitycznej zapisano:
Ile wynosi zawartość procentowa Na2B4O7·10H2O w badanej próbce boraksu, jeżeli na zmiareczkowanie 0,3 g próbki zużyto 15,4 cm3 roztworu NaOH?
| 1 cm3 roztworu NaOH o stężeniu 0,1 mol/dm3 odpowiada 19,07 mg tetraboranu sodu Na2B4O7 · H2O |
Na zamieszczonym schemacie trawienia białek cyfrą 1 oznaczono

Po przeprowadzeniu procesu elektrolizy wodnego roztworu określonego związku, na katodzie pojawił się wodór, a na anodzie tlen. Który z tych związków został poddany elektrolizie?
Przedstawiony wzór opisuje titrant stosowany podczas miareczkowania
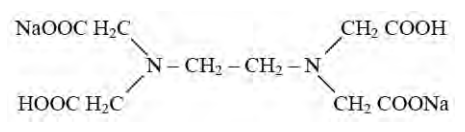
Do zmiareczkowania 30,0 cm3 roztworu HCl o stężeniu 0,1 mol/dm3 użyto KOH. Jaką masę KOH zawierała ta odważka?
MKOH = 56 g/mol
Roztwór tiocyjanianu amonu NH4SCN jest wykorzystywany jako titrant w oznaczaniu bromków przy użyciu metody miareczkowania?
Jakie badanie chemiczne dotyczące wody przeprowadza się przy użyciu miareczkowania kompleksometrycznego?
Spektrofotometria absorpcyjna w zakresie UV-Vis polega na określaniu
W celu wykonania analizy mieszaniny kationów grup I - V należy wybrać sprzęt oznaczony w tabeli numerami:
| Palnik gazowy | Kolba stożkowa | Drut platynowy na pręcie szklanym | Biureta | Płytka ceramiczna do eksperymentów kroplowych | Kolba miarowa |
| 1 | 2 | 3 | 4 | 5 | 6 |
Skróconym badaniom poddano próbki wody z 4 ujęć. Wyniki zapisano w tabeli. Na podstawie analizy danych zawartych w tabelach wskaż zestaw próbek spełniających wymagania jakościowe.
| Wyniki badań próbek wody z 4 ujęć | ||||
|---|---|---|---|---|
| Wskaźnik organoleptyczny | Próbka 1 | Próbka 2 | Próbka 3 | Próbka 4 |
| Barwa (Pt) | 10 | 20 | 15 | 20 |
| Odczyn (pH) | 7,5 | 6,5 | 6,8 | 8,8 |
| Mętność | 5 | 4 | 3 | 5 |
| Zapach | 3 – naturalny, nieuciążliwy | 3 – naturalny, nieuciążliwy | 3 – nieuciążliwy, wyczuwalny zapach chloru | 3 – naturalny, nieuciążliwy |
| Zawiesiny, plamy oleju, itp. | Niewidoczne w szklanych naczyniach | Niewidoczne w szklanych naczyniach | Niewidoczne w szklanych naczyniach | Niewidoczne w szklanych naczyniach |
| Warunki organoleptyczne, jakim powinna odpowiadać woda do picia i na potrzeby gospodarcze | ||||
| Lp. | Wskaźniki organoleptyczne, Nazwa substancji | Jednostka miary | Najwyższa dopuszczalna dawka lub przedział | |
| 1 | Barwa (Pt) | mg · dm-3 | 20 | |
| 2 | Odczyn (pH) | ---- | 6,5 – 8,5 | |
| 3 | Mętność | mg · dm-3 | 5 | |
| 4 | Zapach | ---- | 3 – naturalny, nieuciążliwy, dopuszczalny zapach chloru przy dezynfekcji chlorem | |
| 5 | Zawiesiny, plamy oleju itp. | ---- | Niewidoczne w szklanych naczyniach | |
Analiza składników chemicznych próbki substancji organicznej odbywa się w badaniu