Pytanie 1
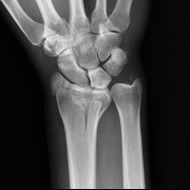
Na obrazie radiologicznym nadgarstka uwidoczniono złamanie nasady
Wynik: 37/40 punktów (92,5%)
Wymagane minimum: 20 punktów (50%)
Na obrazie radiologicznym nadgarstka uwidoczniono złamanie nasady

Jaka jest standardowa odległość OF do wykonania rentgenowskich zdjęć kości i stawów kończyny górnej?
Jakie są wielkości mocy dawki stosowanej w brachyterapii HDR?
Który typ głowicy ultrasonograficznej przedstawiono na ilustracji?

Zamieszczone obrazy związane są z badaniem
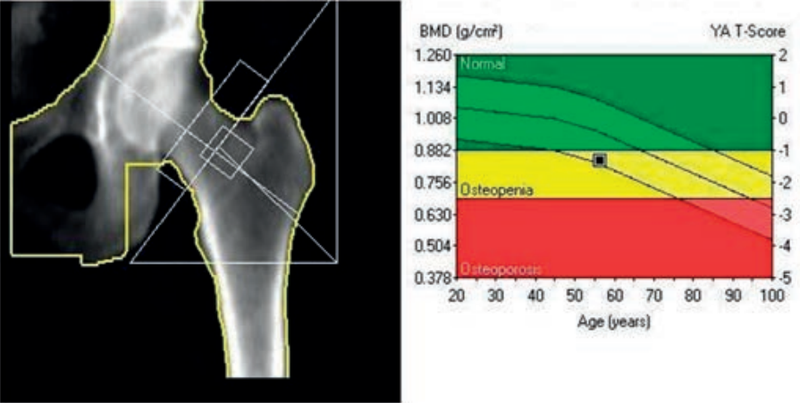
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
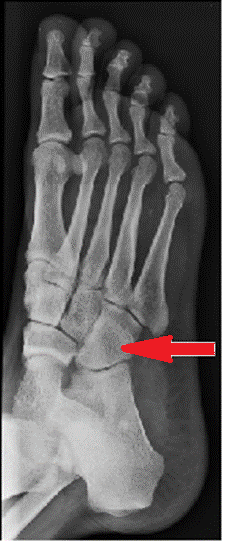
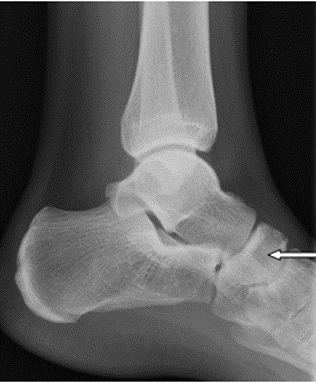
Na radiogramie stopy strzałką wskazano kość
W pracowni ultrasonograficznej technik elektroradiolog nie korzysta z przepisów dotyczących
Jaki jest cel stosowania bolusa w radioterapii?
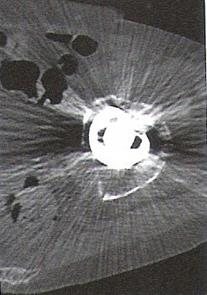
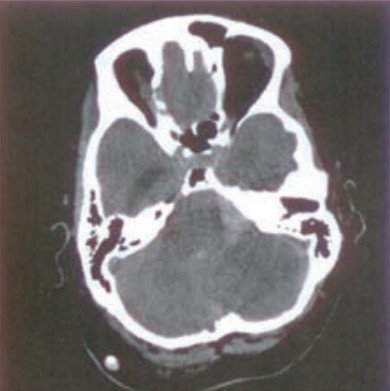
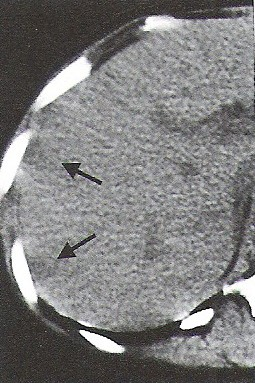
Zarejestrowany na obrazie TK artefakt jest spowodowany
Jaki kolor ma warstwa korowa kości w badaniu MR na obrazie T1- zależnym?
Na zamieszczonej rycinie przedstawiono
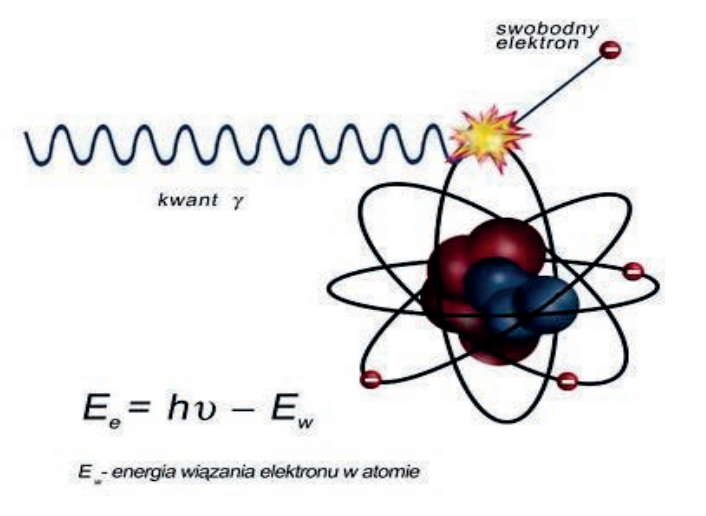
W metodzie RM (rezonansu magnetycznego) po umieszczeniu pacjenta w silnym, stałym polu magnetycznym dochodzi do oddziaływania
Zamieszczony obraz został wykonany metodą
W badaniu EEG elektrody referencyjne przymocowane do płatka ucha to
Zarejestrowane na elektrokardiogramie miarowe fale f w kształcie „zębów piły” poprzedzielane prawidłowymi zespołami QRS są charakterystyczne dla
Elementem pomocniczym w radioterapii, zapewniającym powtarzalność ułożenia w pozycji terapeutycznej, a także unieruchomienie pacjenta, jest
Skrótem HRCT (High Resolution Computed Tomography) określa się tomografię komputerową
Ligand stosuje się
W celu maksymalnego ograniczenia dawki promieniowania badanie rentgenowskie u dzieci należy wykonać
Jaki rozmiar kasety należy zastosować, wykonując standardowe zdjęcie stawu kolanowego w projekcji bocznej?
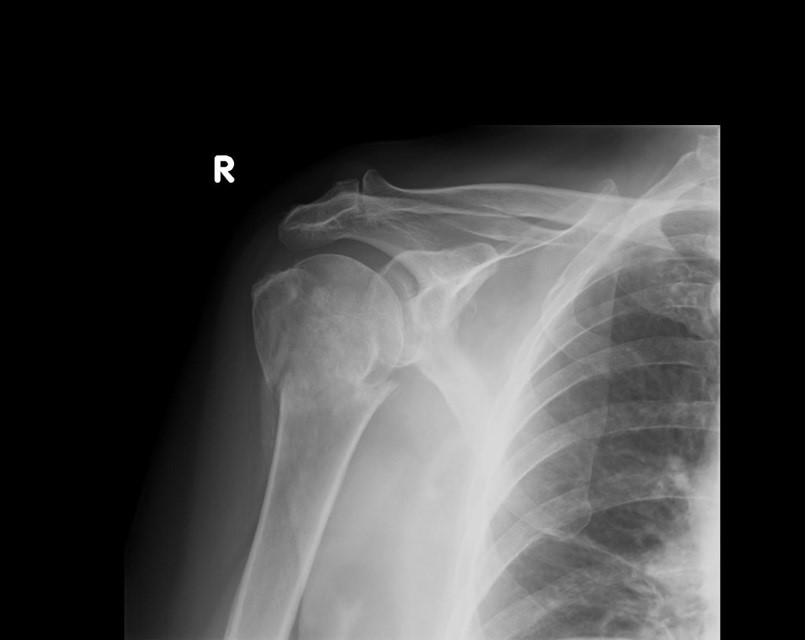
Na radiogramie uwidoczniono złamanie
Znak umieszczony w pracowni rezonansu magnetycznego zakazuje wstępu osobom

Teleradioterapia 4D na etapie planowania leczenia wykorzystuje obrazy
Na zamieszczonym radiogramie strzałką oznaczono kość
Droga przewodnictwa powietrznego fali akustycznej przebiega przez
Wskaż roczną dawkę graniczną dla osób zatrudnionych w warunkach narażenia na promieniowanie jonizujące.
Który wynik badania tympanometrycznego potwierdza, że słuch badanego pacjenta jest w granicach normy?
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
Które zdjęcia należy wykonać pacjentom z chorobą reumatoidalną stawów kolanowych?
W systemie międzynarodowym ząb pierwszy przedtrzonowy po stronie lewej oznacza się symbolem
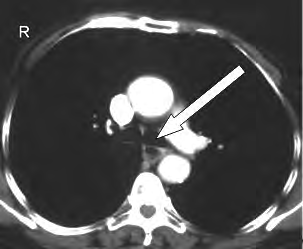
Na obrazie TK klatki piersiowej w przekroju poprzecznym strzałką oznaczono
Który z nowotworów jest hormonozależny?
Parametrem krwi, który powinien zostać oznaczony u pacjenta przed wykonaniem badania MR z kontrastem, jest
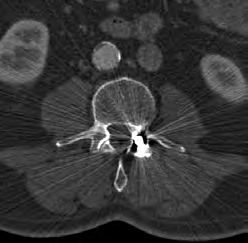
Który artefakt jest widoczny na skanie tomografii komputerowej?
Jak oznacza się w radioterapii obszar tkanek zawierający GTV i mikrorozsiewy w fazie niewykrywalnej klinicznie?
Podczas wykonywania badania EEG elektrodę P4 umieszcza się w okolicy
Który program wtórnej rekonstrukcji obrazów TK pozwala na odwzorowanie wnętrza jelita grubego, tchawicy i oskrzeli?
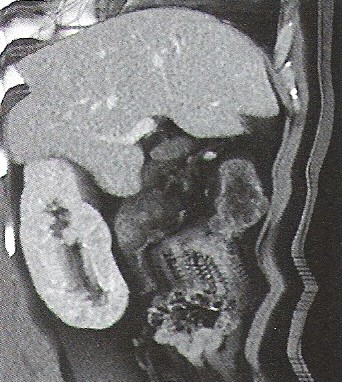
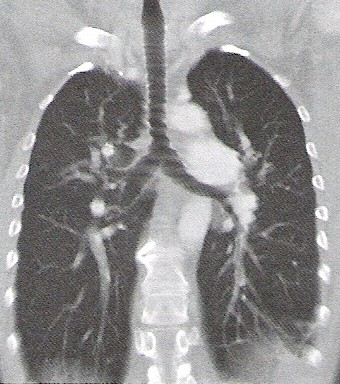
Na którym obrazie TK uwidoczniony jest artefakt spowodowany ruchami oddechowymi pacjenta?

W badaniu EKG punktem przyłożenia odprowadzenia przedsercowego C2 jest